Clear Sky Science · it
Ingegneria genica del microambiente tumorale indotta da LOAd703 in combinazione con atezolizumab nel melanoma maligno metastatico: uno studio di fase I/II
Perché questo nuovo studio sul melanoma è importante
Per le persone con melanoma cutaneo avanzato che non risponde più alle potenti immunoterapie odierne, le opzioni terapeutiche sono limitate e spesso gravose. Questo studio mette alla prova un’idea diversa: utilizzare un virus ingegnerizzato geneticamente, iniettato direttamente nei tumori, insieme a un farmaco immunostimolante già in uso, per risvegliare le difese dell’organismo e riprendere il controllo sul cancro. I risultati preliminari suggeriscono che questo approccio può essere somministrato in sicurezza e potrebbe aiutare una quota significativa di pazienti la cui malattia aveva precedentemente resistito alla terapia standard.
Un cancro cutaneo ostinato che elude il trattamento
Il melanoma è uno dei tumori cutanei seri più comuni nei Paesi occidentali e la sua incidenza è aumentata considerevolmente negli ultimi decenni. I moderni farmaci che bloccano i checkpoint immunitari, che rimuovono i freni dalle cellule T, hanno trasformato gli esiti clinici, portando la sopravvivenza a cinque anni nel melanoma avanzato a circa la metà dei pazienti. Tuttavia molti tumori smettono infine di rispondere. Spesso questi tumori resistenti sono circondati da un ‘‘vicinato’’ freddo di cellule e molecole che tengono fuori le cellule immunitarie o le disattivano. Trovare modi per riprogettare questo microambiente tumorale in modo che le cellule T possano riconoscere e attaccare nuovamente il cancro è una priorità di ricerca importante.
Un virus progettato per rimodellare il microambiente tumorale
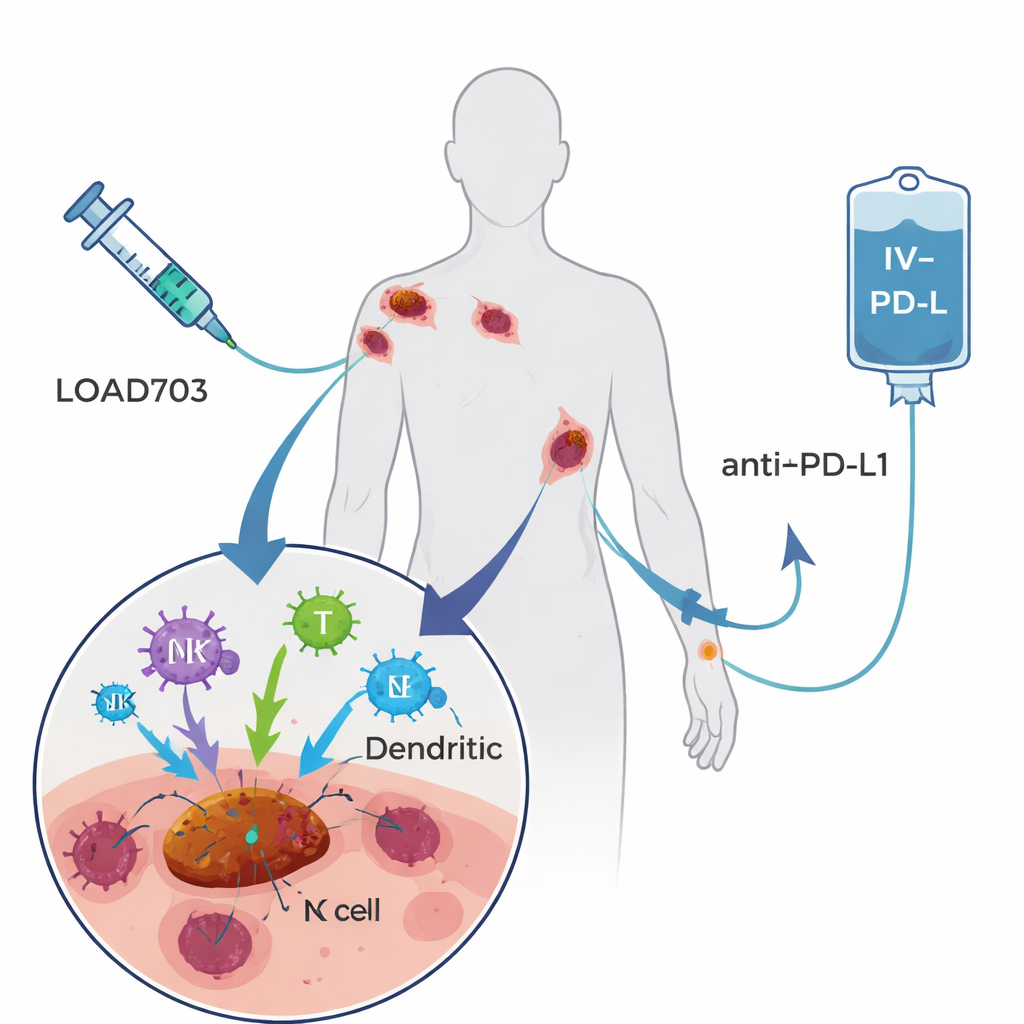
Il trattamento testato qui, chiamato LOAd703, è un adenovirus modificato — un tipo di virus del raffreddore comune — ingegnerizzato per svolgere due funzioni. Primo, tende a replicarsi e distruggere le cellule tumorali, una strategia nota come viroterapia oncolitica. Secondo, porta istruzioni genetiche per due potenti segnali immunostimolanti espressi sulle cellule infette. Questi segnali, CD40L e 4‑1BBL, favoriscono la maturazione delle sentinelle immunitarie professionali (cellule dendritiche) e la presentazione dei frammenti tumorali, e rafforzano ed espandono le cellule T e le cellule natural killer che combattono il cancro. I pazienti nello studio hanno ricevuto LOAd703 iniettato direttamente in uno o più tumori ogni tre settimane, insieme ad atezolizumab, un anticorpo già consolidato somministrato per via endovenosa che blocca il freno PD‑L1 sulle cellule T. L’ipotesi era che il virus trasformasse i tumori in fabbriche vaccinali in loco, mentre l’anticorpo mantenesse attive le cellule T rivitalizzate.
Chi è stato trattato e come sono andati
Lo studio di fase I/II ha arruolato 24 persone con melanoma in stadio IV che aveva chiaramente progredito nonostante almeno un trattamento precedente con inibitori di PD‑1; molti avevano ricevuto diverse linee di immunoterapia e farmaci target. Sono stati testati due livelli di dose del virus. Complessivamente la combinazione è stata ben tollerata. Gli effetti collaterali più comuni riconducibili al virus — febbre, brividi, nausea e sintomi simil‑influenzali — sono stati in gran parte lievi e temporanei. Solo due pazienti hanno avuto reazioni più gravi ma reversibili alla dose più alta, e nessuno ha dovuto interrompere il trattamento per problemi correlati al virus. Nella valutazione delle risposte tumorali, quattro pazienti (17%) hanno mostrato una riduzione misurabile dei tumori, e oltre la metà ha avuto almeno una stabilità di malattia per un certo periodo. A due anni dall’ingresso nello studio, quasi la metà dei partecipanti era ancora in vita, inclusi alcuni i cui esami hanno mostrato un controllo di lunga durata o una completa scomparsa della malattia rilevabile dopo il completamento della terapia.
Segnali che il sistema immunitario è stato riattivato
Per capire cosa stesse accadendo all’interno dei tumori e nel sangue, il team ha analizzato biopsie tissutali e campioni di sangue prelevati prima del trattamento e circa nove settimane dopo l’inizio. Nei tumori iniettati è stata osservata una maggiore attività di geni associati alle risposte immunitarie di tipo 1, inclusi marcatori di cellule T attivate e cellule natural killer, e molecole che aiutano queste cellule a entrare nei tumori dai vasi sanguigni vicini. Sono aumentati anche segnali associati alla presentazione dell’antigene — il processo con cui i frammenti tumorali vengono esposti alle cellule T — suggerendo che la terapia virale stesse trasformando il microambiente tumorale da soppressivo a più favorevole all’immunità. Nel sangue, diverse proteine legate all’immunità, incluso lo stesso PD‑L1, sono aumentate dopo la terapia, coerentemente con un’ampia attivazione delle vie immunitarie. I pazienti che hanno vissuto più a lungo tendevano a mostrare profili genici legati a una robusta funzione delle cellule T e a protezioni antivirali, mentre quelli con sopravvivenza più breve presentavano pattern associati a tipi cellulari soppressivi e segnali di rimodellamento tissutale.
Cosa potrebbe significare per le cure future
Questo è stato uno studio piccolo e a braccio singolo senza un gruppo di confronto, quindi i dati di sopravvivenza e di risposta vanno interpretati con cautela. Tuttavia, la combinazione di buona tollerabilità, attivazione immunitaria nei tumori e controllo della malattia incoraggiante in pazienti pesantemente pretrattati suggerisce che virus oncolitici ingegnerizzati come LOAd703 potrebbero aiutare a ri‑sensibilizzare il melanoma al blocco dei checkpoint — o persino mantenere i tumori sotto controllo da soli. I risultati supportano trial più grandi e controllati, eventualmente abbinando il virus ad altri farmaci che mirano il sistema immunitario, per chiarire quali pazienti traggono maggior beneficio e come integrare al meglio questa strategia nella cura del melanoma.
Citazione: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Parole chiave: melanoma, immunoterapia, virus oncolitico, microambiente tumorale, resistenza agli inibitori dei checkpoint