Clear Sky Science · it
Rilevamento massivamente parallelo basato su nanopori per il profiling di peptidi e l’identificazione delle proteine
Leggere le proteine una molecola alla volta
Le proteine sono i motori del funzionamento cellulare e sapere esattamente quali sono presenti, come vengono modificate e come interagiscono è fondamentale per comprendere salute e malattia. Gli strumenti standard odierni per studiare le proteine sono potenti ma spesso lenti, costosi e difficili da scalare. Questo articolo descrive un nuovo modo per ascoltare singoli frammenti proteici mentre passano attraverso un minuscolo foro in una membrana, usando l’intelligenza artificiale per trasformare quei segnali in impronte dettagliate. L’approccio potrebbe aprire la strada a test più rapidi ed economici per monitorare marker di malattia e verificare quanto siano efficaci nella pratica gli anticorpi usati in ricerca e diagnostica.
Trasformare le proteine in pezzi leggibili
I ricercatori si basano sulla tecnologia dei nanopori, sviluppata originariamente per il sequenziamento del DNA. Nel loro sistema, le proteine naturali vengono prima tagliate in frammenti più corti chiamati peptidi e modificati delicatamente in modo che ciascun pezzo possa essere legato a entrambe le estremità a brevi tratti di DNA. Questo crea una struttura “Oligo–Peptide–Oligo” che si comporta bene nei dispositivi a nanopori pensati per il DNA. Il team utilizza un enzima di taglio specifico che tende a lasciare un particolare amminoacido, la lisina, all’estremità di ciascun frammento, rendendo la chimica più prevedibile e compatibile con molte proteine diverse. Il risultato finale è una libreria purificata di molte di queste costruzioni peptido–DNA preparata in poche ore.
Ascoltare con molti nanopori contemporaneamente
Per rilevare effettivamente questi frammenti peptidici, gli autori usano un array di nanopori biologici—minimi fori costituiti da proteine inseriti in una membrana e collegati a elettrodi. Quando viene applicata una tensione, le strutture DNA–peptide–DNA vengono tirate, una alla volta, attraverso ciascun poro da un motore molecolare. Man mano che il peptide passa attraverso la parte più stretta, blocca parzialmente il flusso di ioni, modificando la corrente elettrica. Poiché la piattaforma usa 256 pori in parallelo e può raccogliere oltre 100.000 eventi di questo tipo da una singola libreria in due ore, produce un flusso massiccio di segnali a singola molecola che catturano come ogni specifico peptide interagisce con il poro. 
Da segnali rumorosi a impronte distintive
In superficie, queste tracce di corrente appaiono rumorose e variabili; lo stesso peptide può entrare in orientamenti diversi e assumere conformazioni differenti. Misure riassuntive tradizionali come la corrente media e la durata dell’evento spesso si sovrappongono fra peptidi simili. Il progresso chiave di questo lavoro è una pipeline di intelligenza artificiale in due fasi. Prima, una rete neurale convoluzionale profonda viene addestrata su grandi quantità di tracce per classificare quale peptide ha prodotto ciascun pattern. Secondo, il team crea “matrici di densità” che riassumono come il segnale tende a variare nel corso di ciascun evento, trasformando in pratica nuvole di tracce rumorose in impronte 2D stabili. Vengono conservate solo le letture i cui pattern temporali dettagliati corrispondono a queste impronte. Questa strategia CNN più impronta migliora l’accuratezza fino a circa il 99% per peptidi di test e può distinguere in modo affidabile frammenti che differiscono per un singolo amminoacido, certi isomeri e molte comuni modifiche chimiche che le proteine acquisiscono nelle cellule.
Controllare gli anticorpi e identificare proteine intere
Poiché gli anticorpi riconoscono brevi tratte di proteine, gli autori applicano la loro piattaforma per mappare quali frammenti diversi anticorpi commerciali legano realmente. Mescolando pezzi peptidici sovrapposti di un precursore ormonale, arricchendo quelli legati da ciascun anticorpo e poi leggendo il loro contenuto con il sistema a nanopori, possono individuare le regioni di legame preferite e mostrare quando coppie di anticorpi raccomandate dai fornitori riconoscono effettivamente lo stesso sito e sono poco compatibili per saggi a sandwich. In un altro test, esaminano una nota sequenza tag e quattro varianti quasi identiche, dimostrando che il numero relativo di letture a nanoporo per ciascun peptide rispecchia da vicino la forza di legame con l’anticorpo, in accordo con misurazioni più laboriose basate su superfici. Infine, dimostrano l’identificazione di proteine: addestrano il sistema sulle impronte peptidiche di tre proteine umane, poi digeriscono alla cieca le proteine intere e mostrano che il pattern combinato di peptidi classificati è sufficiente per riconoscere correttamente quale proteina è quale, anche in presenza di frammenti ambigui o mancanti. 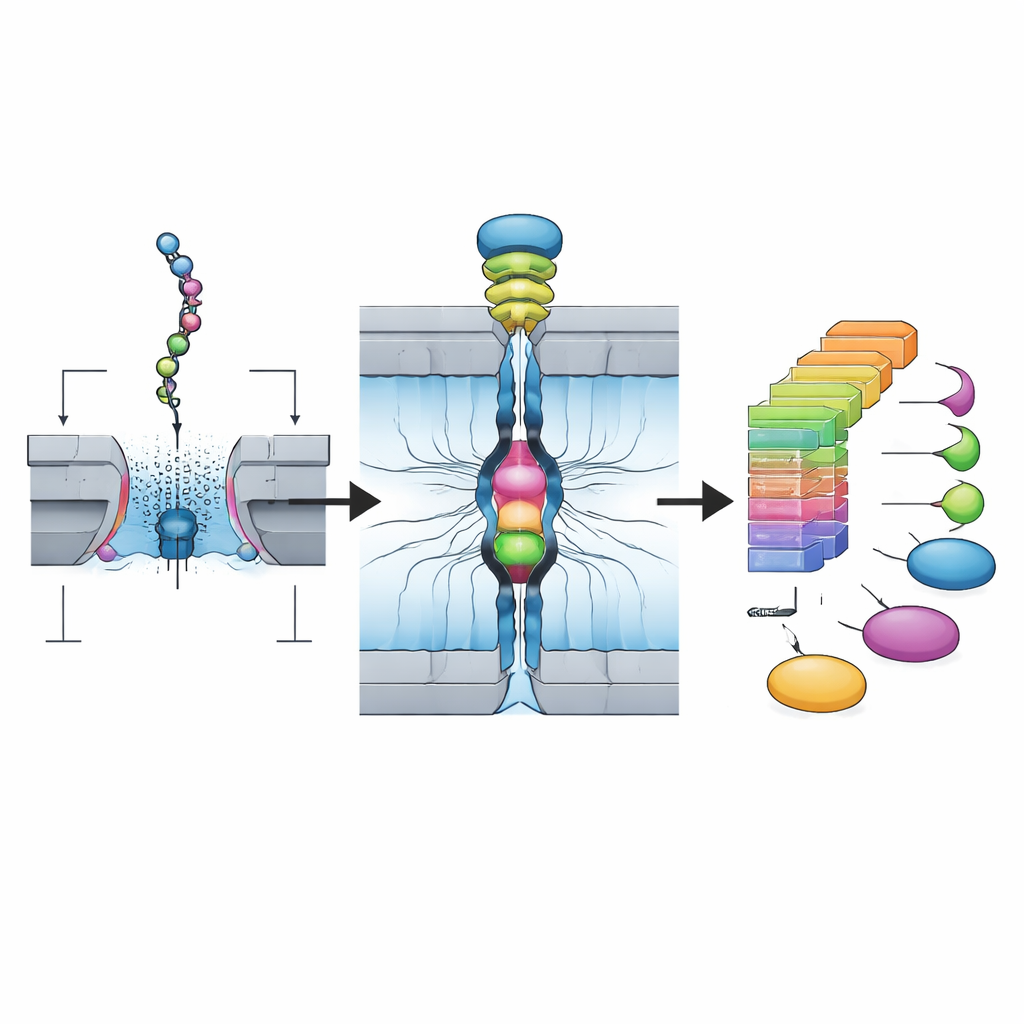
Perché questo conta per i test futuri
In termini pratici, lo studio mostra che un sequenziatore a nanopori in stile DNA, accoppiato a chimica intelligente e IA, può funzionare come un “stetoscopio” altamente parallelo per frammenti proteici. Invece di dover leggere ogni amminoacido in ordine, il sistema si appoggia su impronte statistiche ricche ottenute da migliaia di eventi a singola molecola per distinguere sottili differenze di carica, dimensione e modificazione. Ciò consente controlli rapidi e a basso costo della qualità degli anticorpi e offre una strada per riconoscere proteine intere a partire dai loro pattern peptidici. Pur restando dei limiti—come difficoltà con certi tipi di peptidi e la necessità di buoni dati di addestramento—il lavoro presenta una pipeline end-to-end che potrebbe avvicinare l’analisi proteica ad alto rendimento ai laboratori di ricerca di routine e, in futuro, alla diagnostica clinica.
Citazione: Wang, J., Chen, J., Pan, H. et al. Nanopore-based massively parallel sensing for peptide profiling and protein identification. Nat Commun 17, 3058 (2026). https://doi.org/10.1038/s41467-026-69628-1
Parole chiave: rilevamento con nanopori, proteomica, impronte digitali di peptidi, validazione di anticorpi, identificazione delle proteine