Clear Sky Science · it
Farmaci “incapsulati” attivabili con luce per il rilascio fotocatalitico di ossido nitrico e anestetici per analgesia antibatterica
Combattere germi e dolore contemporaneamente
Le infezioni batteriche non minacciano solo la nostra salute; provocano anche dolore—e spesso intenso. I trattamenti standard di solito mirano ai germi ma lasciano i pazienti dipendenti da analgesici separati, che possono esaurirsi rapidamente o causare effetti collaterali. Questo studio presenta un farmaco controllabile con la luce che mira a uccidere i batteri e alleviare il dolore in un unico passaggio coordinato, offrendo uno sguardo su cure delle infezioni più intelligenti e confortevoli.
Un’idea di farmaco due-in-uno
I ricercatori hanno costruito l’approccio attorno alla tetracaina, un anestetico locale noto e usato per intorpidire pelle e nervi. Hanno legato chimicamente l’ossido nitrico, una piccola molecola gassosa nota per le sue potenti azioni antibatteriche e antinfiammatorie, alla tetracaina. Questo ha creato un “pro-farmaco” chiamato TTC-NO che è in gran parte inattivo fino a quando non viene attivato. TTC-NO è stato quindi confezionato, insieme a una molecola ausiliaria fotosensibile, in piccole bolle polimeriche chiamate micelle che possono muoversi in ambienti acquosi come il sangue o il fluido tissutale. 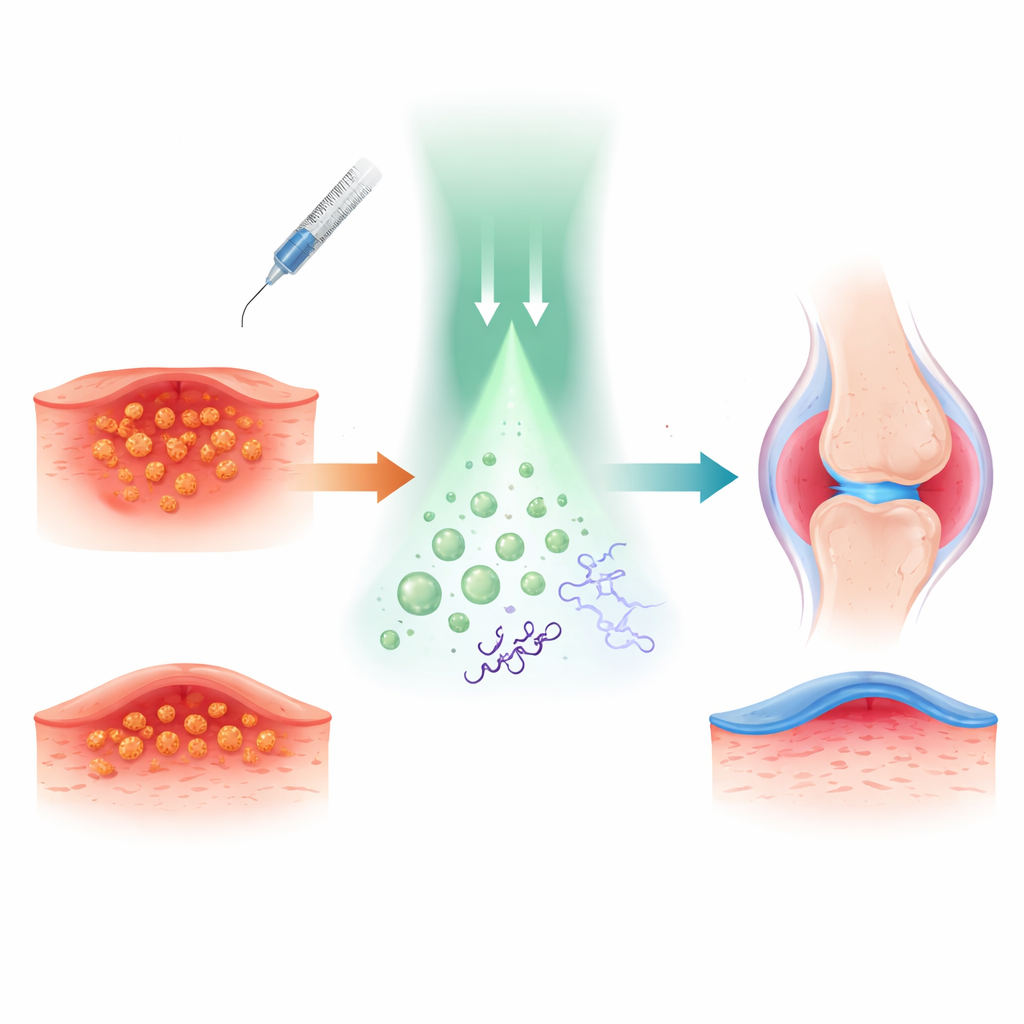
Accendere il farmaco con una luce delicata
Per capire come funziona questo interruttore luminoso, il team ha studiato la chimica in soluzione. Hanno dimostrato che un fotocatalizzatore a base di iridio può trasferire un elettrone a TTC-NO quando illuminato con luce verde. Questo indebolisce un legame specifico, facendo liberare l’ossido nitrico e ripristinando la tetracaina nella sua forma attiva. Misure con spettroscopia e cromatografia hanno confermato che TTC-NO è quasi completamente convertito in tetracaina e ossido nitrico in queste condizioni, mentre rimane essenzialmente invariato al buio. Quando i due componenti sono stati incapsulati nelle micelle, le particelle sono rimaste stabili, di circa 80 nanometri di diametro, e hanno rilasciato il loro contenuto solo quando irradiate, dimostrando che il concetto di “farmaco incapsulato in farmaco” può essere controllato dall’esterno del corpo con la luce.
Favorire una guarigione più rapida delle ferite infette
Il team è poi passato a modelli murini con ferite cutanee deliberatamente infettate da Staphylococcus aureus resistente alla meticillina (MRSA), un patogeno problematico in ambito ospedaliero. Alcune ferite hanno ricevuto trattamenti standard come un antibiotico o un fattore di crescita, mentre altre sono state trattate con micelle di TTC-NO, con o senza luce. Quando la luce è stata accesa, il sistema TTC-NO ha ridotto nettamente i conteggi batterici, calmato l’infiammazione, favorito la neoangiogenesi e aumentato la deposizione di collagene, tutti elementi essenziali per una corretta riparazione. Le ferite trattate in questo modo si sono chiuse più velocemente e in modo più completo rispetto a quelle trattate con sola tetracaina o con micelle mantenute al buio, e le loro prestazioni sono risultate comparabili a un antibiotico di prima linea. È importante che i controlli di sicurezza non abbiano mostrato danni importanti agli organi o alla chimica del sangue.
Alleviare il dolore e silenziare i segnali nervosi
Poiché l’infezione e il danno tissutale attivano fortemente le vie del dolore, gli scienziati hanno misurato con cura i comportamenti correlati al dolore nello stesso modello di ferita. La tetracaina tradizionale aumentava brevemente la forza necessaria per innescare una risposta dolorosa ma perdeva efficacia entro poche ore. Al contrario, le micelle TTC-NO attivate dalla luce fornivano sollievo fino a 12 ore. Studi microscopici di gruppi nervosi vicino al midollo spinale e registrazioni di attività nella corteccia sensoriale cerebrale hanno rivelato che il trattamento combinato attenuava il fuoco dei neuroni sensoriali del dolore molto tempo dopo che la sola tetracaina aveva perso effetto. Esperimenti aggiuntivi suggeriscono che la maggiore durata del sollievo deriva dalla riduzione del carico batterico e dell’infiammazione grazie all’ossido nitrico, e non solo dall’intorpidimento dei nervi.
Proteggere articolazioni dolorose e infette
I ricercatori hanno testato il sistema anche in topi con artrite settica, una grave infezione da MRSA all’interno dell’articolazione del ginocchio che causa gonfiore, perdita ossea e dolore intenso. Le micelle TTC-NO attivate dalla luce hanno ridotto la larghezza dell’articolazione, diminuito i numeri batterici e protetto la struttura ossea come mostrato da scansioni ad alta risoluzione. I livelli di molecole infiammatorie nocive nel sangue sono diminuiti, mentre sono aumentati i segnali protettivi. A livello comportamentale, i topi trattati hanno tollerato una pressione meccanica maggiore sulla zampa interessata e si sono mossi più liberamente in un’arena aperta, mostrando ancora una volta un sollievo di durata superiore rispetto alla sola tetracaina. Misurazioni nervose e cerebrali rispecchiavano questi miglioramenti comportamentali, indicando un’ampia attenuazione delle vie del dolore senza tossicità locale o sistemica evidente. 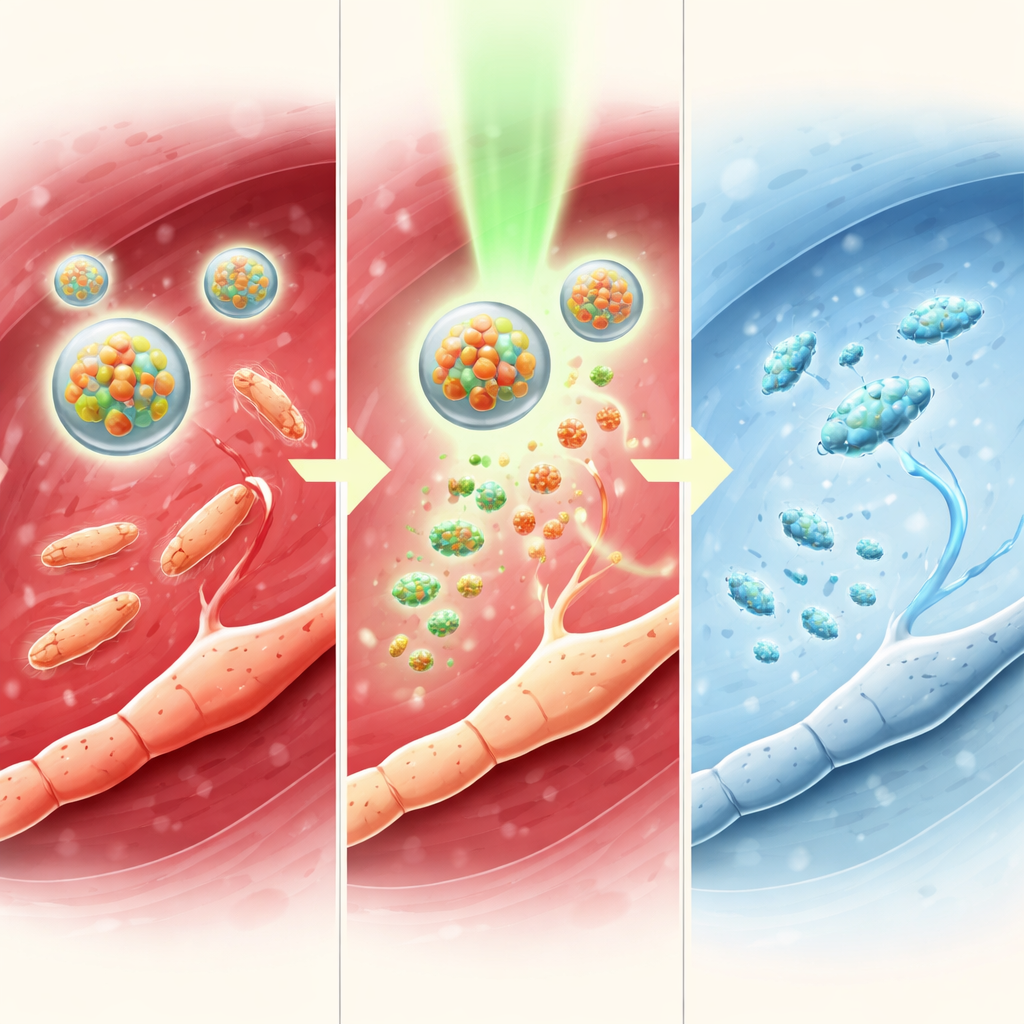
Cosa potrebbe significare per i pazienti
Nel complesso, il lavoro dimostra un singolo nanosistema attivabile con la luce che può sia eliminare infezioni batteriche ostinate sia ridurre in modo significativo il dolore associato. Cagando chimicamente un anestetico all’interno di una struttura rilasciatrice di ossido nitrico e confezionandolo in micelle, gli autori ottengono il rilascio localizzato e su richiesta di due agenti utili usando luce visibile tenue. Nei modelli animali di ferite cutanee e infezioni articolari, questo design accelera la guarigione e prolunga il sollievo dal dolore oltre quanto può offrire un anestetico locale convenzionale. Pur essendo necessari molti altri test prima dell’uso umano, lo studio sottolinea come farmaci intelligenti e commutabili potrebbero un giorno rendere i trattamenti delle infezioni più efficaci e più confortevoli.
Citazione: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Parole chiave: terapia con ossido nitrico, farmaci attivati dalla luce, analgesia antibatterica, nanomedicina, infezioni da MRSA