Clear Sky Science · it
Cation radicalico e dication isolabili del dialumene
Perché questa storia sull'alluminio è importante
I chimici sono sempre alla ricerca di metalli più economici e più abbondanti in grado di svolgere i lavori sofisticati oggi affidati a elementi preziosi come il palladio o il platino. Questo studio mostra che l'alluminio — un metallo più noto per lattine e aeromobili — può essere indotto in forme sorprendentemente reattive che si comportano un po' come minuscoli interruttori elettronici. Capire e controllare queste specie di alluminio esotiche potrebbe, in futuro, aiutare a costruire nuovi catalizzatori per processi chimici e materiali più puliti.
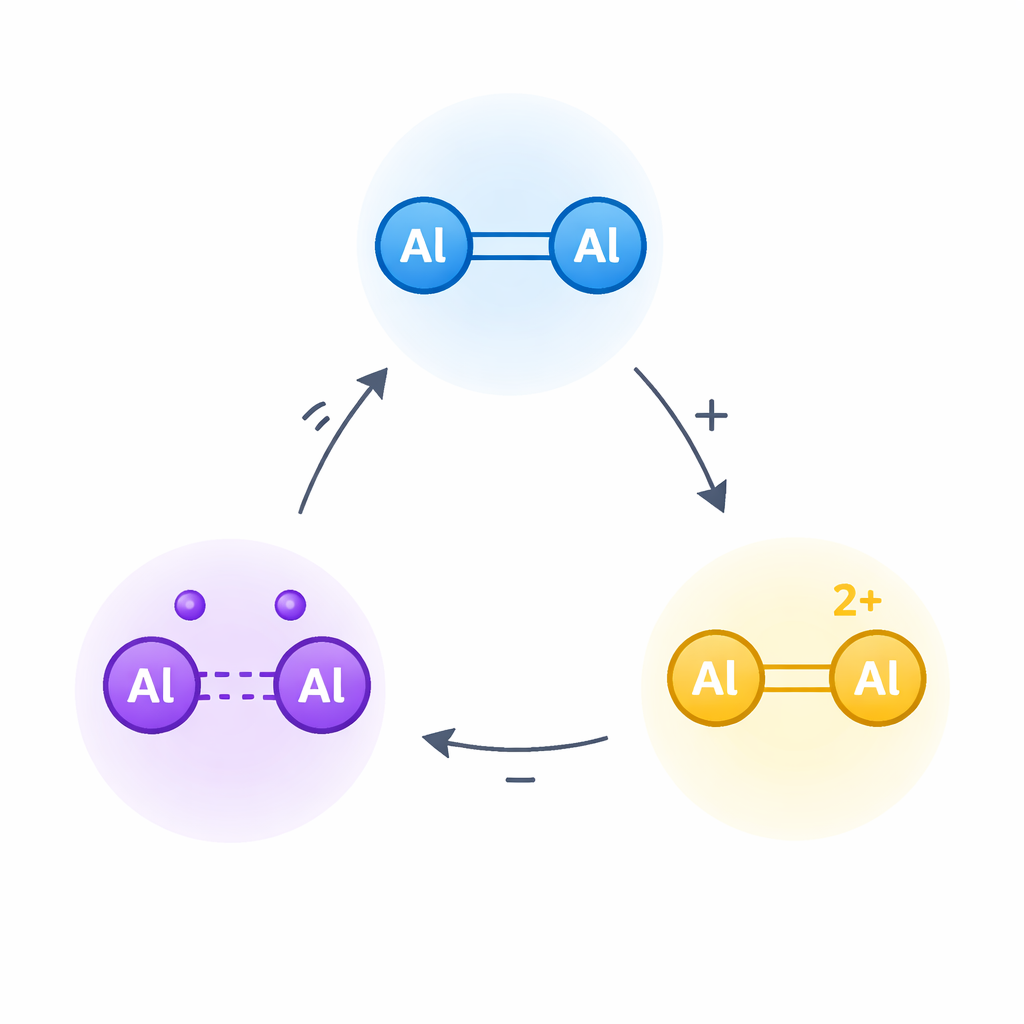
Trasformare un legame familiare in un interruttore elettronico
Il lavoro si concentra sul dialumene, una molecola in cui due atomi di alluminio condividono un doppio legame, in qualche modo simile al doppio legame carbonio–carbonio negli alcheni comuni. Nelle molecole organiche tali doppi legami possono essere ossidati gradualmente per dare prima cationi radicalici e poi dicationi — forme altamente cariche e reattive che stanno alla base di molte reazioni in elettrochimica e scienza dei materiali. Gli autori si sono chiesti se il legame alluminio–alluminio nel dialumene potesse essere spinto attraverso una simile ossidazione in due passi, anche se l'alluminio è fortemente elettronegativo verso la perdita di elettroni e tali specie cariche dovrebbero essere eccezionalmente instabili.
Progettare un'infrastruttura molecolare protettiva
Per domare questa reattività, il gruppo ha costruito un dialumene circondato da ingombranti gruppi a base di silicio e da forti leganti donatori di elettroni di tipo “carbene”. Questi fungono come un’armatura imbottita e cuscinetti elettronici: schermano il delicato nucleo alluminio–alluminio da reazioni indesiderate e aiutano a fornire densità elettronica dove è necessaria. Partendo da questo dialumene neutro, etichettato come 1, hanno usato agenti ossidanti scelti con cura per rimuovere prima un elettrone e poi un secondo, generando un catione radicalico centrato sull’alluminio (2) e poi un dicatione (3). La cristallografia a raggi X ha fornito istantanee dei tre stati, rivelando come il legame alluminio–alluminio si allunghi progressivamente e cambi carattere man mano che gli elettroni vengono rimossi.
Dimostrare un vero ciclo redox a tre stati
Misure chiave hanno confermato che il catione radicalico porta effettivamente un elettrone spaiato centrato tra i due atomi di alluminio, non sui leganti circostanti. La spettroscopia di risonanza paramagnetica elettronica ha mostrato un segnale chiaro compatibile con un singolo elettrone condiviso dai due centri di alluminio. Studi computazionali hanno supportato questo quadro, indicando che l'elettrone residuo di legame occupa un orbitale principalmente alluminio–alluminio. Quando viene rimosso il secondo elettrone per formare il dicatione, il legame si indebolisce verso una singola coordinazione e la carica positiva si accumula sulla coppia di alluminio. Importante, i ricercatori hanno dimostrato che tutti questi cambiamenti sono reversibili: reinserendo elettroni con un agente riducente si rigenerano prima il catione radicalico e poi il dialumene originale, e mescolando le forme neutre e doppiamente cariche si ottiene il catione radicalico tramite un processo di comproporzionamento. Insieme, queste reazioni dimostrano un ciclo redox a tre stati robusto e isolabile su una semplice unità alluminio–alluminio.
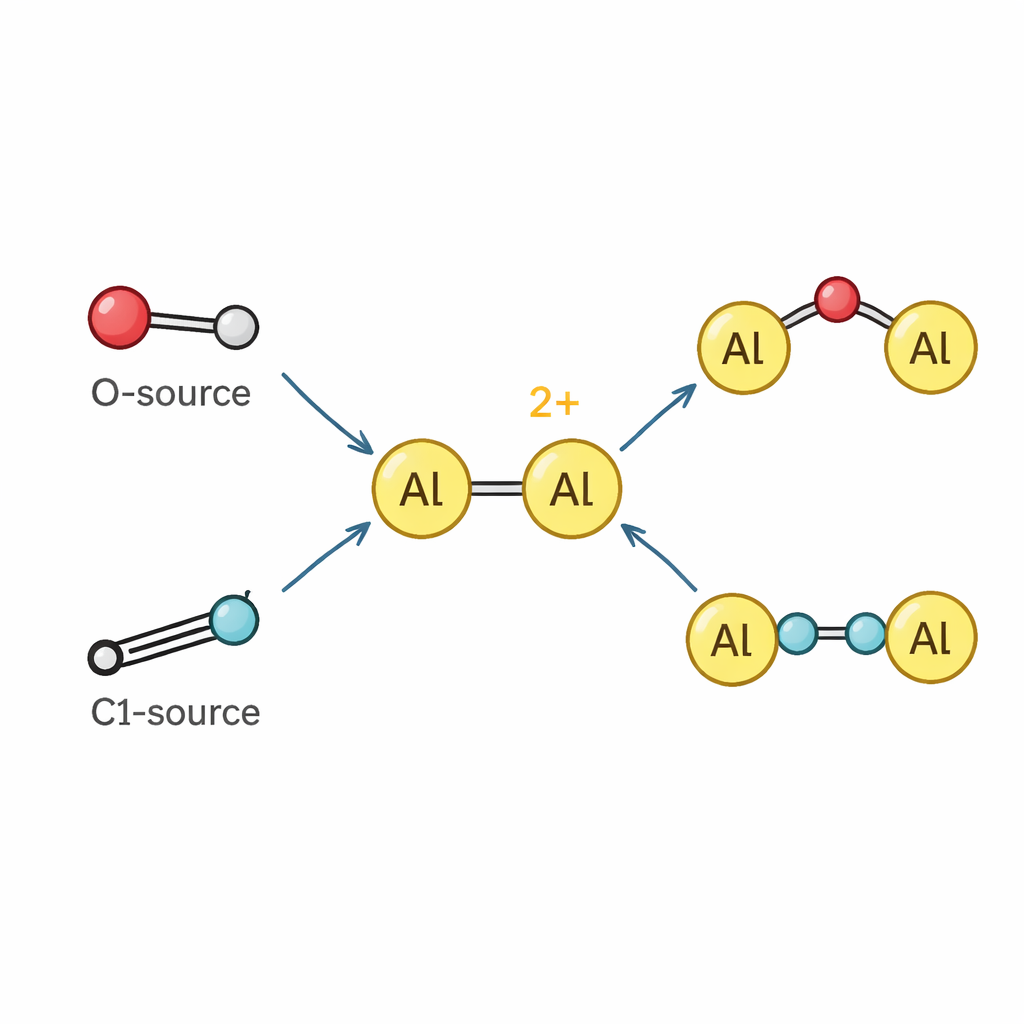
Far comportare l'alluminio come un metallo di transizione
Con il dicatione a disposizione, il gruppo ha esplorato come reagisce con altre molecole. Poiché i suoi atomi di alluminio sono fortemente poveri di elettroni, il dicatione si comporta come un potente acido di Lewis, legando facilmente partner basici come la piridina e molecole affini per dare nuovi complessi dialuminio. Oltre al semplice legame, il dicatione può spezzare e inserirsi in legami chimici. Estrae atomi di ossigeno dal protossido d'azoto e dall'N-ossido di piridina, formando specie stabili in cui un atomo di ossigeno fa da ponte tra i due centri di alluminio oppure è incorporato in una corta catena alluminio–ossigeno–silicio che ricorda un piccolo frammento di struttura tipo zeolite. Interagisce anche con isocianuri — piccole unità carbonio–azoto usate come mattoni monocarboniosi — per cucirle insieme in frammenti più lunghi N–C–C–N che si estendono tra i due atomi di alluminio, dimostrando un raro esempio di “omologazione” di isocianuri guidata da un catione del gruppo principale.
Cosa significa per il futuro
In termini pratici, i ricercatori hanno trasformato un legame alluminio–alluminio in un interruttore elettronico controllabile a tre posizioni che può essere commutato tra stati neutro, singolarmente caricato e doppiamente caricato, ciascuno con forme e reattività distinte. La versione doppiamente carica è particolarmente versatile, attraendo elettroni e piccoli frammenti da altre molecole in modi solitamente associati a metalli di transizione più costosi. Mostrando che tale comportamento è possibile con l'alluminio e che gli stati diversi possono essere interconvertiti in modo affidabile, questo lavoro apre la strada alla progettazione di nuovi catalizzatori sostenibili e materiali funzionali costruiti con uno dei metalli più abbondanti sulla Terra.
Citazione: Liu, X., Kostenko, A., Körber, E. et al. Isolable radical cation and dication of dialumene. Nat Commun 17, 1937 (2026). https://doi.org/10.1038/s41467-026-69607-6
Parole chiave: catalisi dell'alluminio, molecole a commutazione redox, chimica dei principali gruppi, cationi radicalici, attivazione di piccole molecole