Clear Sky Science · it
L’asse Treg-γδ determina la dimorfismo sessuale nell’epatocarcinogenesi
Perché alcuni tumori al fegato colpiscono più duramente gli uomini
I medici sanno da tempo che il cancro del fegato colpisce gli uomini circa il doppio delle donne, ma le ragioni vanno oltre le semplici differenze ormonali. Questo studio esplora le cellule immunitarie presenti all’interno dei tumori epatici e rivela una conversazione nascosta tra due tipi di cellule T che aiuta a spiegare perché il fegato maschile è più vulnerabile — e come questa conoscenza potrebbe indicare nuove terapie più mirate.
La tensione immunitaria all’interno dei tumori epatici
Il cancro del fegato, in particolare il carcinoma epatocellulare, cresce in un contesto complesso di cellule immunitarie, vasi sanguigni e tessuto cicatriziale. Gli autori hanno confrontato i tumori di uomini e donne, sia nei pazienti sia in modelli murini, e hanno trovato un forte squilibrio: i tumori maschili erano ricchi di cellule T regolatorie, o Treg, un tipo cellulare che normalmente attenua risposte immunitarie eccessive. Allo stesso tempo, il numero totale delle altre cellule T comuni non differiva molto tra i sessi. Poiché livelli elevati di Treg erano associati a una sopravvivenza peggiore, il team ha ipotizzato che queste cellule non fossero solo spettatrici, ma complici attive che aiutano i tumori a sfuggire all’attacco immunitario. 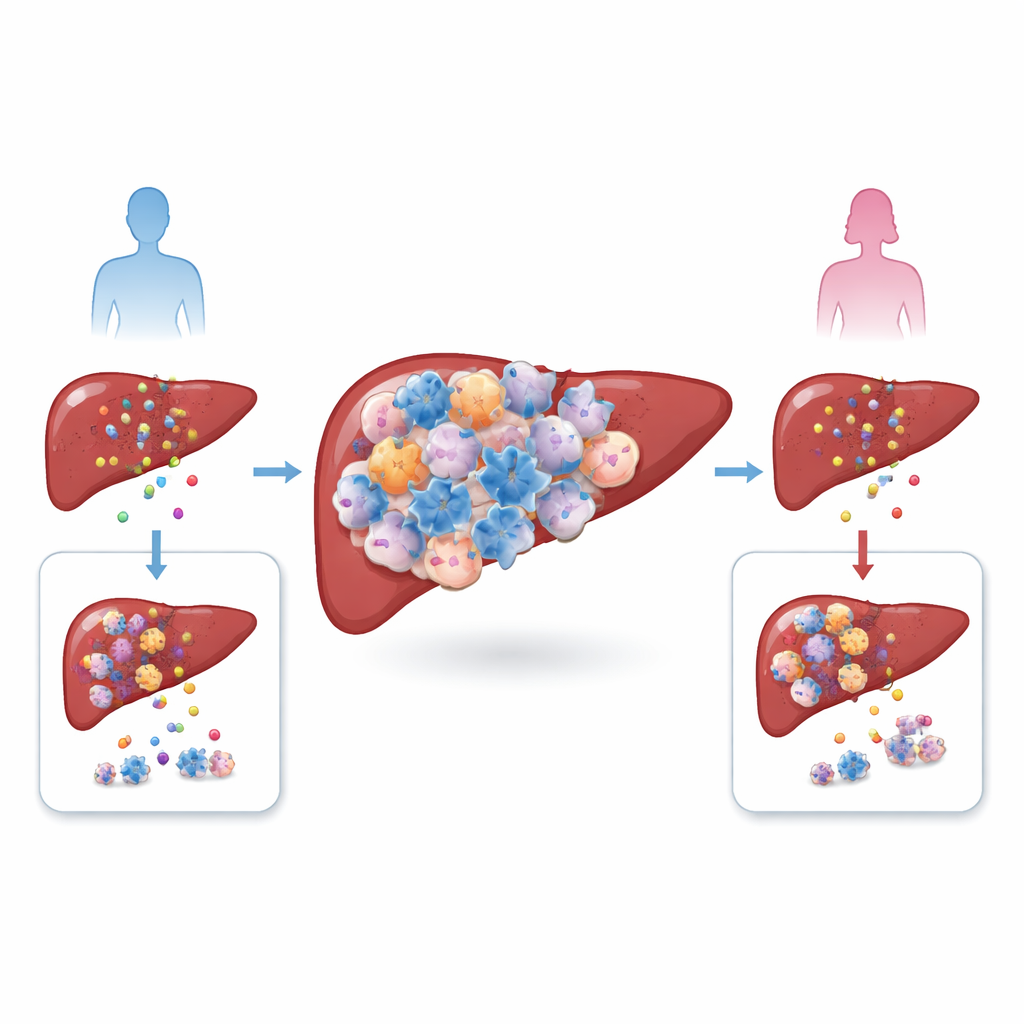
Come gli ormoni maschili richiamano cellule soppressive
Per capire perché i tumori maschili attirano più Treg, i ricercatori si sono concentrati sui segnali chimici prodotti dalle cellule tumorali. Hanno scoperto che i tumori epatici maschili producevano quantità maggiori di una molecola chiamata Ccl2, mentre le Treg esprimevano più del suo recettore corrispondente, Ccr2. Questo abbinamento funziona come un segnale di richiamo, attirando le Treg nel tumore. Quando il segnale Ccl2 o il recettore Ccr2 venivano rimossi nei topi, i tumori si riducevano e molte meno Treg entravano nel fegato, soprattutto nei maschi. Il team ha quindi mostrato che il testosterone, il principale ormone sessuale maschile, guida questo processo: attiva una catena di proteine nelle cellule del cancro epatico che accende il gene Ccl2, intensificando il richiamo chimico che convoca le Treg. I topi maschi castrati, che producono meno testosterone, avevano livelli più bassi di Ccl2 nei tumori e meno Treg infiltranti.
Cellule guardiane che potrebbero combattere il cancro — ma sono frenate
Un altro tipo di cellule T, note come cellule T gamma-delta, può agire come “guardie” a risposta rapida che riconoscono e uccidono le cellule tumorali senza il normale meccanismo di presentazione dell’antigene. Nel fegato sano queste cellule sono relativamente scarse, ma nel cancro del fegato possono essere potenti combattenti tumorali. Lo studio ha rilevato che i tumori femminili contenevano più di queste cellule gamma-delta e che erano più attive e meglio armate con molecole tossiche. Rimuovere gli ormoni sessuali maschili nei topi aumentava il numero e la vitalità delle cellule gamma-delta nei tumori, lasciando per lo più invariati i classici linfociti CD8 killer. In colture cellulari, le gamma-delta danneggiavano facilmente le cellule del cancro epatico, ma questo effetto veniva indebolito quando venivano aggiunte le Treg, suggerendo che le Treg limitano specificamente questa promettente popolazione antitumorale.
Ipoxia, pacchetti segreti e difensori silenziati
Approfondendo, i ricercatori hanno chiesto come le Treg riescano a spegnere le cellule gamma-delta. All’interno dei tumori l’ossigeno è spesso scarso, uno stato chiamato ipossia. In queste condizioni di basso ossigeno, le Treg nei tumori maschili cominciavano a produrre grandi quantità di una proteina chiamata S100a4. Invece di agire direttamente come molecola libera, S100a4 veniva confezionata in piccole particelle rivestite di membrana note come vescicole extracellulari. Queste vescicole si staccavano dalle Treg e venivano assorbite dalle vicine cellule gamma-delta. Una volta all’interno, S100a4 rimodellava i sistemi di controllo genetico: riduceva l’accessibilità di regioni del DNA che regolano molecole chiave di segnalazione e di uccisione e ne abbassava l’attività. Le cellule gamma-delta diventavano meno capaci di rispondere tramite i loro recettori T e meno in grado di rilasciare proteine tossiche e citochine, smussando di fatto la loro lama antitumorale. 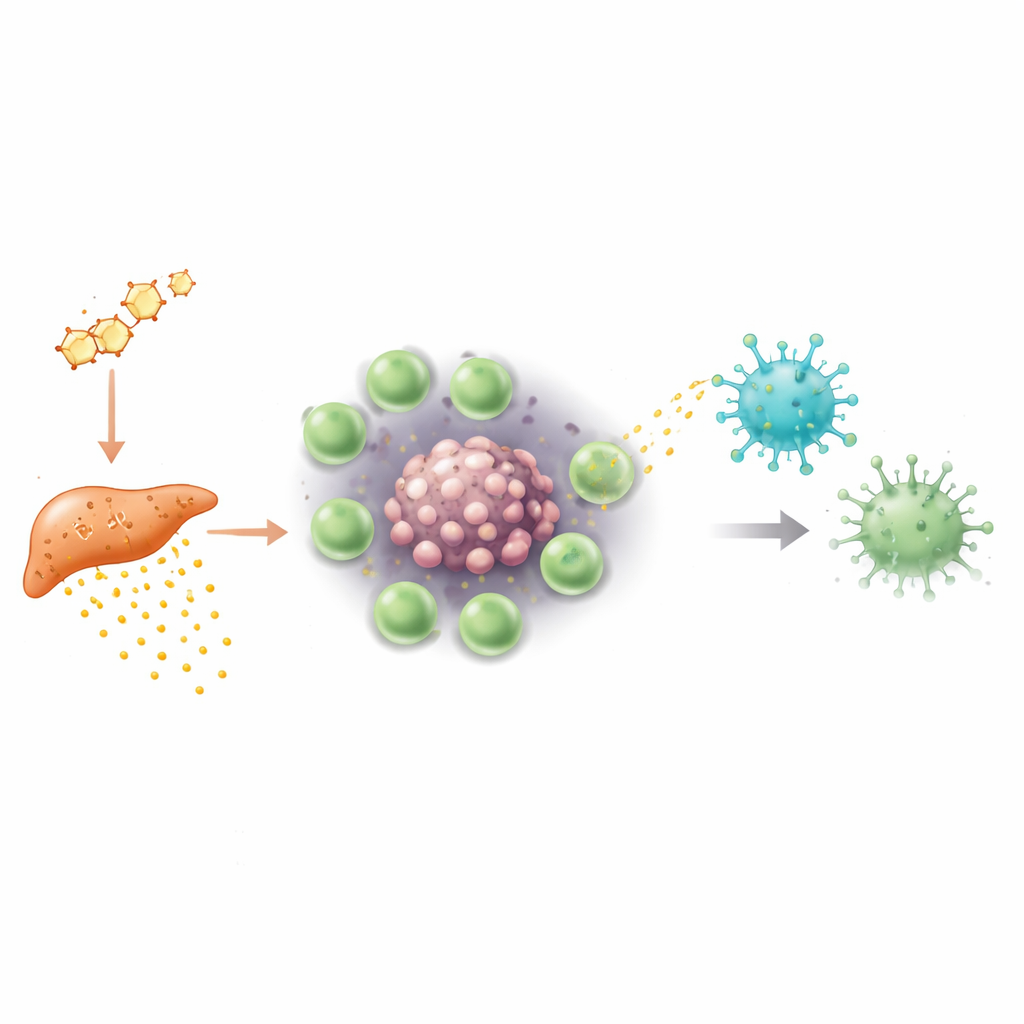
Spezzare il circuito dannoso
Infine, il team ha testato cosa succede se questo asse Treg–S100a4–gamma-delta viene interrotto. In topi ingegnerizzati in modo che le Treg non potessero produrre S100a4, i tumori epatici maschili si riducevano, il livello complessivo di S100a4 nei tumori calava e le cellule gamma-delta diventavano più numerose e più attive. È importante notare che il numero di Treg nel tumore non diminuiva — veniva solo meno il loro effetto soppressivo sulle cellule gamma-delta. Questo cambiamento ha quasi annullato il consueto divario nella gravità del tumore tra topi maschi e femmine, sottolineando quanto sia centrale questo percorso nelle differenze legate al sesso nel cancro del fegato.
Cosa significa per le terapie future
In termini accessibili, lo studio mostra che gli ormoni maschili spingono le cellule del cancro epatico a inviare segnali di “benvenuto” più forti per le Treg immunosoppressive. Una volta nel tumore — e sotto lo stress del basso ossigeno — queste Treg spediscono vescicole piene di S100a4 che silenziano silenziosamente le vicine cellule gamma-delta, che altrimenti potrebbero tenere sotto controllo il cancro. Mirando al segnale Ccl2 che attira le Treg, oppure ai messaggi S100a4 che zittiscono le gamma-delta, le terapie future potrebbero ripristinare le difese naturali dell’organismo, specialmente negli uomini. Questo lavoro suggerisce che il trattamento del cancro del fegato potrebbe trarre vantaggio dall’essere consapevole del sesso e dal valorizzare, anziché ignorare, i punti di forza unici delle cellule T gamma-delta.
Citazione: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Parole chiave: carcinoma epatocellulare, cellule T regolatorie, cellule T gamma-delta, differenze sessuali, immunologia tumorale