Clear Sky Science · it
La segnalazione del calcio pirimidinergica collega il metabolismo tubulare alla fibrosi nella malattia renale
Perché la cicatrizzazione renale conta
La malattia renale cronica colpisce silenziosamente centinaia di milioni di persone nel mondo e spesso sfocia in reni cicatrizzati e irrigiditi. Una volta instaurata questa cicatrizzazione, detta fibrosi, è difficile recuperare la funzione renale perduta. Eppure i medici dispongono ancora di pochi farmaci in grado di fermare specificamente la fibrosi. Questo studio pone una domanda semplice ma cruciale: come fa un danno a breve termine ai tubuli del rene a trasformarsi gradualmente in tessuto cicatriziale duraturo, e interrompere quella catena di eventi potrebbe rallentare o prevenire l’insufficienza renale?
Tubuli renali indaffarati e la loro chimica nascosta
I tubuli prossimali del rene sono microscopici operai che recuperano la maggior parte di acqua e nutrienti filtrati dal sangue. Per svolgere questo lavoro la loro attività chimica è particolarmente intensa. Analizzando dati di espressione genica a singola cellula provenienti da reni di topo, i ricercatori hanno trovato che queste cellule tubulari sono particolarmente ricche di geni coinvolti nella gestione delle pirimidine, una famiglia di piccole molecole che normalmente servono a costruire e riparare DNA e RNA. Nei tubuli danneggiati, un enzima di una via di “salvataggio”, la citidina deaminasi, risultava fortemente upregolato, suggerendo che le cellule lese riorganizzano l’uso delle pirimidine per mantenere elevati alcuni blocchi di costruzione ricchi di energia, compreso un composto chiamato UDP.
Segnali che fuoriescono dalle cellule danneggiate
Quando il team ha lesionato in coltura cellule umane simili ai tubuli con tossine che imitano la chemioterapia o un sovradosaggio di acido folico, le cellule hanno rilasciato UDP nel fluido circostante. In reni di topo esposti a una lesione, la colorazione di fette di tessuto ha mostrato sia alti livelli dell’enzima che gestisce le pirimidine nei tubuli sia segni che le cellule di supporto vicine, chiamate fibroblasti, si stavano attivando e cambiando forma. I fibroblasti normalmente rimangono silenti tra i tubuli, ma quando si attivano si moltiplicano e contribuiscono a depositare collagene e altre fibre che ispessiscono e irrigidiscono il tessuto renale. Queste osservazioni suggerivano un’idea semplice: i tubuli danneggiati potrebbero «versare» segnali chimici di distress che i fibroblasti vicini possono percepire.
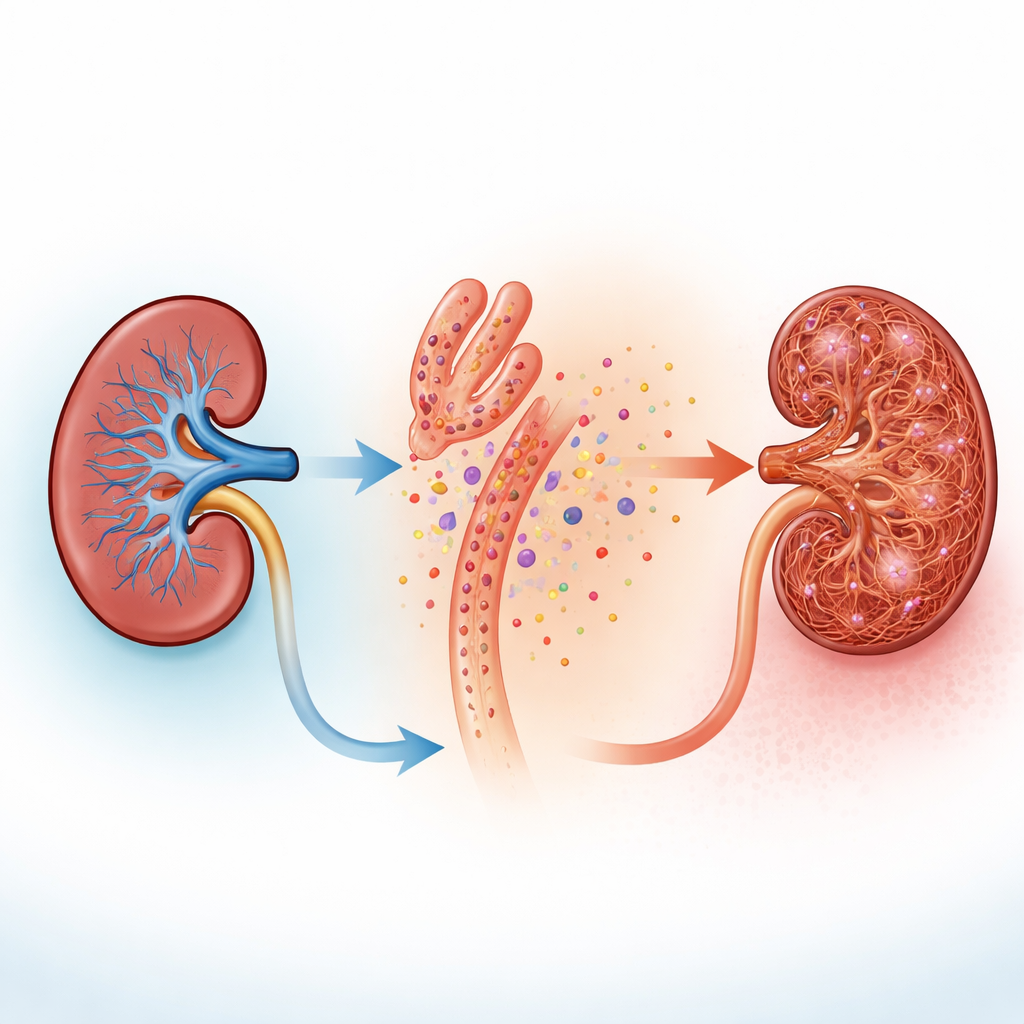
Come i fibroblasti ascoltano con lampi di calcio
Le presunte «orecchie» sui fibroblasti sono i recettori P2Y6, proteine di superficie che rispondono all’UDP. Analizzando diversi dataset a singola cellula, gli autori hanno osservato che P2Y6 era presente sulle cellule stromali e aumentava ulteriormente nei modelli murini di malattia renale cronica. Misurazioni su reni interi hanno confermato forti incrementi dei livelli di P2Y6 in due diversi modelli di cicatrizzazione. In fette renali fresche e in fibroblasti renali coltivati e ingegnerizzati per illuminarsi quando aumenta il calcio intracellulare, l’aggiunta di UDP o di un farmaco che attiva P2Y6 ha prodotto rapide ondate di calcio. Questi lampi iniziavano nei processi lunghi e sottili che avvolgono i tubuli e poi si propagavano nel corpo cellulare, e scomparivano quando P2Y6 veniva bloccato o il calcio veniva chimicamente sequestrato. In topi vivi, la microscopia intravitale ad alta risoluzione ha mostrato che i fibroblasti intorno ai tubuli mostrano un’attività di calcio frequente e irregolare che aumenta drasticamente quando i tubuli sono danneggiati, anche mentre le cellule tubulari stesse perdono attività.
Dai segnali brevi alle cicatrici durature
Le esplosioni di calcio all’interno di una cellula non sono solo fuochi d’artificio; possono riprogrammare il comportamento cellulare. Quando fibroblasti in coltura sono stati esposti a un composto che attiva P2Y6, si sono moltiplicati più rapidamente, si sono mossi con maggiore facilità e hanno attivato geni associati a uno stato più aggressivo di «miofibroblasto». Questi geni codificano proteine come fibronectina, vimentina e collagene che contribuiscono direttamente alla formazione della cicatrice. Bloccare P2Y6 o impedire gli aumenti di calcio annullava questi cambiamenti, e la riduzione dell’espressione del gene del recettore attenuava la risposta. Nei topi, due forme distinte di lesione renale — l’ostruzione dell’uretere e la nefropatia da acido folico — hanno mostrato lo stesso schema: reni lesi presentavano più fibroblasti proliferanti, più marcatori di miofibroblasti, più collagene e aree di fibrosi più estese.
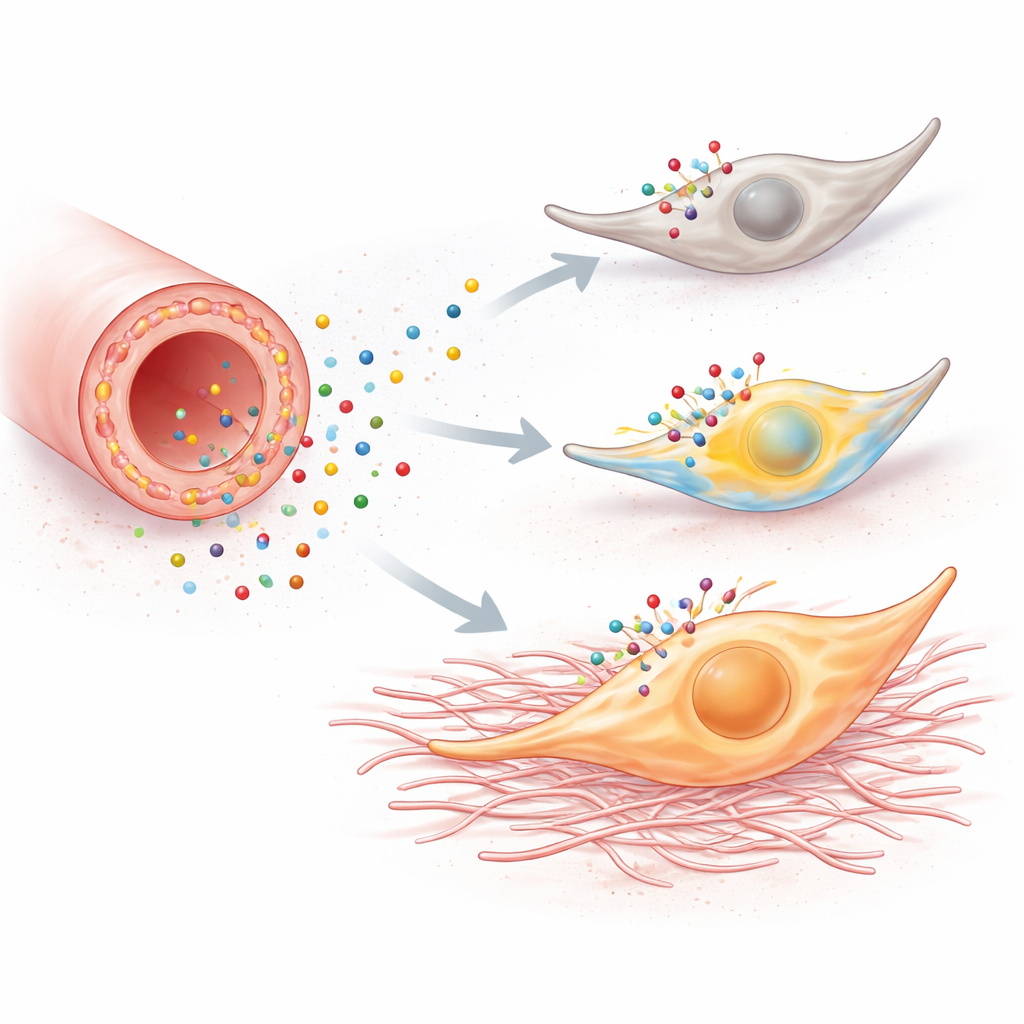
Abbassare il volume della segnalazione dannosa
Per verificare se questa via non fosse soltanto presente ma anche realmente dannosa, i ricercatori hanno rimosso P2Y6 geneticamente o lo hanno bloccato con un farmaco. I topi privi del recettore hanno sviluppato meno fibrosi renale dopo ostruzione dell’uretere o lesione da acido folico: i loro fibroblasti si sono moltiplicati meno, hanno depositato meno matrice fibrosa e hanno reclutato meno cellule infiammatorie. Gli esami del sangue hanno mostrato che questi animali knockout mantenevano anche una migliore funzione di filtrazione renale. Trattare topi normali con un composto inibitore di P2Y6 ha prodotto una protezione comparabile, inclusa una riduzione dell’attività di calcio nei fibroblasti e una minore cicatrizzazione, sebbene i miglioramenti nei marcatori ematici siano risultati più variabili.
Cosa significa per i trattamenti futuri
Nel complesso, il lavoro rivela una catena di eventi semplice ma potente. Quando le cellule dei tubuli renali sono danneggiate, cambiano la loro chimica interna e rilasciano UDP nel tessuto circostante. I fibroblasti vicini rilevano questa molecola attraverso i loro recettori P2Y6, rispondono con ondate di calcio intracellulare e poi passano a uno stato pro-fibrotico — moltiplicandosi, migrando e depositando collagene. Interrompere questa segnalazione pirimidinergica basata sul calcio, in particolare al livello di P2Y6, riduce notevolmente la fibrosi in diversi modelli murini. Per i pazienti, questo suggerisce un nuovo tipo di bersaglio farmacologico: composti che bloccano selettivamente P2Y6 nel rene potrebbero aiutare a spezzare il collegamento tra i danni renali quotidiani e la lenta, irreversibile fibrosi che conduce alla malattia renale cronica.
Citazione: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
Parole chiave: malattia renale cronica, fibrosi renale, segnalazione dei fibroblasti, metabolismo delle pirimidine, recettore P2Y6