Clear Sky Science · it
Doppio reclutamento di due molecole CCM2 su KRIT1 sopprime l’espressione di KLF4
Perché i vasi sanguigni cerebrali richiedono un controllo accurato
I vasi sanguigni nel cervello devono camminare su una lama: devono essere sufficientemente robusti da evitare perdite ma anche abbastanza flessibili da rispondere alle esigenze dell’organismo. Quando questo equilibrio si rompe, si possono sviluppare malformazioni cavernose cerebrali—aggregati di vasi fragili a forma di bolla che possono sanguinare e causare crisi epilettiche o ictus. Questo studio scopre una stretta interazione molecolare inedita fra tre proteine che aiuta a mantenere la stabilità dei vasi cerebrali e mostra come la rottura di tale interazione possa promuovere la malattia.
I guardiani della salute vascolare
Le cellule che rivestono i vasi si affidano a un gruppo di interruttori principali, chiamati KLF2 e KLF4, per controllare i geni che mantengono la forza e l’identità dei vasi. Se questi interruttori vengono eccessivamente attivati, i vasi diventano anomali e più suscettibili a danni. Altre due proteine, KRIT1 e CCM2, sono note per proteggere questo sistema. Chi eredita versioni difettose di una delle due proteine ha un alto rischio di malformazioni cavernose cerebrali. Tuttavia, finora gli scienziati non avevano compreso esattamente come KRIT1 e CCM2 collaborassero per tenere KLF4 sotto controllo.
Un sorprendente trio
I ricercatori hanno utilizzato cellule umane di tipo endoteliale coltivate in laboratorio e hanno ridotto selettivamente la quantità di CCM2 o KRIT1 con strumenti genetici. Quando una delle due proteine veniva depletata, i livelli di KLF4 aumentavano notevolmente, riecheggiando quanto osservato in modelli animali e pazienti. Ripristinare livelli normali di CCM2 o KRIT1 abbassava KLF4—ma solo se le proteine ripristinate potevano ancora legarsi fra loro. Modificando con precisione le regioni in cui CCM2 e KRIT1 interagiscono, il gruppo ha dimostrato che questo contatto fisico è essenziale per impedire l’aumento di KLF4. Questi esperimenti collocano saldamente la partnership KRIT1–CCM2 al centro del sistema di controllo di questo potente fattore di trascrizione.
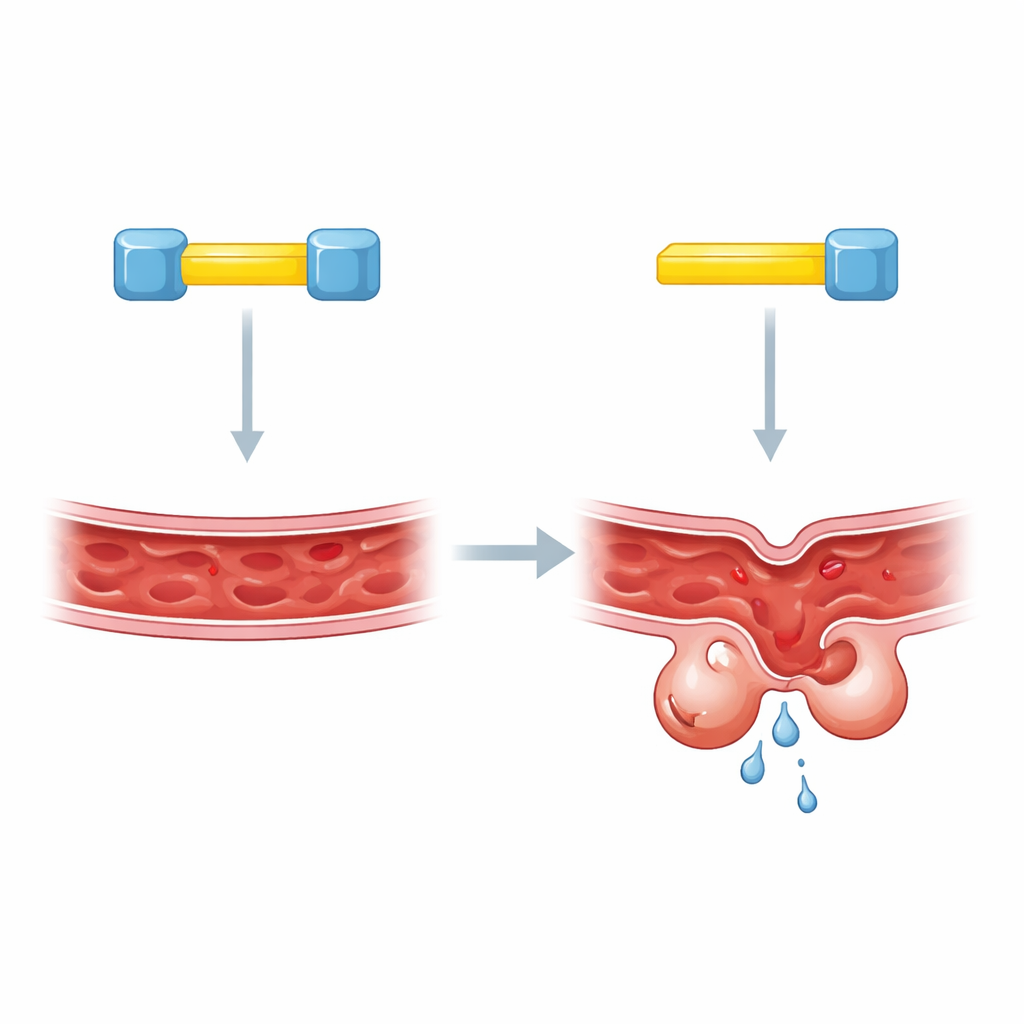
Due serrature su una chiave
Per approfondire, gli autori si sono concentrati su brevi segmenti all’interno di KRIT1 che fungono da siti di ancoraggio molecolare. Studi precedenti avevano suggerito che CCM2 si aggancia a KRIT1 in uno di questi siti, ma metodi diversi avevano fornito risposte contrastanti su quale fosse. Il nuovo studio rivela che la confusione derivava dal fatto che il quadro reale è più complesso: KRIT1 porta due segmenti di ancoraggio vicini, e entrambi sono necessari. Quando uno dei segmenti veniva alterato, i livelli di KLF4 restavano anormalmente elevati, proprio come se KRIT1 mancasse del tutto. Test biochimici in cellule ingegnerizzate hanno mostrato che una singola proteina KRIT1 può collegare due molecole distinte di CCM2 contemporaneamente, suggerendo un’inaspettata assemblazione a tre componenti.
Osservare la morsetta molecolare nei dettagli
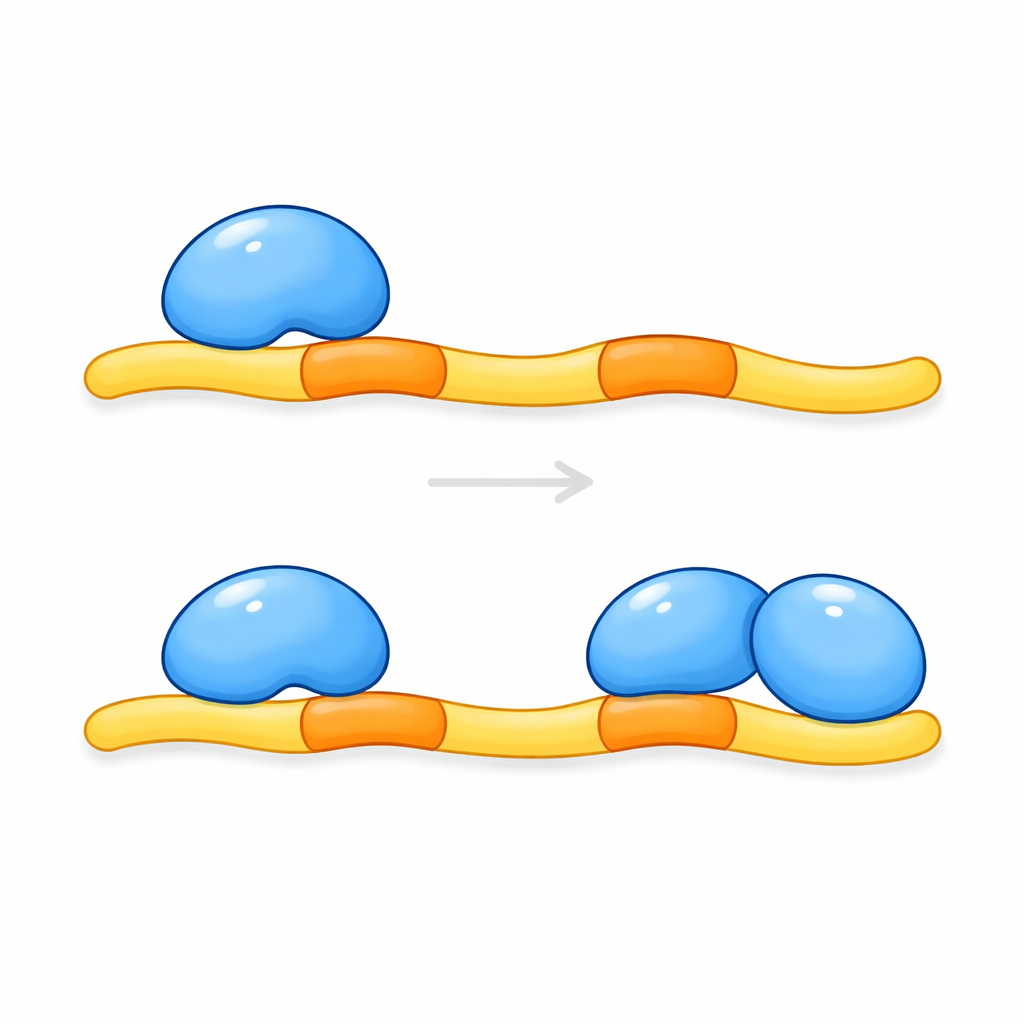
Il gruppo ha quindi purificato i frammenti rilevanti di CCM2 e KRIT1 e ha esaminato come si associano in soluzione e in cristalli. Le misure della massa del complesso indicavano che due copie di una regione chiave di CCM2 si legano a una singola porzione di KRIT1 contenente la coppia di siti di ancoraggio. Istanti strutturali ad alta risoluzione hanno confermato questo arrangiamento 2:1: un peptide esteso di KRIT1 si infila tra due domini di CCM2, con ciascun sito di ancoraggio che si inserisce in una tasca simile su una diversa molecola di CCM2. Un breve segmento elicoidale tra i siti di ancoraggio contribuisce a posizionare i due domini di CCM2 fianco a fianco, creando una struttura avvolgente, simile a una morsetta. Questo tipo di doppio coinvolgimento—due domini di legame che si attaccano a siti tandem su un partner—non era stato osservato prima per questa famiglia di moduli proteici.
Implicazioni per le malattie cerebrali e oltre
Questi risultati mostrano che KRIT1 non si limita a legare una singola molecola di CCM2; agisce piuttosto come uno scaffold che recluta una coppia di proteine CCM2. Solo quando entrambi i siti di ancoraggio su KRIT1 sono occupati il complesso può efficacemente limitare la produzione di KLF4 e, di conseguenza, contribuire a prevenire la crescita di vasi fragili. Le mutazioni in KRIT1 che interferiscono con uno qualsiasi dei due siti di ancoraggio sono perciò destinate ad indebolire questa morsetta protettiva e possono spiegare alcune forme ereditarie di malformazioni cavernose cerebrali. Poiché molte altre proteine umane portano motivi gemelli simili, questo studio suggerisce anche un principio più ampio: l’accoppiamento doppio da parte di coppie di domini correlati potrebbe essere un modo comune con cui le cellule modulano finemente le reti di segnalazione. Comprendere questa interazione a tre partner potrebbe alla fine indirizzare strategie per stabilizzare i vasi sanguigni nelle persone a rischio di emorragie cerebrali.
Citazione: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Parole chiave: malformazioni cavernose cerebrali, cellule endoteliali, KRIT1, CCM2, KLF4