Clear Sky Science · it
Identificazione senza contrasto dello stato della barriera emato‑encefalica nei gliomi tramite AI generativa a diffusione e MRI non contrastata
Perché è importante per i pazienti con tumore cerebrale
I pazienti con tumori cerebrali eseguono routinariamente esami MRI, e molti ricevono anche un mezzo di contrasto iniettato perché i medici possano valutare se la barriera protettiva emato‑encefalica sia compromessa. Queste informazioni guidano interventi chirurgici, radioterapia e prognosi—ma il mezzo di contrasto comporta rischi, aumenta tempi e costi e non è sempre disponibile. Questo studio presenta un sistema di intelligenza artificiale (AI) che interpreta esami MRI di routine senza contrasto e ricostruisce virtualmente le immagini da contrasto mancanti, permettendo ai medici di inferire lo stato della barriera emato‑encefalica senza iniettare alcun agente di contrasto.
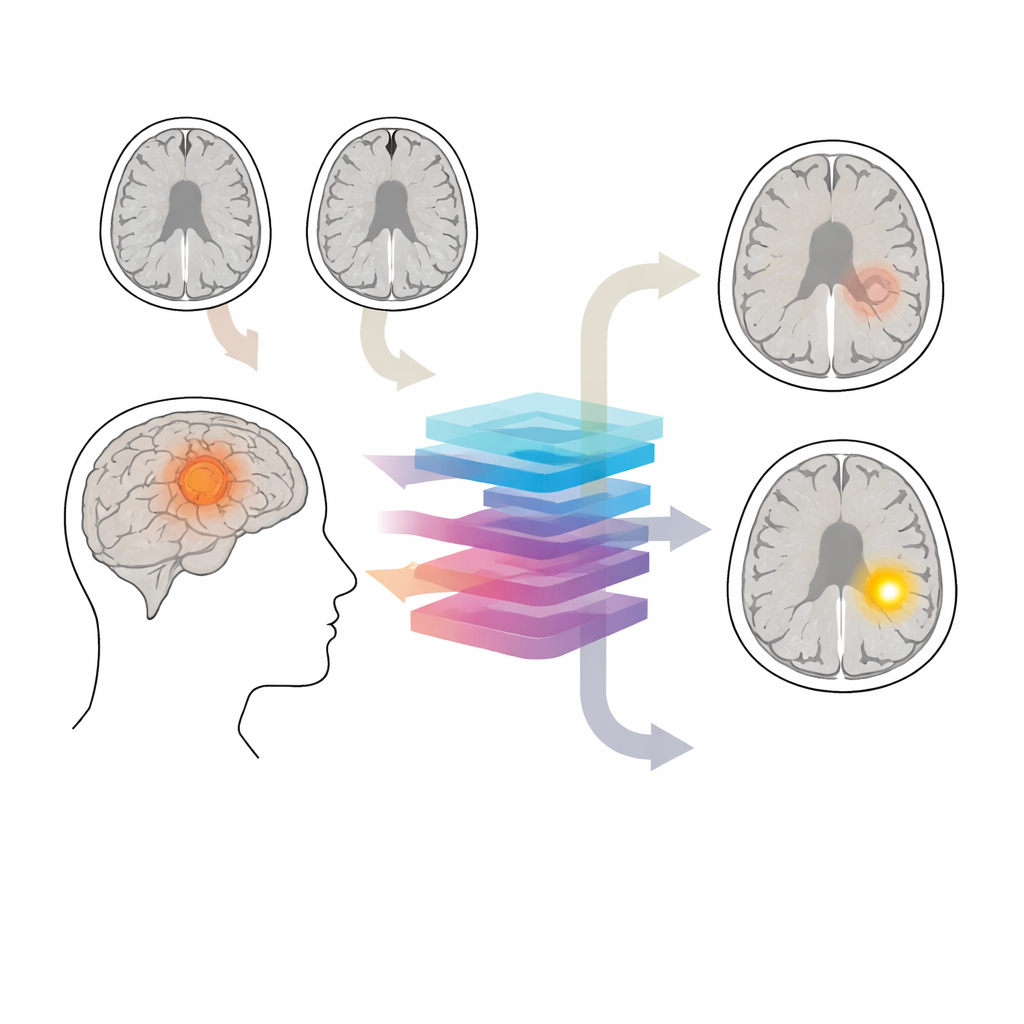
Il guardiano protettivo del cervello
La barriera emato‑encefalica funziona come un filtro microscopico intorno ai vasi sanguigni cerebrali, lasciando passare soltanto piccole molecole. In molti gliomi questa barriera diventa permeabile. Nelle MRI standard con contrasto, le aree che perdono barriera si illuminano dopo l’iniezione, mentre le regioni integre restano scure. Questi pattern influenzano l’intensità del trattamento e aiutano a definire cosa rimuovere chirurgicamente o mirare con la radioterapia. Tuttavia le scansioni con contrasto a volte vengono evitate—forse nelle prime valutazioni o nel follow‑up a lungo termine di tumori a crescita lenta—e alcuni pazienti dovrebbero evitare il contrasto per malattie renali, reazioni allergiche o preoccupazioni circa la deposizione di gadolinio nel cervello.
Convertire scansioni ordinarie in contrasto virtuale
Gli autori si sono chiesti se le scansioni MRI senza contrasto, già ampiamente ottenute, contengano informazioni sottili sufficienti perché l’AI possa dedurre ciò che una scansione con contrasto avrebbe mostrato. Si sono concentrati su due sequenze comuni: T1 e T2‑FLAIR. Pur non mostrando direttamente la perdita di barriera emato‑encefalica, queste sequenze catturano la struttura del tumore, il gonfiore circostante e i danni tissutali che spesso accompagnano la rottura della barriera. Il team ha sviluppato un sistema chiamato CBSI che prima genera immagini sintetiche con contrasto a partire da queste scansioni senza contrasto e poi le usa, insieme alle immagini originali, per decidere se la barriera è intatta o compromessa in ciascun glioma.
Come funziona il nuovo sistema AI
Al centro di CBSI c’è un modello di diffusione—un tipo di AI che parte da immagini rumorose e le “denoisa” iterativamente fino a ottenere immagini realistiche. Qui impara a trasformare l’input non contrastato in due immagini virtuali alternative con contrasto: una assumendo barriera intatta e una assumendo barriera permeabile. Un meccanismo di guida indica al modello quale pattern di enhancement mirare, e un passaggio ausiliario di segmentazione lo aiuta a prestare maggiore attenzione alla regione tumorale. In una seconda fase, una rete separata confronta i due risultati sintetici per ciascun paziente e valuta quale dei due è più auto‑coerente con i dati MRI originali. Tale decisione viene poi tradotta nello stato predetto della barriera emato‑encefalica.
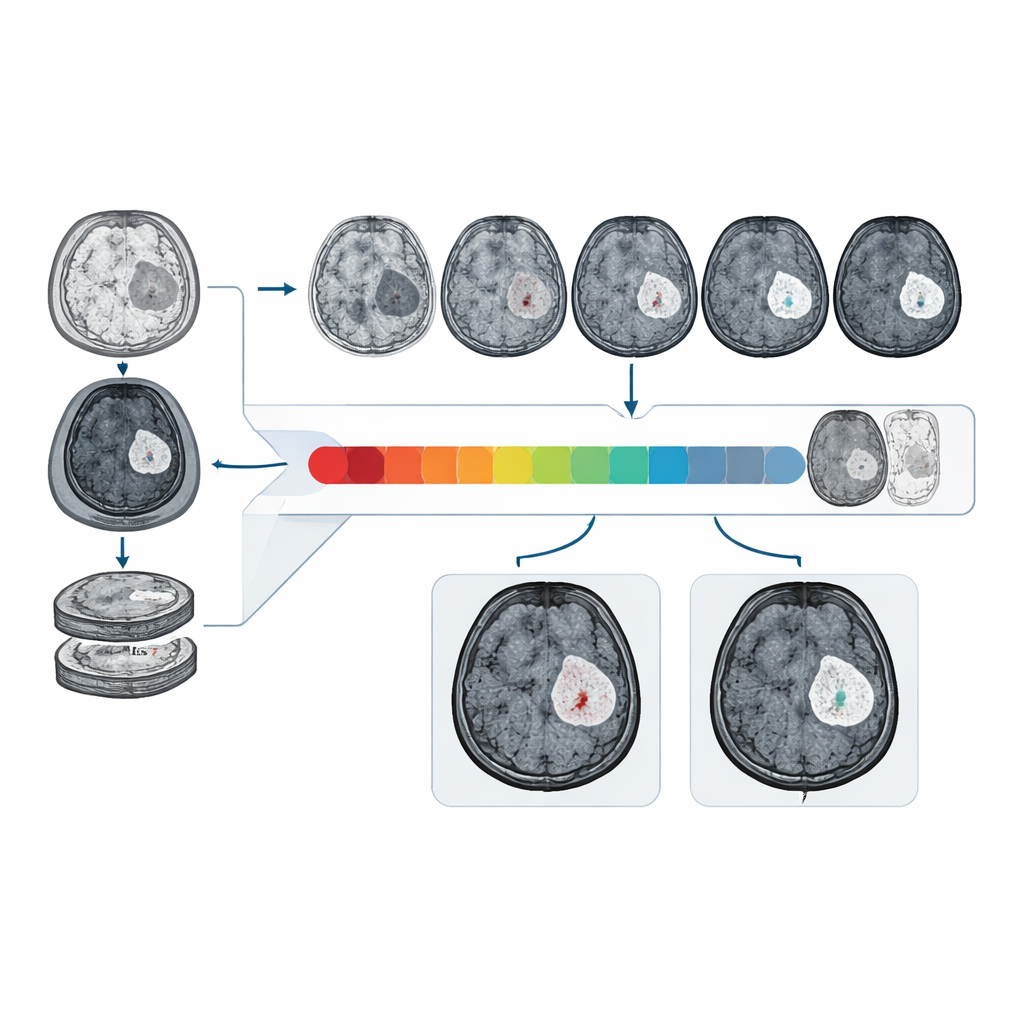
Quanto bene si comporta su dati reali e diversi
I ricercatori hanno addestrato e testato CBSI su dati MRI di 1.535 pazienti con glioma raccolti in più ospedali e da dataset pubblici internazionali. Su un set di test clinico esterno, CBSI ha distinto barriere integre da compromesse con un’area sotto la curva di circa l’81%, chiaramente migliore rispetto a modelli basati solo su immagini non contrastate e avvicinandosi alle prestazioni di modelli che avevano accesso a scansioni con contrasto reali. I radiologi, quando hanno visto mix randomizzati di immagini con contrasto reali e sintetiche prodotte dal sistema, hanno giudicato oltre il 90% delle immagini sintetiche di alta qualità diagnostica, e la loro capacità di identificare l’enhancement sulle immagini sintetiche è stata simile a quella sulle scansioni reali.
Benefici per la pianificazione del trattamento e la cura futura
Poiché le immagini di contrasto sintetiche prodotte da CBSI catturano dettagli tumorali e pattern di enhancement, hanno anche migliorato compiti successivi come il delineamento dei confini tumorali e la stima del grado tumorale—entrambi fortemente dipendenti dal comportamento della barriera emato‑encefalica. Il metodo si è generalizzato bene a differenti scanner, protocolli di imaging e popolazioni di pazienti, inclusi dati dall’Africa subsahariana e ampie coorti internazionali. Pur riconoscendo che ogni sistema di deep‑learning resta uno strumento statistico più che una finestra diretta sulla biologia, i risultati suggeriscono che il contrasto virtuale potrebbe ridurre la dipendenza dagli agenti iniettati, specialmente per pazienti vulnerabili o in contesti dove le scansioni con contrasto sono difficili da ottenere. In termini pratici, questo approccio AI potrebbe permettere ai medici di estrarre informazioni chiave che orientano il trattamento sulla barriera emato‑encefalica dalle scansioni che i pazienti già eseguono—senza una puntura aggiuntiva.
Citazione: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Parole chiave: glioma, barriera emato‑encefalica, risonanza magnetica cerebrale, AI per imaging medico, imaging senza contrasto