Clear Sky Science · it
Anticorpi basati su nanobody bloccano simultaneamente l’attività allergenica ed enzimatica dell’allergene dominante del veleno di ape
Perché le allergie alle punture d’ape sono importanti
Per la maggior parte delle persone, una puntura d’ape è dolorosa ma di breve durata. Per altri, può scatenare una reazione generalizzata potenzialmente letale chiamata anafilassi. Il trattamento preventivo principale oggi disponibile, l’immunoterapia con il veleno, funziona per molti pazienti ma richiede anni, prevede iniezioni frequenti e può a sua volta provocare effetti allergici. Questo studio esplora un modo nuovo e più mirato per proteggere le persone fortemente allergiche al veleno d’ape disattivando un componente chiave del veleno prima che possa causare danno.
Il principale responsabile nel veleno d’ape
Il veleno d’ape è un cocktail di molecole diverse, ma una proteina, chiamata fosfolipasi A2 (o Api m 1), spicca. È l’allergene dominante nei pazienti allergici al veleno d’ape ed è presente in quasi tutti loro. Api m 1 ha un doppio ruolo: danneggia le membrane cellulari, contribuendo al dolore e all’infiammazione nel sito della puntura, ed è anche un bersaglio principale per gli anticorpi che causano allergia noti come IgE. Quando Api m 1 si lega alle IgE ancorate su cellule immunitarie come mastociti e basofili, può innescare una reazione a catena che porta al rilascio improvviso di mediatori infiammatori e, nei casi gravi, all’anafilassi.
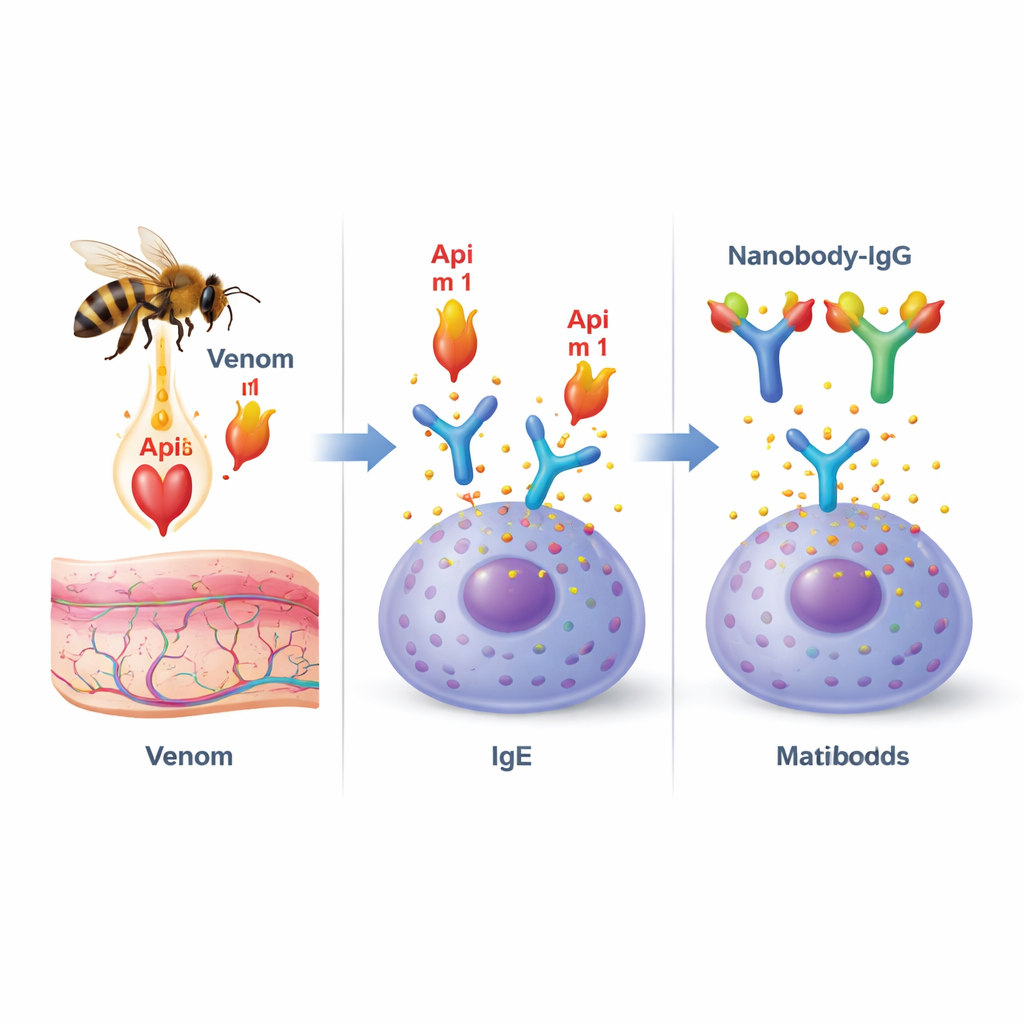
Progettare anticorpi minuscoli per bloccare l’allergene
I ricercatori si sono rivolti ai “nanobody”, piccoli e stabili frammenti di anticorpi scoperti originariamente nei camelidi. Essendo piccoli ed allungati, i nanobody sono particolarmente adatti ad inserirsi in scanalature e tasche delle proteine. Il team ha isolato nanobody specifici per Api m 1 da una libreria immunitaria e ha selezionato due candidati distinti, denominati AM1‑1 e AM1‑4. Lavori strutturali dettagliati con cristallografia a raggi X hanno mostrato che questi due nanobody si agganciano su lati opposti di Api m 1 e non interferiscono tra loro. Un nanobody, AM1‑1, si posiziona direttamente sopra il centro attivo dell’enzima, suggerendo che potrebbe bloccare la funzione di danneggiamento delle membrane di Api m 1, mentre AM1‑4 si ancora in una tasca separata sulla superficie della proteina.
Trasformare i nanobody in potenti bloccanti
Per trasformare questi piccoli leganti in farmaci a lunga durata, gli scienziati hanno fuso ciascun nanobody al frammento Fc dell’IgG1 umano, creando molecole di maggiori dimensioni simili ad anticorpi con migliore stabilità in circolo. Hanno inoltre progettato una versione “bispecifica” che porta sia AM1‑1 sia AM1‑4 in un singolo composto simile a IgG. I test di laboratorio hanno mostrato che queste fusioni nanobody‑IgG si legano ad Api m 1 con affinità estremamente elevata e, quando presenti, possono ridurre fortemente il legame delle IgE provenienti dal sangue di pazienti allergici all’ape con Api m 1. In saggi su cellule, hanno diminuito l’attivazione dei basofili, le cellule immunitarie che normalmente rispondono vigorosamente all’esposizione ad Api m 1 negli individui allergici.
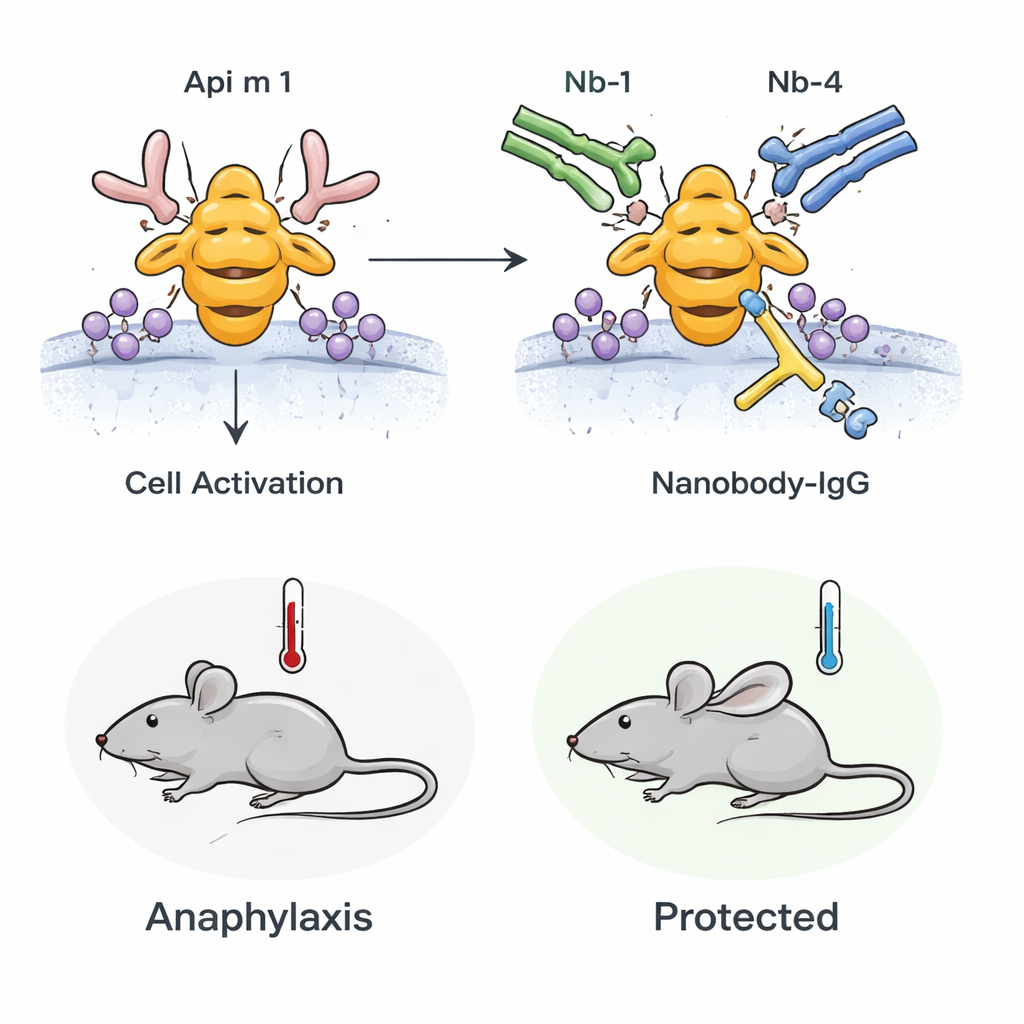
Dalla provetta agli animali viventi
Il team ha poi verificato se questo effetto bloccante si mantenesse in un organismo vivente. Hanno utilizzato topi sensibilizzati al veleno d’ape in modo che il loro sistema immunitario reagisse ad Api m 1 in modo che imita l’allergia umana. Quando questi topi sono stati sfidati con Api m 1, hanno sviluppato segni di anafilassi, inclusa una diminuzione della temperatura corporea e marcatori di attivazione dei mastociti nel sangue. Tuttavia, se i topi erano pretrattati con il nanobody‑IgG bispecifico, sia il calo di temperatura sia l’attivazione dei mastociti sono risultati significativamente ridotti. Ciò dimostra che anticorpi bloccanti preesistenti e ad alta affinità possono attenuare la reazione allergica sistemica ad Api m 1 in vivo.
Cosa potrebbe significare per le persone con allergia al veleno d’ape
Nel complesso, lo studio mostra che molecole IgG basate su nanobody accuratamente progettate possono bloccare simultaneamente le azioni allergeniche ed enzimatiche di Api m 1, il principale colpevole nell’allergia al veleno di ape. Per i pazienti, questo apre la possibilità di un’immunizzazione passiva stagionale: alcune iniezioni di tali anticorpi durante i mesi in cui le punture d’api sono più probabili potrebbero offrire protezione temporanea contro reazioni gravi, senza il lungo impegno e i rischi dell’immunoterapia tradizionale con il veleno. Pur richiedendo ulteriori studi per estendere l’approccio ad altri componenti del veleno e per valutarne sicurezza ed efficacia nell’uomo, questa strategia basata su nanobody offre un modo preciso per proteggere gli individui vulnerabili dalle punture d’api pericolose.
Citazione: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
Parole chiave: allergia al veleno d’api, nanobody, immunoterapia passiva, fosfolipasi A2, prevenzione dell’anafilassi