Clear Sky Science · it
Riconoscimento del promotore mediato da una pinza cooperativa da parte della RNA polimerasi dei poxvirus e del suo partner simile a TBP/TFIIB
Come un virus riconfigura il controllo genico all’interno delle nostre cellule
I poxvirus, che includono il virus storicamente responsabile del vaiolo, effettuano tutta la loro espressione genica nel citoplasma delle nostre cellule, lontano dal centro di controllo del DNA della cellula, il nucleo. Per riuscirci, portano con sé una propria “fabbrica genetica” in miniatura. Questo studio svela, a livello atomico, come uno di questi virus, il Vaccinia, attivi un’onda specifica dei suoi geni a metà infezione, usando una proteina a forma di morsa inaspettata che funziona insieme alla macchina virale di copiatura.
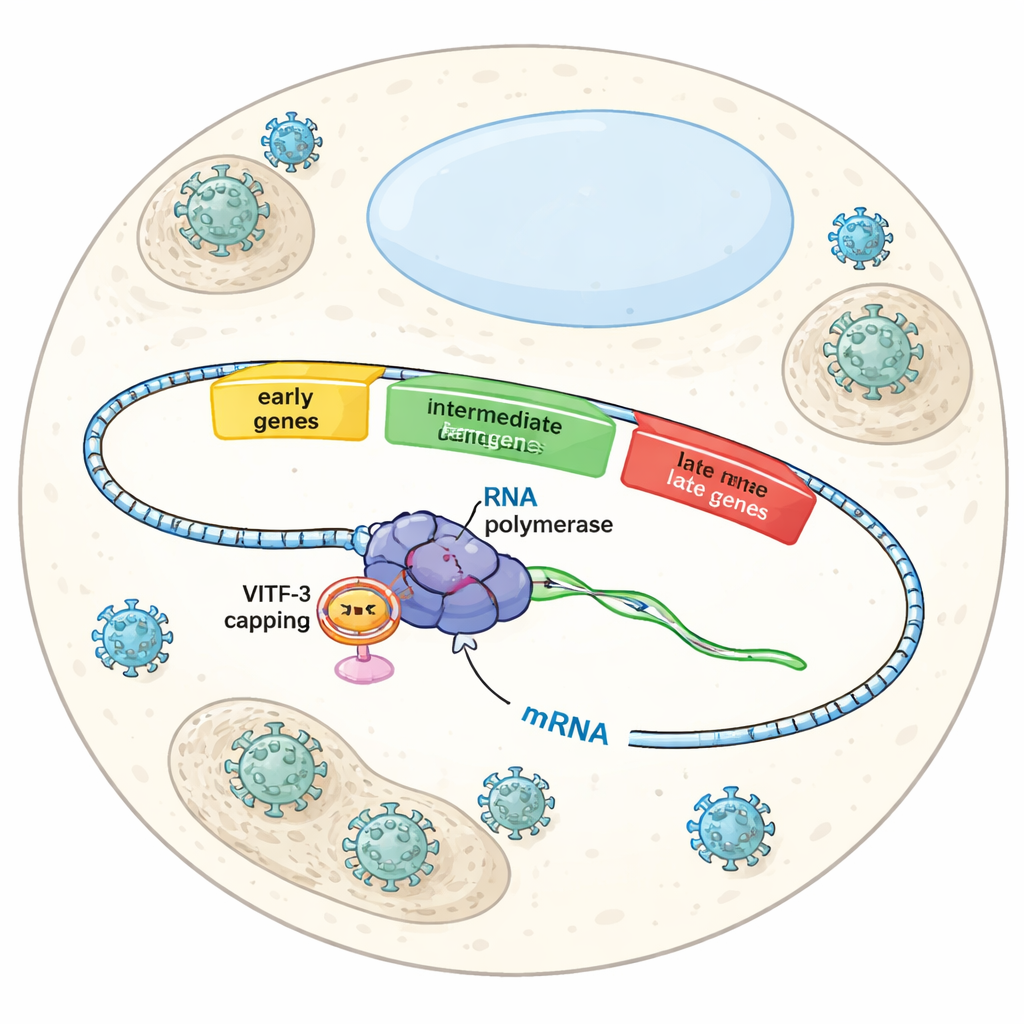
Tre onde in un’assunzione di controllo virale
Quando il Vaccinia infetta una cellula, non attiva tutti i suoi geni contemporaneamente. Segue invece un copione cronometrato con geni precoci, intermedi e tardivi. I geni precoci preparano il terreno per la replicazione virale, i geni intermedi contribuiscono a costruire la macchina per la produzione di nuove particelle virali e i geni tardivi completano l’assemblaggio e l’imballaggio. Ogni ondata dipende dalla stessa RNA polimerasi virale — l’enzima che legge il DNA per produrre RNA — ma fattori helper diversi indicano alla polimerasi quale gruppo di geni attivare in ciascuna fase. Finora gli scienziati comprendevano abbastanza bene il controllo dei geni precoci, ma rimaneva un mistero come il virus riconoscesse e attivasse specificamente i geni intermedi.
Un aiuto ad anello che ha bisogno di un partner
I ricercatori si sono concentrati su una proteina in due parti chiamata VITF‑3, nota per essere necessaria all’attivazione dei geni intermedi. Molti organismi, compresi gli esseri umani, usano una coppia di proteine chiamate TBP e TFIIB per guidare la loro RNA polimerasi al punto giusto sul DNA. Il gruppo ha dimostrato che VITF‑3 è una versione altamente modificata di questa stessa coppia antica. Tuttavia, a differenza dei suoi cugini cellulari, VITF‑3 da sola non si lega al DNA. Invece, i suoi due sottounità si incastrano formando un anello chiuso che è inerte nei confronti del DNA a meno che non sia presente la RNA polimerasi virale. Questo era inatteso, perché nella maggior parte dei sistemi il componente simile a TBP lega prima il DNA del promotore e poi recluta la polimerasi; qui, il virus sembra aver riorganizzato l’ordine degli eventi.
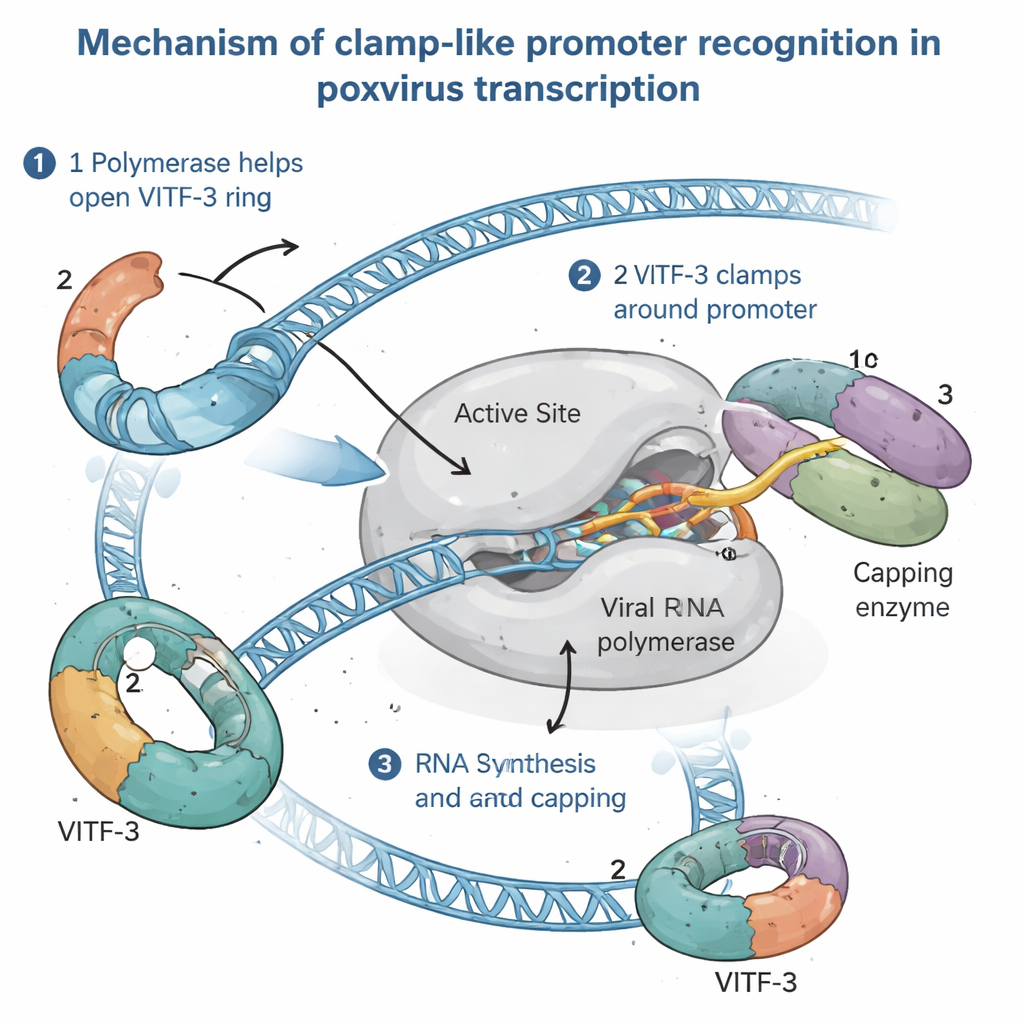
Osservare la macchina di trascrizione intermedia in azione
Per capire come funziona questo assetto insolito, gli autori hanno isolato il complesso pre‑iniziazione intermedio completo — l’assemblaggio pronto poco prima dell’avvio della sintesi dell’RNA — da cellule umane infette. Utilizzando la crio‑microscopia elettronica ad alta risoluzione, hanno visualizzato il complesso a circa 2,4 Ångström di dettaglio, abbastanza fine da vedere le catene laterali degli amminoacidi e le singole basi del DNA. Le immagini hanno rivelato la RNA polimerasi virale che afferra il DNA del promotore, con VITF‑3 che forma un anello stretto attorno a un tratto ricco di AT immediatamente a monte del sito di inizio. Questo anello piega nettamente il DNA di circa 90 gradi e lo convoglia in una fenditura della polimerasi. Allo stesso tempo, un enzima virale di capping — responsabile dell’aggiunta del cappuccio protettivo all’estremità 5′ dell’RNA virale — è ancorato alla polimerasi, pronto a modificare i nuovi trascritti appena emergono.
Un meccanismo di caricamento a morsa ripreso nello spirito
Combinando istantanee strutturali con test biochimici, lo studio propone che la RNA polimerasi virale carichi attivamente VITF‑3 sul DNA, agendo come un “caricatore di morsa”. Innanzitutto, la polimerasi si lega a un promotore intermedio e aiuta ad aprire l’anello di VITF‑3. Poi, insieme all’enzima di capping, richiude l’anello attorno alla regione ricca di AT, bloccando il complesso in posizione. Il DNA si denatura vicino al sito di inizio e la polimerasi legge direttamente un breve segnale di quattro lettere (un motivo TAAA) che indica esattamente dove deve iniziare la sintesi dell’RNA. Man mano che l’RNA cresce, segue lo stesso percorso occupato da una parte di VITF‑3 nel complesso iniziale, quindi l’RNA emergente probabilmente spinge VITF‑3 fuori strada, permettendo alla polimerasi di lasciare il promotore e proseguire lungo il gene mentre VITF‑3 potrebbe restare indietro per favorire il riutilizzo dello stesso promotore.
Cosa significa per la comprensione e il targeting dei poxvirus
In termini semplici, questo lavoro mostra che il virus Vaccinia ha reinterpretato un modulo universale di controllo genico in una morsa che afferra il DNA solo quando la sua stessa RNA polimerasi glielo ordina. Questa soluzione intelligente permette al virus di usare un unico enzima centrale per gestire tre programmi di trascrizione molto diversi, semplicemente scambiando helper specifici della fase. Poiché lo stesso tipo di fattori è conservato in molti poxvirus, inclusi patogeni umani, il meccanismo di caricamento a morsa ora rivelato e l’anello unico di VITF‑3 offrono bersagli strutturali concreti per strategie antivirali volte a interrompere la capacità del virus di temporizzare e controllare i propri geni durante l’infezione.
Citazione: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Parole chiave: trascrizione dei poxvirus, virus Vaccinia, RNA polimerasi, riconoscimento del promotore, fattori di trascrizione