Clear Sky Science · it
Ustilago maydis altera le reti di segnalazione dei carboidrati per indurre ipertrofia nelle cellule ospiti
Quando le malattie delle colture trasformano le cellule in “tumori”
Il mais è una delle colture alimentari e zootecniche più importanti al mondo e ha un nemico insolito: il fungo della carbossidiosi Ustilago maydis, che provoca rigonfiamenti simili a tumori su foglie e pannocchie. Oltre all'aspetto evidente, queste escrescenze dirottano silenziosamente gli zuccheri della pianta lontano dalla crescita e dalla difesa normali, a vantaggio del fungo. Questo studio svela come una singola proteina fungina riesca a ribaltare gli interruttori energetici interni della pianta, trasformando cellule fogliari ordinarie in fabbriche ingrossate, piene di amido, che nutrono il patogeno.
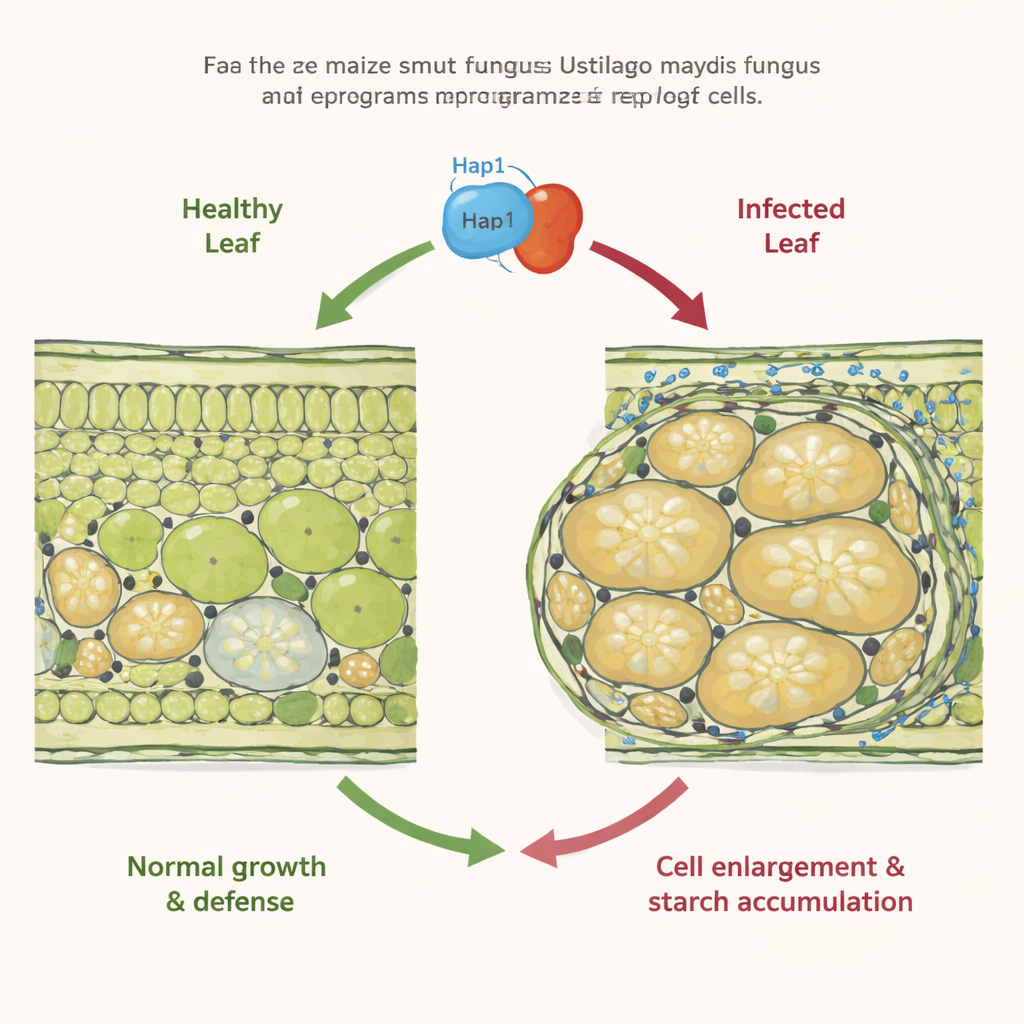
Un fungo che riconfigura la crescita delle piante
La maggior parte dei funghi della carbossidiosi si diffonde silenziosamente nelle colture di cereali e deforma principalmente i fiori. Ustilago maydis è diverso: può formare tumori localizzati su quasi tutte le parti aeree del mais. Lavori precedenti avevano mostrato che nelle foglie infette alcune cellule iniziano a dividersi troppo (iperaplasia), mentre le vicine cellule del mesofillo, che normalmente svolgono la fotosintesi, si ingrossano in modo drammatico (ipertrofia) e smettono di dividersi. Queste cellule ipertrofiche si riempiono anche di granuli di amido in luoghi dove le piante C4 come il mais di solito non immagazzinano amido. Tuttavia, i segnali molecolari alla base di questo estremo ingrossamento cellulare e dell'accumulo di zuccheri erano sconosciuti.
Individuare il trigger fungino dell'ingrossamento cellulare
I ricercatori si sono concentrati sulle proteine “effettori” fungine—molecole secrete nel tessuto vegetale che rimodellano la biologia dell'ospite. Da un elenco di effettori attivi specificamente nelle cellule tumorali ipertrofiche, hanno usato CRISPR‑Cas9 per eliminare diversi geni candidati in U. maydis. Un gene, UMAG_02473, è emerso in modo chiaro: i mutanti privi di questo gene provocavano molti meno tumori e mostravano cellule vegetali con nuclei più piccoli e molto meno amido nel mesofillo fogliare. Poiché i nuclei ingranditi sono un tratto distintivo dell'endoreduplicazione—cellule che duplicano il DNA senza dividersi—il team ha concluso che questo effettore, che hanno chiamato Hap1 (proteina associata all'ipertrofia 1), è cruciale per spingere le cellule del mesofillo verso un programma di crescita senza divisione e per guidare l'accumulo di amido.
Dirottare il termostato energetico della pianta
Per capire come Hap1 rimodella il metabolismo del mais, gli scienziati hanno cercato i suoi bersagli nella pianta. Hanno dimostrato che Hap1 viene consegnato nelle cellule ospiti e si accumula sia nel citoplasma sia nel nucleo. Utilizzando pull‑down proteici e spettrometria di massa, hanno scoperto che Hap1 si lega alla proteina del mais SnRK1, un sensore energetico centrale che normalmente risponde a stress e bassa energia attivando percorsi di rilascio degli zuccheri, riducendo le biosintesi costose in termini energetici (come la formazione di amido) e potenziando le risposte di difesa. Test ulteriori hanno confermato che Hap1 interagisce fisicamente con le subunità catalitiche di SnRK1. Quando Hap1 è presente, i pattern di fosforilazione delle componenti di SnRK1 e di noti proteine bersaglio cambiano, e un saggio diretto di chinasi ha mostrato che Hap1 attenua la capacità di SnRK1 di fosforilare un substrato di prova standard. In breve, Hap1 interferisce con il “termostato” energetico della pianta, indebolendo la sua risposta abituale a stress e carenza di nutrienti.
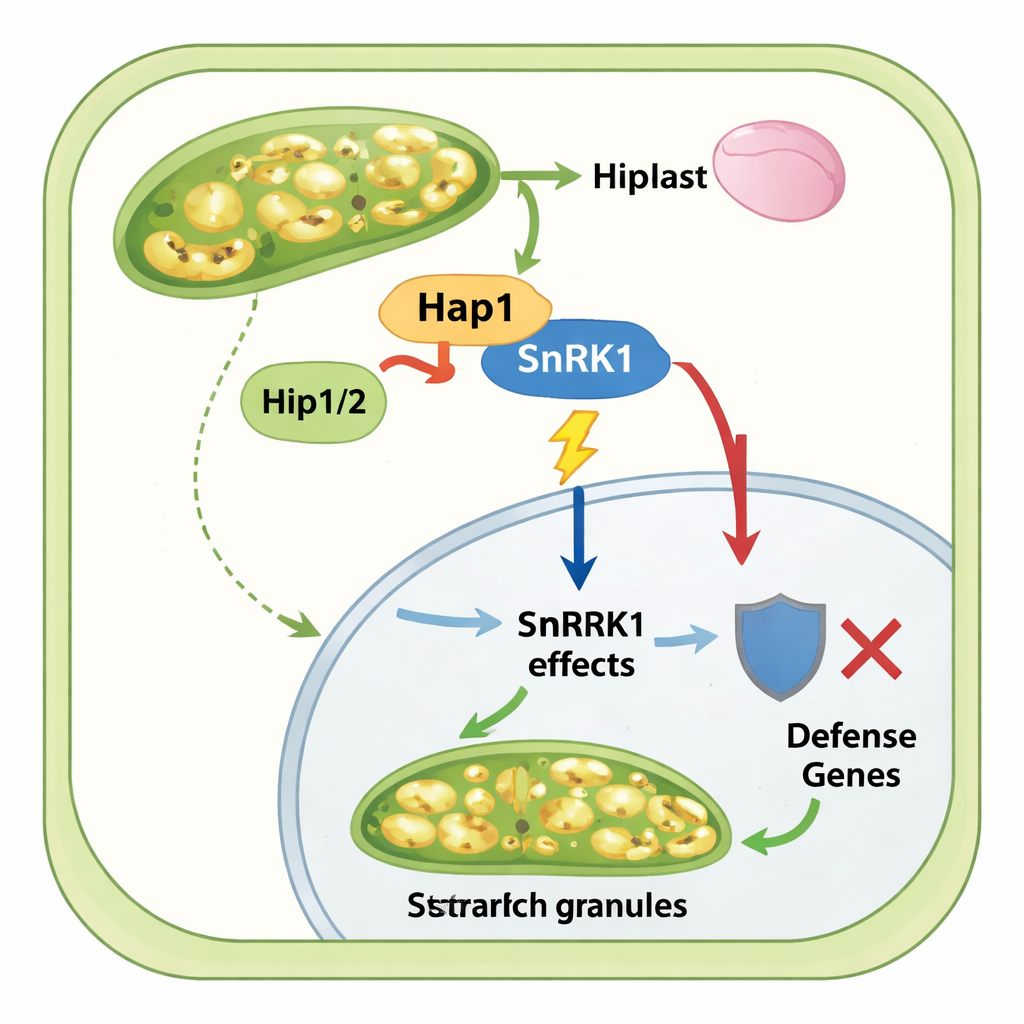
Effettori aiutanti e un nicchia tumorale ricca di zuccheri
La storia non finisce con Hap1 da solo. Il team ha scoperto due effettori fungini aggiuntivi, Hip1 e Hip2, che interagiscono specificamente con Hap1 e sono anch'essi espressi nelle cellule tumorali ipertrofiche. Sebbene la delezione di questi aiutanti avesse un impatto limitato sulla gravità complessiva della malattia, esperimenti biochimici hanno mostrato che Hip1 e Hip2 legano sia Hap1 sia il complesso SnRK1, contribuiscono a mantenere i livelli di proteina Hap1 e sono necessari affinché Hap1 possa effettivamente co‑precipitare SnRK1 dal tessuto di mais infetto. Dati di fosfoproteomica ed espressione genica insieme hanno mostrato che quando Hap1 è presente, i tumori del mais sovraregolano geni e enzimi della biosintesi dell'amido, mentre i geni legati alla difesa della pianta e alla normale macchina proteica sono attenuati. In assenza di Hap1, l'accumulo di amido nelle cellule del mesofillo diminuisce drasticamente e le vie di segnalazione legate a stress e difesa diventano più attive.
Cosa significa per il mais e le sue difese
In termini comprensibili, questo lavoro mostra che Ustilago maydis non ha successo solo danneggiando i tessuti, ma manipolando abilmente i controlli energetici interni della pianta. L'effettore Hap1, sostenuto dai partner Hip1 e Hip2, sembra mettere “in muto” SnRK1, un guardiano chiave che normalmente conserva energia e sostiene le difese immunitarie. Con questa salvaguardia indebolita, le cellule del mesofillo del mais smettono di comportarsi come normali fabbriche verdi e invece si ingrossano, duplicano il DNA senza dividersi e accumulano amido. Queste cellule simili a tumori diventano isole ricche di nutrienti che nutrono il fungo. Comprendere questa strategia fungina apre la strada alla selezione o all'ingegneria di varietà di mais in cui SnRK1 o percorsi correlati siano meno vulnerabili, aiutando le colture a resistere alle infezioni che formano tumori senza sacrificare la crescita.
Citazione: Lee, Y.J., Zhang, D., Stolze, S.C. et al. Ustilago maydis disrupts carbohydrate signaling networks to induce hypertrophy in host cells. Nat Commun 17, 1990 (2026). https://doi.org/10.1038/s41467-026-69532-8
Parole chiave: carie del mais, immunità delle piante, effettori fungini, metabolismo dell'amido, segnalazione SnRK1