Clear Sky Science · it
FOXF2 regola il segnale pericitico–endoteliale necessario per l’omeostasi vascolare dopo danno polmonare neonatale da iperossia
Perché i polmoni dei neonati devono essere protetti con cura
Per i bambini nati prematuri, respirare può essere faticoso. Molti necessitano di ossigeno supplementare per sopravvivere, ma questa terapia salvavita può anche danneggiare i loro fragili polmoni e i vasi sanguigni, contribuendo a una condizione cronica chiamata displasia broncopolmonare. Questo studio esplora un gruppo poco noto di cellule di supporto che avvolgono i minuscoli vasi polmonari e svela un interruttore genetico chiave che aiuta queste cellule a proteggere e riparare il polmone del neonato dopo un danno indotto dall’ossigeno.
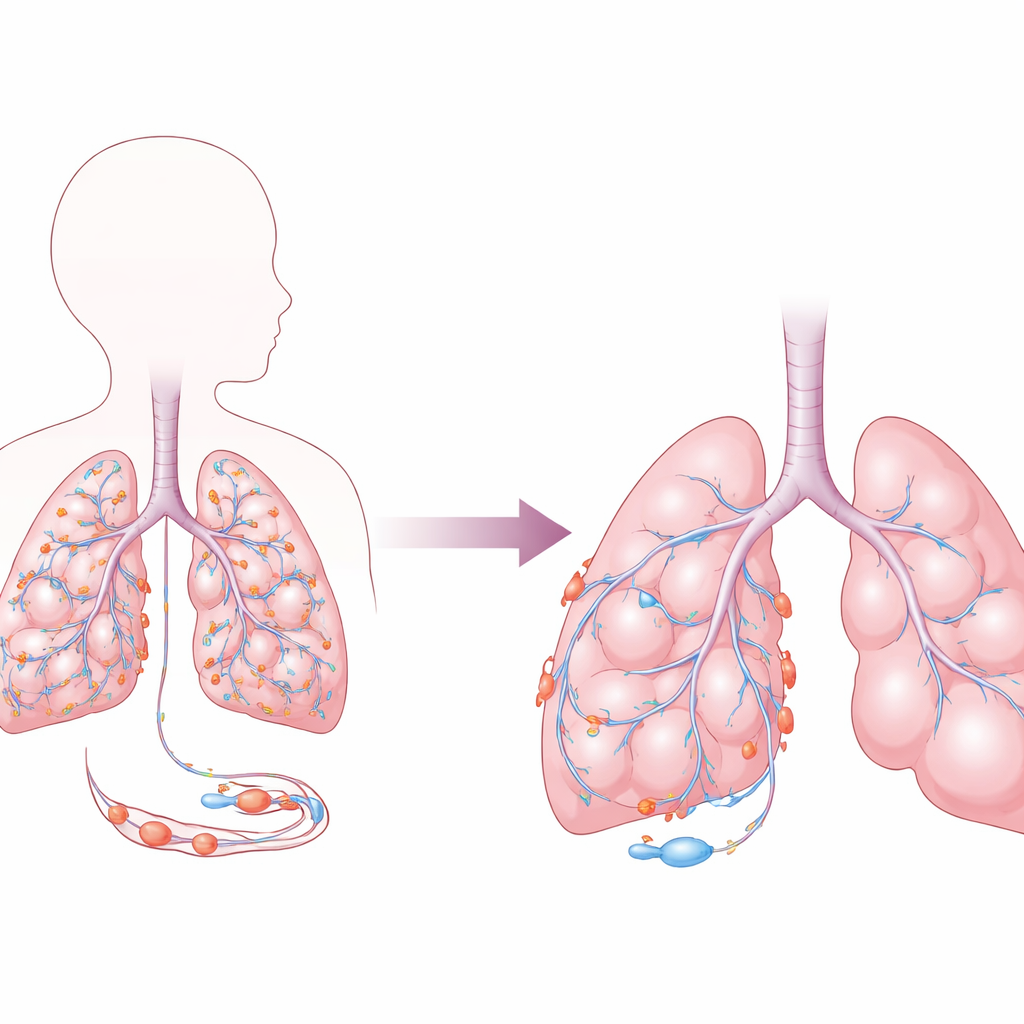
Gli aiutanti nascosti intorno ai vasi polmonari
Gli alveoli polmonari, dove l’ossigeno entra nel sangue, sono rivestiti da una densa rete di capillari. Avvolti attorno a molti di questi capillari ci sono i periciti, cellule di supporto che contribuiscono a mantenere la stabilità dei vasi, guidare la crescita di nuovi vasi e preservare una barriera ermetica in modo che i liquidi non fuoriescano negli spazi aerei. Gli autori si sono concentrati su un gene chiamato FOXF2, un fattore di trascrizione che controlla quali altri geni vengono attivati o repressi all’interno dei periciti. Analizzando dati di RNA a singola cellula provenienti da polmoni di topo in sviluppo, hanno osservato che l’attività di Foxf2 nei periciti aumenta dopo la nascita in parallelo a geni associati alla maturità dei periciti, allo sviluppo vascolare e alla migrazione cellulare. Al contrario, la sua attività è molto più bassa in altri tipi cellulari vicini, suggerendo un ruolo specializzato in queste cellule di supporto vascolare.
Quando si rimuove il freno dai periciti
Per verificare cosa faccia realmente FOXF2, il gruppo ha generato topi in cui Foxf2 poteva essere eliminato specificamente nei periciti PDGFRβ-positivi subito dopo la nascita. In condizioni di ossigeno normali, la struttura polmonare complessiva e i livelli di ossigeno nel sangue sembravano per lo più normali, ma i dettagli rivelavano un quadro diverso. I periciti si moltiplicavano in modo eccessivo e si disponevano in modo denso attorno ai capillari, mentre i marcatori dei periciti maturi e ben funzionanti diminuivano. Questi periciti erano più frequentemente nella fase di sintesi del DNA del ciclo cellulare, e esperimenti in vitro confermarono che bloccare Foxf2 direttamente in periciti coltivati aumentava la loro proliferazione e riduceva la migrazione. Allo stesso tempo, geni che normalmente favoriscono la crescita e la stabilità dei vasi, come Angptl4 e Angpt2, risultavano down-regolati, mentre geni che guidano la divisione cellulare e la produzione energetica erano up-regolati. Nel complesso, il quadro è quello di periciti numerosi ma meno competenti.
Lo stress ossigeno mette in luce una debolezza critica
Le conseguenze sono diventate molto più gravi quando i topi neonati sono stati esposti a livelli elevati di ossigeno, un modello standard di danno polmonare pretermine. Sia nei polmoni dei topi sia in campioni umani di neonati con displasia broncopolmonare, FOXF2 nei periciti risultava marcatamente ridotto dopo tale lesione. Quando i topi privi di Foxf2 sperimentavano iperossia, la loro sopravvivenza calava drasticamente, la saturazione di ossigeno nel sangue diminuiva e gli alveoli diventavano ingranditi e semplificati, indice di scarso sviluppo alveolare. Contemporaneamente, la copertura capillare negli alveoli si riduceva, le cellule endoteliali si dividevano meno e più tracciante fluorescente fuoriusciva dai vasi nel tessuto polmonare—segno di una barriera vascolare compromessa. La citometria a flusso ha confermato che, sotto danno, il numero di cellule endoteliali diminuiva mentre i periciti si accumulavano ulteriormente e restavano altamente proliferativi, evidenziando un collasso della normale collaborazione tra questi due tipi cellulari.
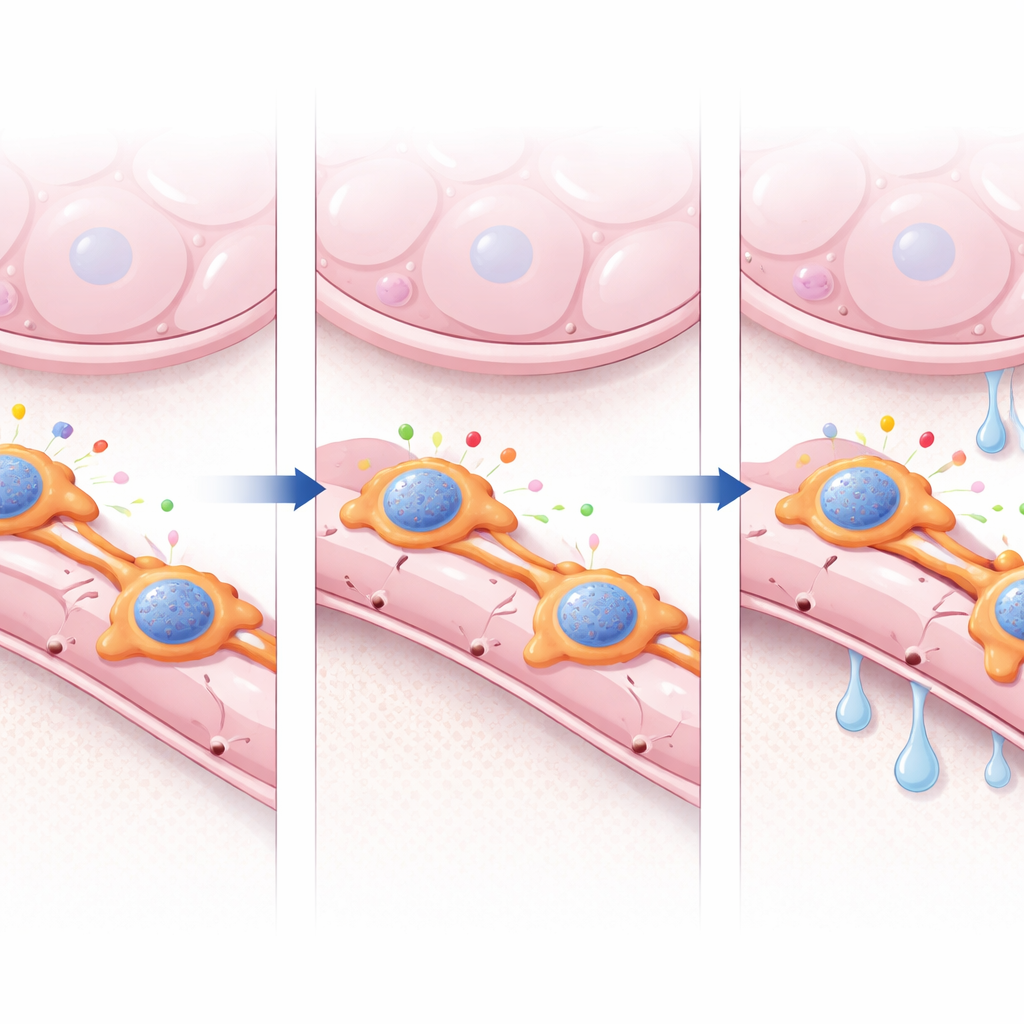
Come i segnali dei periciti plasmano la riparazione dei vasi
Approfondendo il dialogo molecolare, i ricercatori hanno utilizzato strumenti computazionali per mappare le vie di segnalazione tra periciti e cellule endoteliali. Nei polmoni sani erano prominenti percorsi che promuovono la crescita e la stabilità dei vasi, incluso quello che coinvolge ANGPTL4, una proteina secreta con ruoli pro-angiogenici e nella modulazione della barriera. Nei polmoni privi di Foxf2 questi segnali utili si indebolivano, mentre si rinforzavano vie legate allo stress e all’infiammazione. Il mezzo condizionato da periciti carenti di Foxf2 supportava meno formazione di tubi da parte di cellule endoteliali polmonari umane in coltura, ma l’aggiunta di ANGPTL4 ricombinante in parte recuperava questo difetto, indicando un asse FOXF2–ANGPTL4 come motore chiave della riparazione. Il profilo della cromatina ha inoltre rivelato che FOXF2 si lega in prossimità di molti geni pro-angiogenici e contribuisce a mantenere accessibili le regioni di DNA circostanti. Quando FOXF2 viene perso, l’accessibilità cala in migliaia di questi siti, incluso il locus di Angptl4, suggerendo che FOXF2 agisce come un organizzatore della cromatina che permette ad altri fattori di mantenere un programma pericitico sano.
Cosa significa per i polmoni fragili dei neonati
Nel complesso, i risultati mostrano che FOXF2 funge da regolatore maestro che mantiene i periciti polmonari neonatali maturi, contenuti nella loro crescita e capaci di inviare i segnali corretti alle cellule endoteliali vicine. Quando i livelli di FOXF2 scendono dopo un danno da ossigeno, i periciti diventano abbondanti ma disfunzionali: inviano meno segnali di supporto come ANGPTL4, i capillari non riescono a rigenerarsi correttamente, le pareti dei vasi diventano permeabili e l’architettura degli alveoli si deteriora. Per le famiglie e i clinici che assistono i neonati prematuri, questo lavoro mette in evidenza i periciti—e le reti geniche guidate da FOXF2 al loro interno—come promettenti bersagli per future terapie mirate a preservare i piccoli vasi, migliorare lo scambio gassoso e ridurre il danno polmonare a lungo termine dopo l’esposizione precoce all’ossigeno.
Citazione: Sun, F., Zhao, Y., Do, J. et al. FOXF2 regulates pericyte–endothelial signaling required for vascular homeostasis after neonatal hyperoxic lung injury. Nat Commun 17, 2691 (2026). https://doi.org/10.1038/s41467-026-69525-7
Parole chiave: displasia broncopolmonare, sviluppo polmonare, periciti, angiogenesi, iperossia neonatale