Clear Sky Science · it
Terapia termica interstiziale laser e pembrolizumab adiuvante in astrocitoma ad alto grado recidivante: uno studio di Fase 1/Fase 2b randomizzato
Perché questo studio sul cancro cerebrale è importante
L'astrocitoma ad alto grado recidivante, incluso il glioblastoma, è uno dei tumori cerebrali più letali e i trattamenti attuali raramente riescono a controllarlo a lungo. Questo studio testa una strategia in due fasi che utilizza il calore di un laser per distruggere il tessuto tumorale e aprire le difese del cervello, seguita da un farmaco immunitario che aiuta i linfociti T dell’organismo ad attaccare eventuali cellule neoplastiche residue. Per pazienti e famiglie che affrontano questa diagnosi, il lavoro esplora se una procedura minimamente invasiva possa trasformare un tumore quasi non responsivo in uno che finalmente reagisce all’immunoterapia.
Un nuovo modo di affrontare tumori cerebrali ostinati
I pazienti in questo trial avevano tutti astrocitomi ad alto grado recidivati dopo la terapia standard, che di norma comprende chirurgia, radioterapia e chemioterapia. I ricercatori si sono concentrati su due strumenti. Il primo, la terapia termica interstiziale laser (LITT), è una procedura a “foro chiave” in cui una sottile sonda viene guidata tramite risonanza magnetica nel tumore e usata per riscaldare e uccidere il tessuto canceroso, risparmiando gran parte del cervello circostante. Il secondo strumento è il pembrolizumab, un farmaco immunoterapico ampiamente usato che blocca PD-1, un “freno” molecolare che spesso impedisce ai linfociti T di attaccare i tumori. I tentativi precedenti di usare da soli questi farmaci in questi tumori cerebrali erano stati deludenti. Il team quindi si è chiesto se usare prima il laser potesse preparare il tumore e il sistema immunitario a rispondere meglio al pembrolizumab. 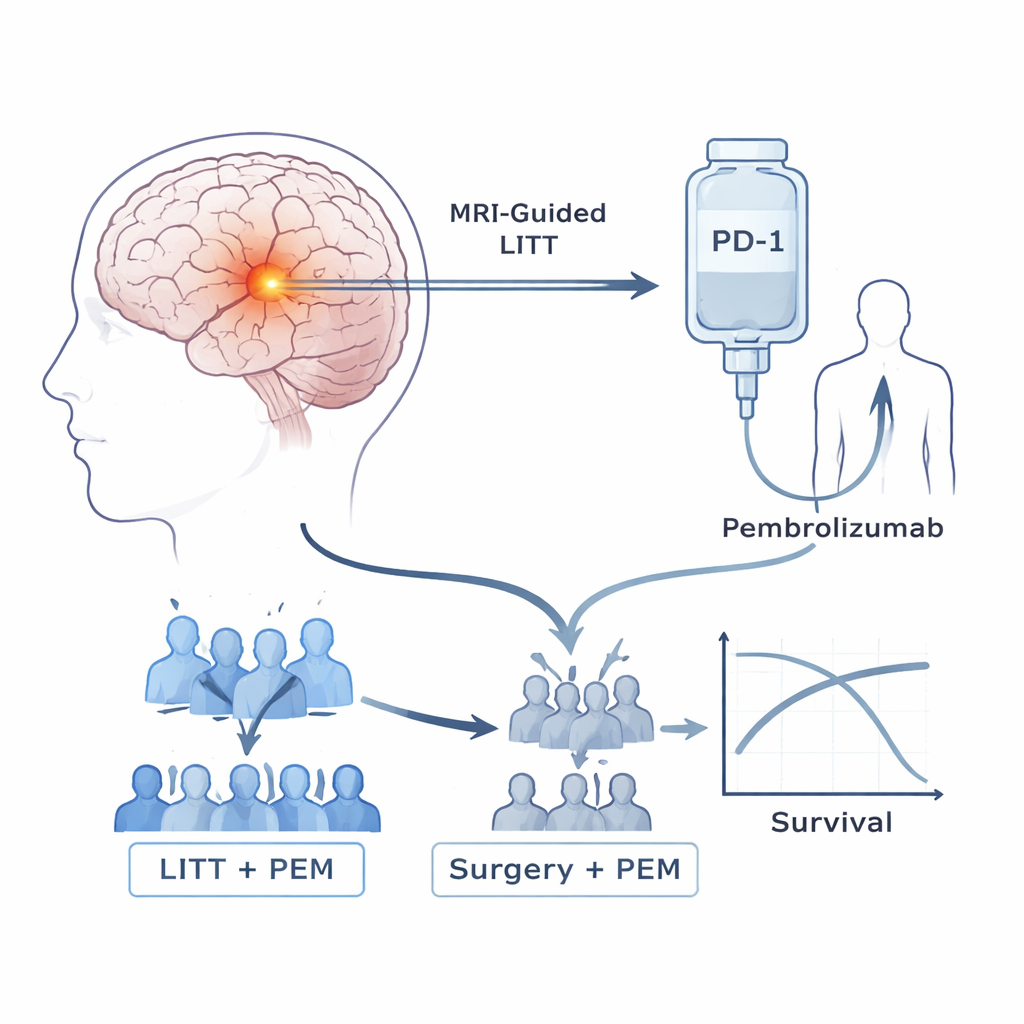
Come è stato condotto il trial clinico
Lo studio è iniziato con una piccola fase di sicurezza, che ha mostrato che i pazienti potevano ricevere in sicurezza pembrolizumab ogni tre settimane dopo la LITT, senza effetti collaterali dose-limitanti. È poi passato a un trial di Fase 2b. Inizialmente i pazienti venivano assegnati in modo casuale a uno dei due gruppi: LITT seguita da pembrolizumab, oppure una rivascolarizzazione chirurgica convenzionale senza laser, seguita da pembrolizumab. Con il crescere delle evidenze esterne che la chirurgia più immunoterapia offriva poco beneficio da sola, un comitato indipendente ha riesaminato i risultati precoci di questo trial. Vedendo segnali che il gruppo senza laser stava andando peggio mentre il gruppo LITT pareva vivere più a lungo, hanno interrotto la randomizzazione e tutti i pazienti successivi hanno ricevuto la combinazione laser più farmaco.
Cosa è successo alla sopravvivenza e al controllo del tumore
Tra i 39 pazienti che hanno ricevuto il trattamento secondo il piano, quelli trattati con LITT più pembrolizumab hanno vissuto in modo significativamente più lungo rispetto a chi aveva subito chirurgia più pembrolizumab. La sopravvivenza globale mediana è stata circa 11,8 mesi con l’approccio combinato LITT, contro 5,2 mesi con la sola chirurgia, e nessuno dei pazienti operati senza laser era vivo a 18 mesi rispetto al 42% di quelli del gruppo LITT. Anche il tempo prima della ripresa di crescita tumorale è migliorato, passando da 1,6 mesi nel gruppo chirurgico a 4,5 mesi con la LITT. Circa il 27% dei pazienti trattati con LITT ha mostrato una riduzione misurabile dei tumori e il 70% ha ottenuto almeno un controllo temporaneo della malattia, mentre tutti i pazienti sottoposti a chirurgia non laser più pembrolizumab hanno avuto progressione. Gli effetti collaterali della terapia combinata sono stati per lo più lievi e gestibili, con alcuni casi di diarrea, debolezza muscolare e aumenti degli enzimi epatici, ma nessun decesso correlato al trattamento.
Cosa faceva il sistema immunitario
Per capire perché la combinazione potesse funzionare, gli scienziati hanno esaminato attentamente nel tempo le cellule del sangue usando RNA-sequenziamento a singola cellula e il tracciamento del recettore delle cellule T. Dopo la LITT hanno osservato un gruppo specifico di cellule immunitarie innate, chiamate monociti non classici, che si sono spostate verso uno stato più attivo associato a migrazione, infiammazione e interazione con le cellule T—cambiamenti non riscontrati dopo la chirurgia standard. Quando è stato poi avviato il pembrolizumab, i pazienti che sono sopravvissuti più a lungo hanno mostrato forti ondate di attivazione e espansione clonale delle cellule T CD8, cioè molte cellule T identiche che prendevano di mira gli stessi antigeni si moltiplicavano. Queste cellule T tendevano a entrare in stati di memoria ed effetto capaci di riconoscere e uccidere le cellule tumorali, piuttosto che diventare esauste e inefficaci. I sopravvissuti a lungo termine hanno anche mostrato una diminuzione di IDO-1, una molecola associata alla soppressione immunitaria, suggerendo che la combinazione possa alleviare più strati del “freno” immunitario. 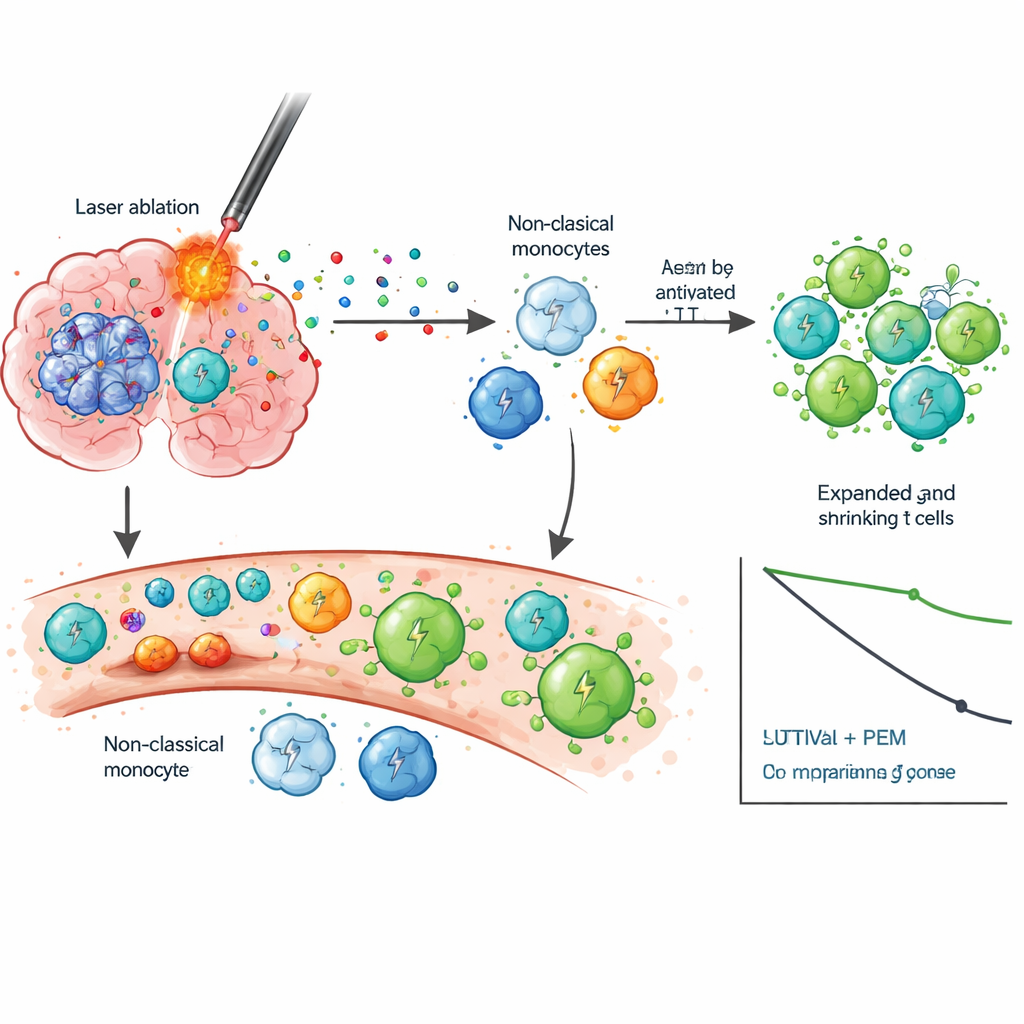
Cosa potrebbe significare per i pazienti
Per le persone con astrocitoma ad alto grado recidivante, questo lavoro suggerisce che usare l’ablazione laser guidata da MRI per ridurre il volume tumorale, allentare temporaneamente la barriera emato‑encefalica e liberare frammenti tumorali nella circolazione può preparare il terreno perché l’immunoterapia funzioni dove di norma fallisce. Accendendo una “lanterna” per il sistema immunitario e poi rimuovendo il freno PD‑1 con pembrolizumab, la combinazione sembra generare risposte delle cellule T più durature e prolungare la sopravvivenza in un tumore con pochissime opzioni. Poiché lo studio è stato relativamente piccolo e la randomizzazione è terminata precocemente, gli autori sottolineano che sono necessari studi più ampi e controllati. Anche così, i risultati indicano una strategia promettente: associare la distruzione fisica del tumore mirata con farmaci immunitari per trasformare un tumore cerebrale “freddo” e resistente in uno che il corpo può finalmente riconoscere e combattere.
Citazione: Campian, J.L., Le, S.B., Ghiaseddin, A. et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun 17, 1763 (2026). https://doi.org/10.1038/s41467-026-69522-w
Parole chiave: glioblastoma, ablazione laser, pembrolizumab, immunoterapia, tumore cerebrale