Clear Sky Science · it
Segnalazione eccessiva di FGFR3 nell acondroplasia altera il ricambio dei condrociti della zona di riposo tramite la via CREB
Perché questo studio sulla crescita ossea è importante
L'acondroplasia è la causa più comune di nanismo a arti corti di origine genetica. Non interessa soltanto l'altezza, ma anche la salute della colonna vertebrale, la mobilità e la qualità della vita. I trattamenti attuali aiutano ma non ripristinano completamente la crescita ossea. Questo studio utilizza un modello murino sofisticato per scoprire una zona del processo di crescita finora nascosta e indica un nuovo interruttore di segnalazione, chiamato CREB, come bersaglio promettente per terapie future.
Come crescono in lunghezza le ossa sane
Le ossa lunghe, come il femore nella coscia, si allungano nelle placche di crescita vicino alle loro estremità. Queste placche sono organizzate in tre strati principali di cellule cartilaginee. In cima si trova la zona di riposo, dove le cellule si comportano come un serbatoio di cellule staminali, dividendosi lentamente e inviando le cellule figlie verso il basso. Sotto c’è la zona proliferativa, che contiene cellule a rapida divisione disposte in colonne ordinate che guidano l’allungamento. Più avanti, la zona ipertrofica ospita cellule ingrandite e mature che contribuiscono alla formazione del nuovo osso. L’equilibrio tra queste zone mantiene la crescita ossea al ritmo e alla forma corretti.
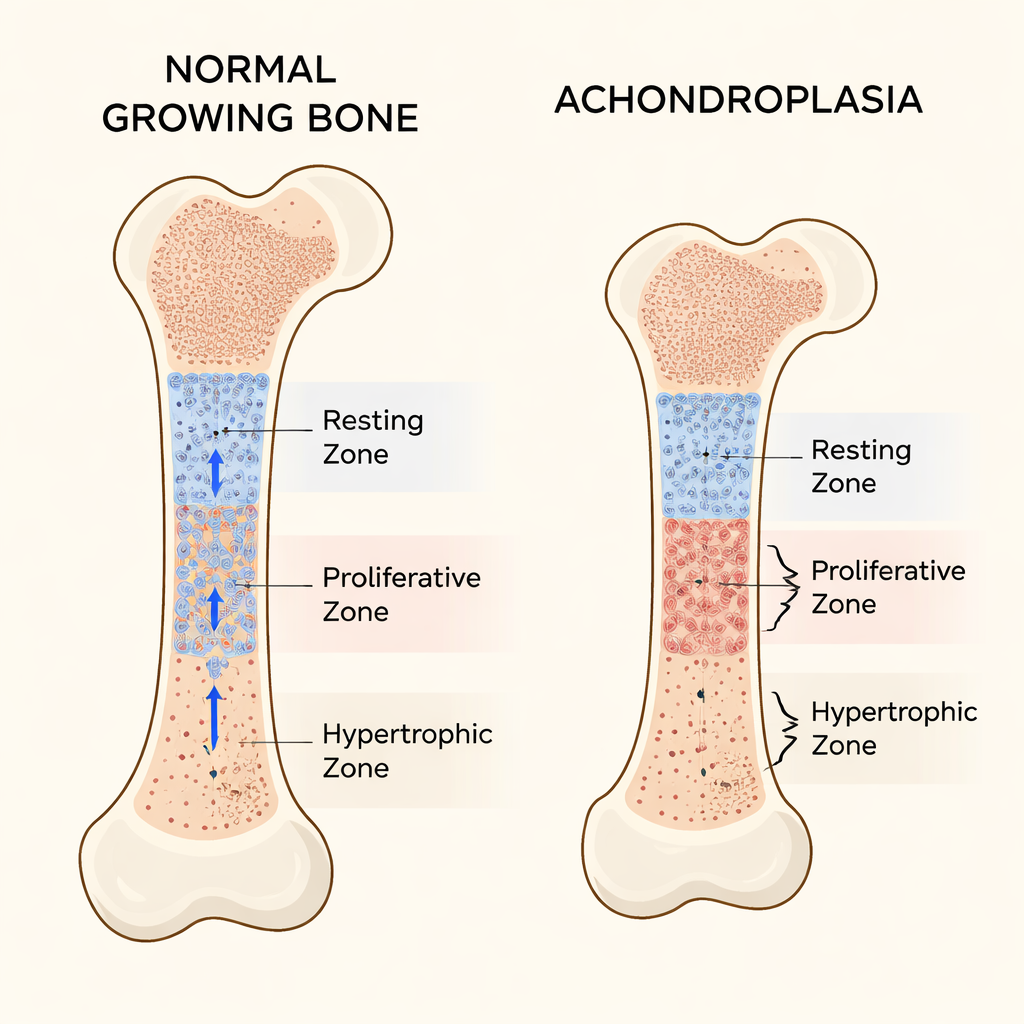
Cosa va storto nell acondroplasia
Nella maggior parte delle persone con acondroplasia, una singola mutazione nel gene FGFR3 rende il suo recettore iperattivo, frenando la crescita ossea. Lavori precedenti avevano mostrato che questa segnalazione rallenta la divisione cellulare nella zona proliferativa e blocca l’ingrandimento finale delle cellule nella zona ipertrofica. Utilizzando topi ingegnerizzati per portare la mutazione umana dell acondroplasia, gli autori hanno confermato arti molto corti e placche di crescita accorciate. Ma misurazioni accurate hanno rivelato qualcosa che era stato in gran parte trascurato: la zona di riposo stessa diventava insolitamente spessa. Invece di fungere da serbatoio stabile e ben regolato di cellule staminali, questa regione si espandeva e conteneva cellule povere della normale matrice cartilaginea.
Le cellule della zona di riposo perdono il comportamento “simile a staminale”
Per capire questa espansione, il team ha seguito come le cellule della placca di crescita si dividevano e si muovevano nel tempo. Nei topi normali, le cellule della zona di riposo si dividevano raramente e le loro discendenti migravano verso il basso in colonne rette per rifornire la zona proliferativa. Nei topi mutanti, molte più cellule nella zona di riposo si dividevano lentamente e rimanevano al loro posto, accumulandosi in uno strato affollato che non alimentava correttamente le zone inferiori. Il tracciamento di lignaggi con etichette genetiche multicolore ha mostrato che le colonne clonali erano corte e disorganizzate, con cellule figlie che si disperdevano in direzioni casuali invece di formare pile ordinate. I marcatori di identità simile a cellule staminali, come la proteina CD73, andavano persi nella zona di riposo espansa, suggerendo che l iperattività di FGFR3 aveva corrotto il nichio staminale normale.
Un nuovo colpevole nella segnalazione: CREB
I ricercatori hanno poi usato il sequenziamento dell'RNA a singola cellula per profilare migliaia di singole cellule della placca di crescita. Hanno identificato un cluster distinto che corrispondeva alla zona di riposo espansa ed era ricco di un gene chiamato Spon1, tra gli altri. L’analisi dei percorsi ha messo in evidenza l’attivazione di CREB, una proteina che attiva geni quando è fosforilata. La microscopia ha mostrato che le cellule della zona di riposo nei topi mutanti esprimevano fortemente CREB attivato e il suo coattivatore CBP, insieme ad alti livelli di FGFR3 e molecole a valle come STAT5. In colture cellulari, la stimolazione della via FGFR3 aumentava l’attività di CREB e incrementava SPONDIN1 (la proteina SPON1), mentre il blocco di FGFR3 o di CREB riduceva questi segnali. Ciò pone CREB come un relè chiave tra il recettore iperattivo sulla superficie cellulare e il comportamento difettoso delle cellule della zona di riposo.
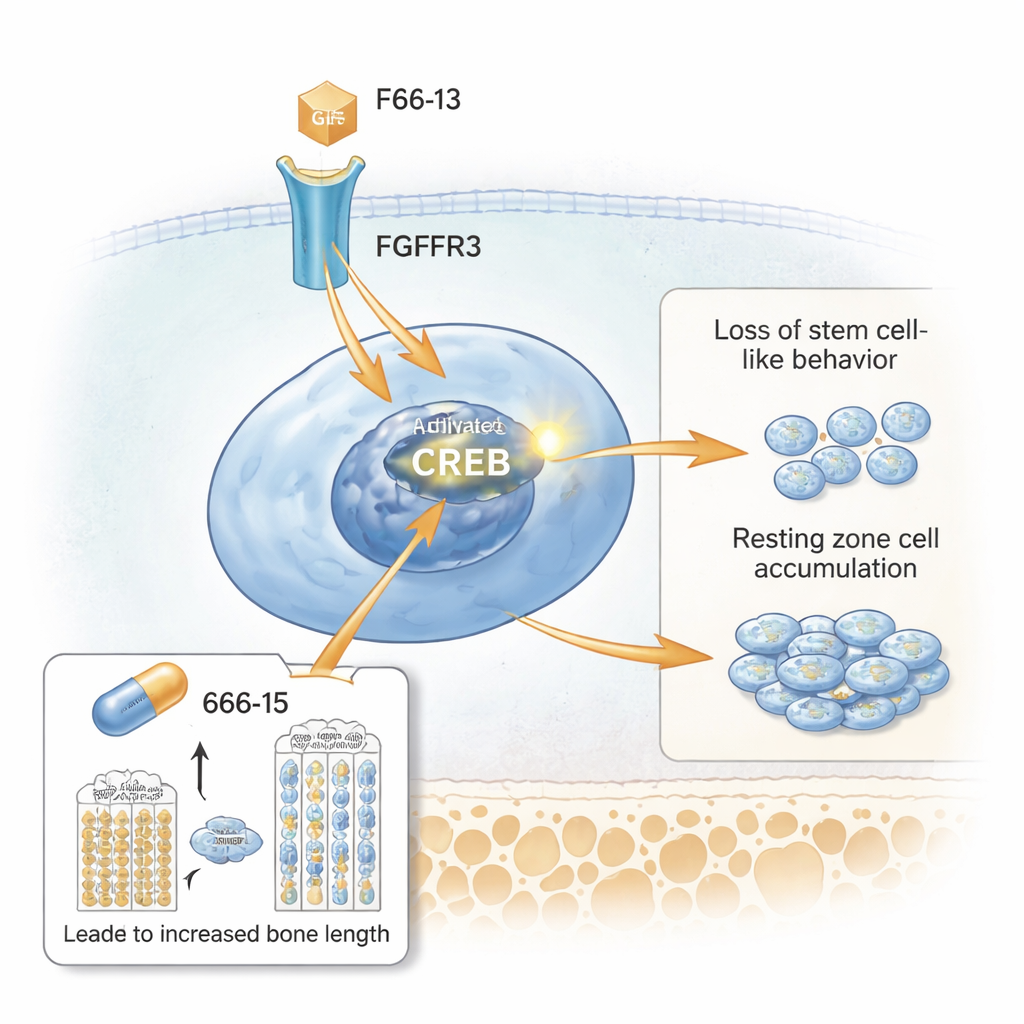
Testare un farmaco che attenua CREB
Infine, il team ha chiesto se ridurre CREB potesse attenuare i problemi di crescita. Hanno trattato topi modello di acondroplasia con un inibitore di piccola molecola di CREB, chiamato 666-15, durante il periodo di rapida crescita dopo la nascita. Rispetto ai topi mutanti non trattati, quelli trattati con 666-15 avevano maggiore peso corporeo e femori più lunghi. Le loro placche di crescita apparivano più normali: la zona di riposo si assottigliava, le zone proliferativa e ipertrofica recuperavano in altezza e le proteine della matrice cartilaginea ricomparivano. I marcatori di segnalazione CREB iperattiva, inclusi fosfo-CREB, SPONDIN1 e STAT5, diminuivano nella zona di riposo, mentre il marcatore simile a cellule staminali CD73 ritornava. Importante, lo stesso farmaco aveva scarso effetto nei topi di controllo sani alla dose testata, suggerendo che agisca principalmente quando CREB è anormalmente alto.
Cosa significa per i trattamenti futuri
Lo studio mostra che nell acondroplasia l iperattività di FGFR3 fa più che rallentare la divisione e l’ingrandimento cellulare; deraglia anche la tranquilla zona di riposo simile a staminale attivando CREB. Questa perturbazione priva le zone inferiori della placca di crescita di nuove cellule e contribuisce alle ossa corte. Farmaci esistenti come vosoritide mirano principalmente ad altre vie nelle zone proliferativa e ipertrofica e ripristinano solo parzialmente la lunghezza ossea. Aggiungendo CREB all’elenco dei bersagli—soprattutto nella zona di riposo—terapie combinate future potrebbero normalizzare più completamente la crescita nei bambini con acondroplasia.
Citazione: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
Parole chiave: acondroplasia, FGFR3, placa di crescita, cellule staminali della cartilagine, segnalazione CREB