Clear Sky Science · it
Densità di carica del metallo idratato come descrittore universale che spiega le variazioni meccanicistiche nell'attivazione del periodato per la degradazione degli inquinanti
Ripulire l'acqua con chimica intelligente
Molti farmaci e prodotti chimici industriali sfuggono agli impianti di trattamento convenzionali e finiscono nei fiumi e nelle acque potabili. Questo studio esplora un metodo promettente per scomporre tali inquinanti ostinati usando un comune agente ossidante, il periodato, e mostra che una proprietà semplice degli ioni metallici in acqua può predire quanto — e quanto in modo sicuro — questa chimica funzionerà. Comprendere questa regola potrebbe aiutare i progettisti a sviluppare sistemi di trattamento più puliti ed efficienti per acque reali e diverse.
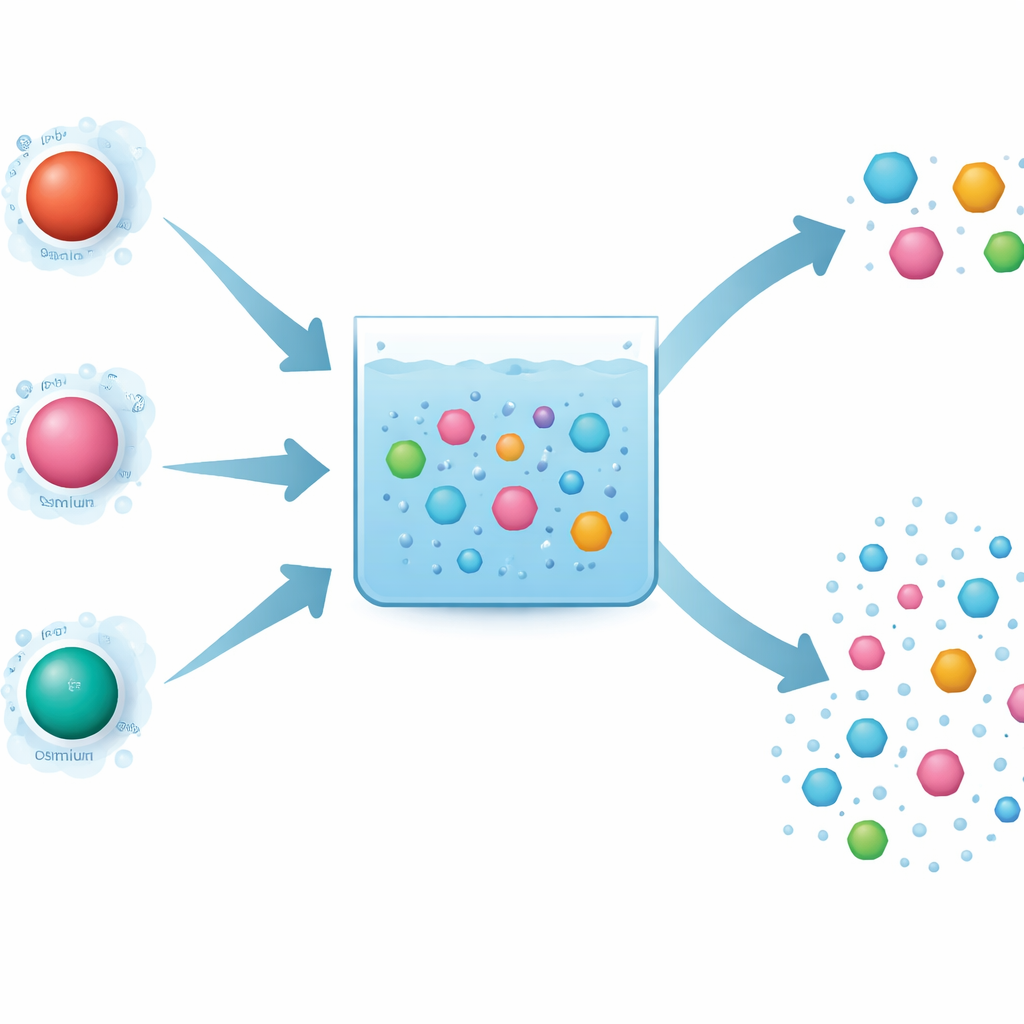
Perché la scelta del metallo conta nella degradazione degli inquinanti
I processi di ossidazione avanzata impiegano specie reattive potenti per spezzare le molecole organiche. Il periodato è uno di questi ossidanti e può essere «attivato» da ioni metallici disciolti. Gli autori hanno confrontato tre metalli strettamente correlati — ferro, rutenio e osmio — che appartengono alla stessa colonna della tavola periodica e che ci si potrebbe aspettare si comportino in modo simile. Tutti e tre possono attivare il periodato e contribuire a distruggere un inquinante di prova, il carbamazepina. Tuttavia, gli esperimenti hanno mostrato differenze sorprendenti: il rutenio agiva estremamente velocemente, il ferro era più lento e l'osmio si trovava in mezzo. Ancora più curioso, l'osmio rimuoveva una vasta gamma di inquinanti con poca preferenza, mentre ferro e rutenio erano selettivi, attaccando alcuni composti molto più facilmente di altri.
Due percorsi chimici molto diversi
Per scoprire cosa stava dietro a queste differenze, il team ha monitorato quali specie ossidanti a vita breve apparivano in ciascun sistema metallo–periodato. Con ferro e rutenio, i protagonisti predominanti erano unità «metallo–ossigeno» che si comportano come strumenti di precisione, trasferendo un atomo di ossigeno direttamente su siti specifici di un inquinante. Questi percorsi tendevano a formare prodotti epossidici — strutture ad anello che aggiungono un singolo atomo di ossigeno — indicando che la reazione è piuttosto selettiva. Nel sistema con osmio, invece, gli attori principali erano i radicali idrossilici, frammenti estremamente reattivi che attaccano quasi qualsiasi molecola organica vicina, portando a prodotti idrossilati e piccoli frammenti con anelli aperti. Test con sonde chimiche e spettroscopia di intrappolamento di spin hanno confermato che sono i radicali idrossilici e le specie reattive dell'ossigeno correlate, e non unità ossigeno–osmio ad alto stato di ossidazione, a guidare la maggior parte della distruzione degli inquinanti in presenza di osmio.
Come le condizioni dell'acqua modellano le reazioni
Il gruppo ha anche esaminato come il pH e i componenti naturali dell'acqua influenzino questi processi. Per l'osmio, la rimozione degli inquinanti aumentava con l'alcalinità dell'acqua, dove la coordinazione di ioni idrossido aggiuntivi attorno al metallo facilita il movimento degli elettroni e la formazione di radicali. A dosi elevate di metallo o ossidante, tuttavia, il sistema con osmio si «autointerrompeva» perché i radicali appena formati venivano consumati da eccesso di reagenti anziché dagli inquinanti. La materia organica naturale, che spesso interferisce con le reazioni di ossidazione, ha avuto sorprendentemente poco impatto sulla degradazione indotta dall'osmio, suggerendo che il percorso radicalico rimane robusto in acque realistiche. Al contrario, ferro e rutenio funzionavano meglio in condizioni acide, e la materia organica naturale sopprimeva fortemente la loro attività assorbendo gli ossidanti chiave metallo–ossigeno.
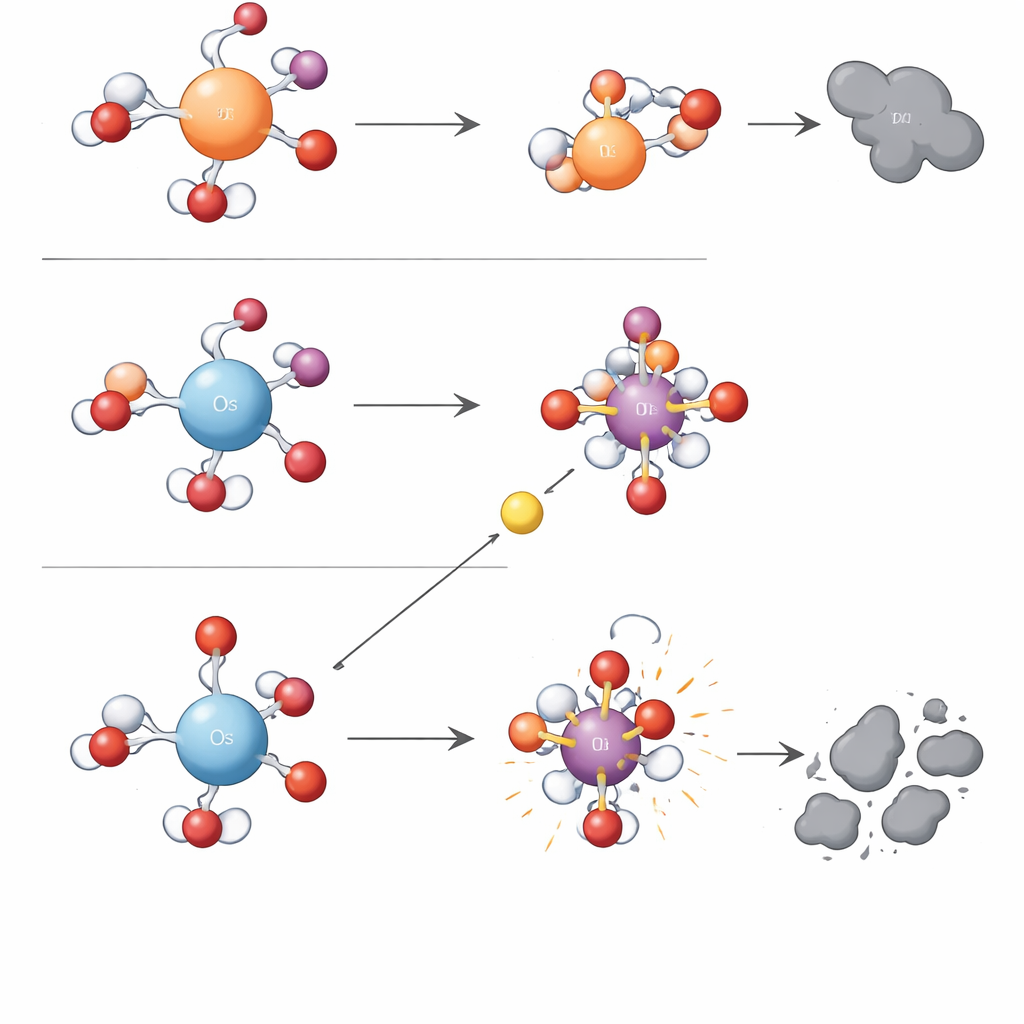
Una regola semplice della carica dietro una chimica complessa
Per andare oltre il metodo empirico, i ricercatori si sono rivolti a calcoli quantistico‑chimici. Hanno scoperto che una singola caratteristica elettronica — la densità di carica positiva del centro metallico idratato — poteva spiegare la separazione tra i due tipi di reazione. L'osmio in acqua porta una densità di carica positiva più concentrata rispetto a ferro o rutenio. Questo centro positivo forte trattiene saldamente il suo atomo di ossigeno legato, rendendo la sua unità metallo–ossigeno stabile ma lenta nel trasferimento diretto di ossigeno. Allo stesso tempo, l'attrazione intensa sull'acqua e sugli ioni vicini abbassa la barriera energetica per passaggi a singolo elettrone che alla fine rompono un legame dell'ossigeno nel periodato e rilasciano radicali idrossilici. I metalli con densità di carica inferiore, come ferro e rutenio, tengono gli elettroni in modo più saldo, favorendo la formazione e l'uso degli ossidanti selettivi metallo–ossigeno invece dei radicali liberi. Gli autori chiamano questa idea organizzativa il «Meccanismo di Controllo della Densità di Carica» e mostrano che razionalizza anche le tendenze riportate per altri metalli come il manganese.
Progettare trattamenti idrici migliori partendo da una sola manopola
Collegando un insieme complesso di osservazioni a un semplice descrittore — la densità di carica di un metallo circondato dall'acqua — questo lavoro offre una roadmap per personalizzare i processi di ossidazione avanzata. I metalli ad alta densità di carica dovrebbero favorire la degradazione ampia e basata su radicali di miscele complesse di inquinanti, specialmente in acque alcaline o ricche di materia organica. I metalli a bassa densità di carica sono più adatti quando è desiderata un'ossidazione selettiva e più delicata, per esempio per trasformare contaminanti specifici senza reagire eccessivamente con tutto il resto presente. In termini pratici, ciò significa che chimici e ingegneri possono selezionare o progettare catalizzatori per la purificazione dell'acqua regolando quanto saldamente i centri metallici trattengono la carica nel loro ambiente acquoso, invece di ottimizzare ogni sistema solo tramite tentativi ed errori.
Citazione: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Parole chiave: processi di ossidazione avanzata, attivazione del periodato, trattamento delle acque, catalisi da metalli di transizione, radicali idrossilici