Clear Sky Science · it
Workflow di proteomica chimica ad alto rendimento per mappare la dinamica della citrullinazione delle proteine
Perché cambiare i mattoni delle proteine conta
Le nostre cellule regolano costantemente il comportamento delle proteine aggiungendo piccole modifiche chimiche dopo la loro sintesi. Una di queste modifiche, chiamata citrullinazione, altera sottilmente la carica di un amminoacido comune e può rimodellare il modo in cui le proteine si ripiegano, si legano al DNA o interagiscono con altre molecole. Questi piccoli interventi sono sempre più associati a malattie autoimmuni, infezioni, cancro e funzione cerebrale, ma sono notoriamente difficili da rilevare. Questo studio presenta un workflow di laboratorio ad alto rendimento che finalmente rende possibile mappare la citrullinazione su migliaia di proteine, rivelando quando e dove compare nei tessuti e nelle cellule immunitarie.
Un interruttore nascosto sulle proteine
La citrullinazione avviene quando enzimi chiamati PAD modificano chimicamente l’amminoacido arginina, rimuovendone la carica positiva. Questo piccolo cambiamento può allentare l’impaccamento del DNA, modificare la rigidità delle proteine strutturali o alterare il modo in cui il sistema immunitario riconosce i tessuti propri. Una citrullinazione anomala è stata implicata in artrite reumatoide, disturbi neurodegenerativi, infezioni virali e cancro. Eppure le proteine citrullinate sono rare e facilmente confuse con altre modifiche più comuni, quindi i metodi standard di spettrometria di massa spesso non le rilevano. Il risultato è che i ricercatori hanno avuto solo una visione frammentata del “citrullinoma” corporeo—l’insieme completo delle proteine citrullinate.
Una strategia in due fasi: etichetta e cattura
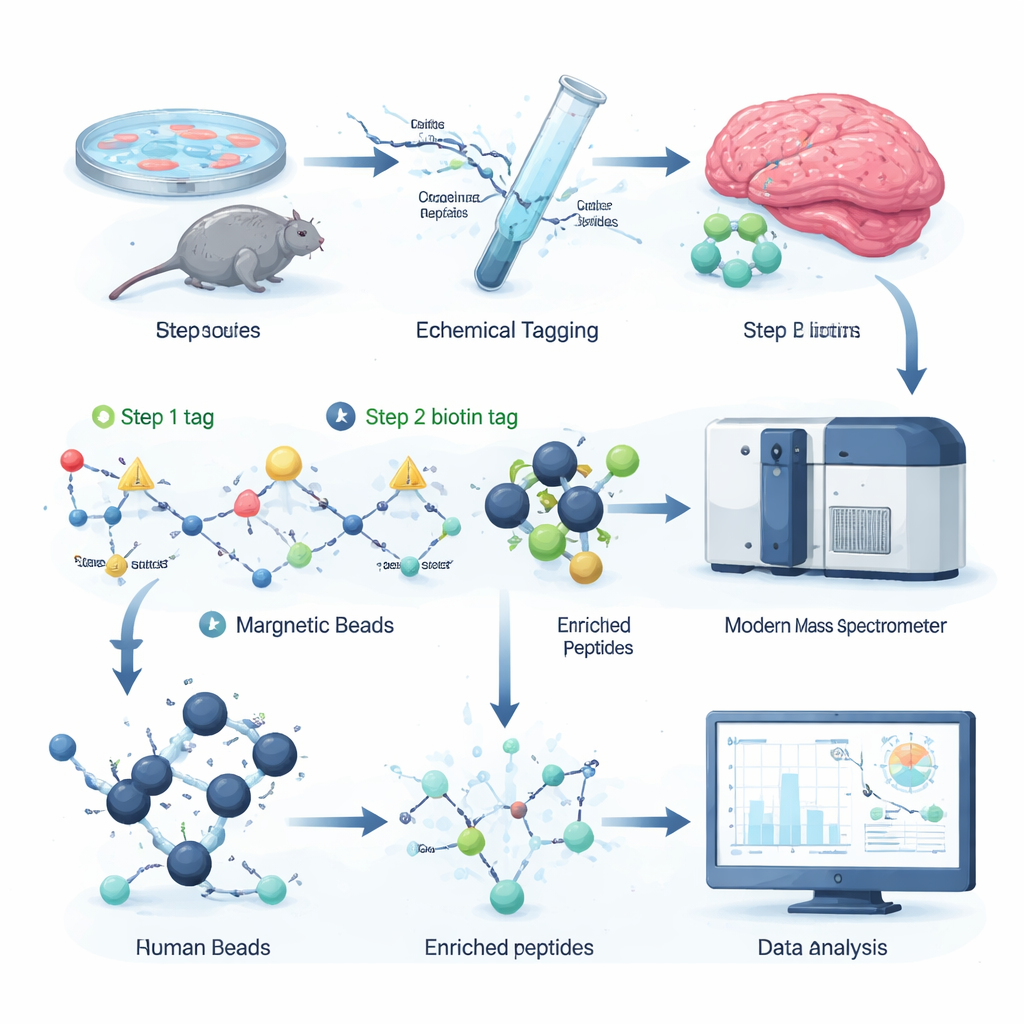
Gli autori hanno ideato una strategia di marcatura chimica che attacca selettivamente una “maniglia” rimovibile ai siti citrullinati sui peptidi, i frammenti di proteine analizzati dalla spettrometria di massa. Nella prima fase, una piccola molecola reattiva riconosce la citrullina e installa un piccolo tag. Nella seconda, viene collegato tramite click un più grande tag biotinico, che permette di prelevare i peptidi marcati da una miscela complessa usando sfere di streptavidina, uno strumento biochimico comune. Un trattamento chimico delicato poi asporta la parte ingombrante del tag, lasciando un piccolo e ben definito scostamento di massa che lo spettrometro può rilevare facilmente. Poiché tutti i reagenti sono disponibili in commercio e l’intero protocollo si adatta a piastre da 96 pozzetti, il workflow è rapido, scalabile e compatibile con gli allestimenti proteomici esistenti.
Vedere di più del citrullinoma
Incastrando peptidi citrullinati noti negli estratti cellulari e diluendoli in modo sistematico, il gruppo ha mostrato che la loro strategia di arricchimento aumenta il segnale dei peptidi citrullinati di oltre dieci volte, anche quando rappresentano meno di uno su mille molecole. In campioni complessi, il numero di siti citrullinati rilevati e le loro intensità misurate sono aumentati drasticamente dopo l’arricchimento. Applicando il metodo al tessuto cerebrale di topo sono stati scoperti due‑tre volte più siti di citrullinazione distinti rispetto a un precedente approccio all’avanguardia, inclusi molti sulla proteina basica della mielina, che isola le fibre nervose, e su proteine coinvolte nella comunicazione sinaptica. Ciò suggerisce che la citrullinazione possa influenzare sia il modo in cui le cellule nervose segnalano sia il mantenimento dell’architettura cerebrale.
Cellule immunitarie che gettano reti proteiche appiccicose
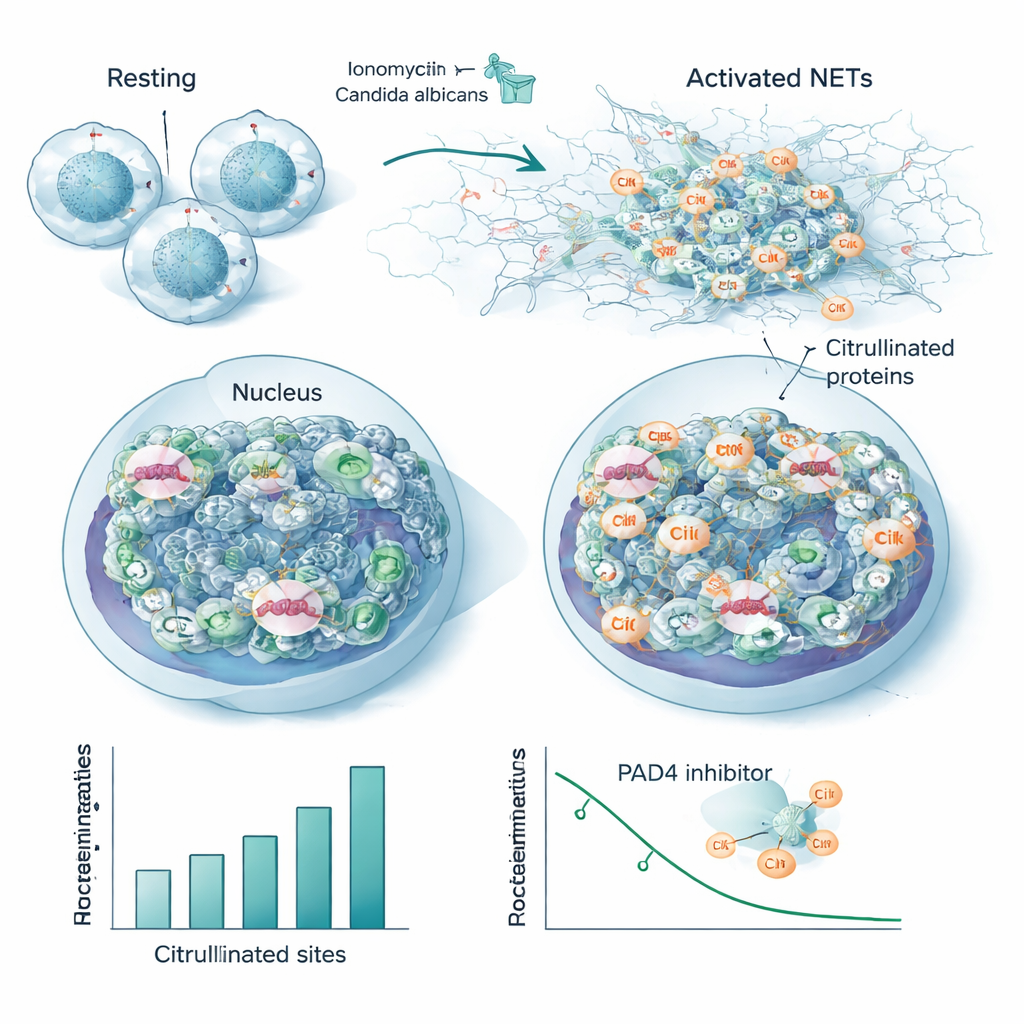
I neutrofili, un tipo di globulo bianco di prima linea, possono combattere gli invasori rilasciando reti appiccicose di DNA e proteine chiamate trappole extracellulari dei neutrofili, o NET. La formazione delle NET dipende da PAD4, un enzima citrullinante che allenta la cromatina permettendo al DNA di fuoriuscire. Usando il loro nuovo workflow, i ricercatori hanno seguito come la citrullinazione cambiava in neutrofili umani esposti a dosi crescenti di un attivatore chimico. Hanno rilevato fino a 1.700 frammenti peptidici citrullinati distribuiti su 580 proteine, con centinaia di siti che aumentavano o diminuivano in modo dose‑dipendente mentre i livelli proteici complessivi restavano costanti. Le istoni—le proteine che impacchettano il DNA—mostravano citrullinazione diffusa, non solo in pochi siti classici, e le varianti dell’istone linker H1 erano particolarmente modificate. Proteine strutturali come regolatori dell’actina e la lamin B, che modella l’involucro nucleare, sono diventate anch’esse fortemente citrullinate, indicando un ammorbidimento coordinato sia della cromatina sia degli scheletri cellulari durante il rilascio delle NET.
Una firma centrale di citrullinazione nelle infezioni
Per imitare un’infezione reale, il team ha stimolato i neutrofili con Candida albicans uccisa dal calore, un patogeno fungino comune. Sebbene ciò abbia generato complessivamente meno siti modificati rispetto al forte attivatore chimico, la grandissima maggioranza delle proteine e delle posizioni citrullinate è risultata sovrapposta tra i due stimoli. Questa sovrapposizione definisce un “citrullinoma centrale” conservato associato alla formazione delle NET, comprendente molte proteine nucleari e del citoscheletro e diversi autoantigeni noti—proprio i bersagli degli anticorpi nelle malattie autoimmuni. Quando i ricercatori hanno aggiunto un farmaco inibitore di PAD4, molti di questi stessi siti hanno perso la citrullinazione in modo dose‑dipendente, collegandoli direttamente all’attività dell’enzima e suggerendo che potrebbero servire come letture sensibili dell’inibizione di PAD4.
Cosa significa per salute e malattia
Trasformando una modifica elusiva in un segnale misurabile, questo workflow rende possibile tracciare dove e quando la citrullinazione avviene nei tessuti, nelle risposte immunitarie e nei modelli di malattia. Per i non specialisti, il messaggio chiave è che la citrullinazione agisce come un sottile dimmer molecolare sulle proteine, e poter vedere i suoi schemi in alta definizione potrebbe aiutare a spiegare come iniziano le malattie autoimmuni, come le infezioni rimodellano le cellule immunitarie e come le proteine cerebrali cambiano nel tempo. La scalabilità del metodo e l’uso di apparecchiature di laboratorio standard ne facilitano l’adozione, aprendo la strada alla scoperta di nuovi target farmacologici, diagnostiche di precisione e a una comprensione più profonda di come piccole modifiche chimiche possono avere grandi conseguenze biologiche.
Citazione: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Parole chiave: citrullinazione, malattia autoimmune, trappole extracellulari dei neutrofili, spettrometria di massa, modifica post-traduzionale