Clear Sky Science · it
Significato patofisiologico della compromessa acetilazione dell'istone H3K14 dipendente da KAT7 durante la carenza di zinco
Perché i nutrienti microscopici contano per la nostra salute
Lo zinco è un metallo traccia di cui il nostro organismo ha bisogno in quantità minime, eppure sostiene silenziosamente centinaia di proteine che mantengono le cellule operative. Quando lo zinco scarseggia — per dieta, malattia o invecchiamento — è stato associato a problemi che vanno dalla crescita ritardata a un’immunità indebolita e alla steatosi epatica. Questo studio pone una domanda più profonda: come fanno le cellule a percepire che lo zinco sta diventando scarso e in che modo questa carenza viene tradotta in cambiamenti duraturi nell’attività genica e nella salute degli organi?
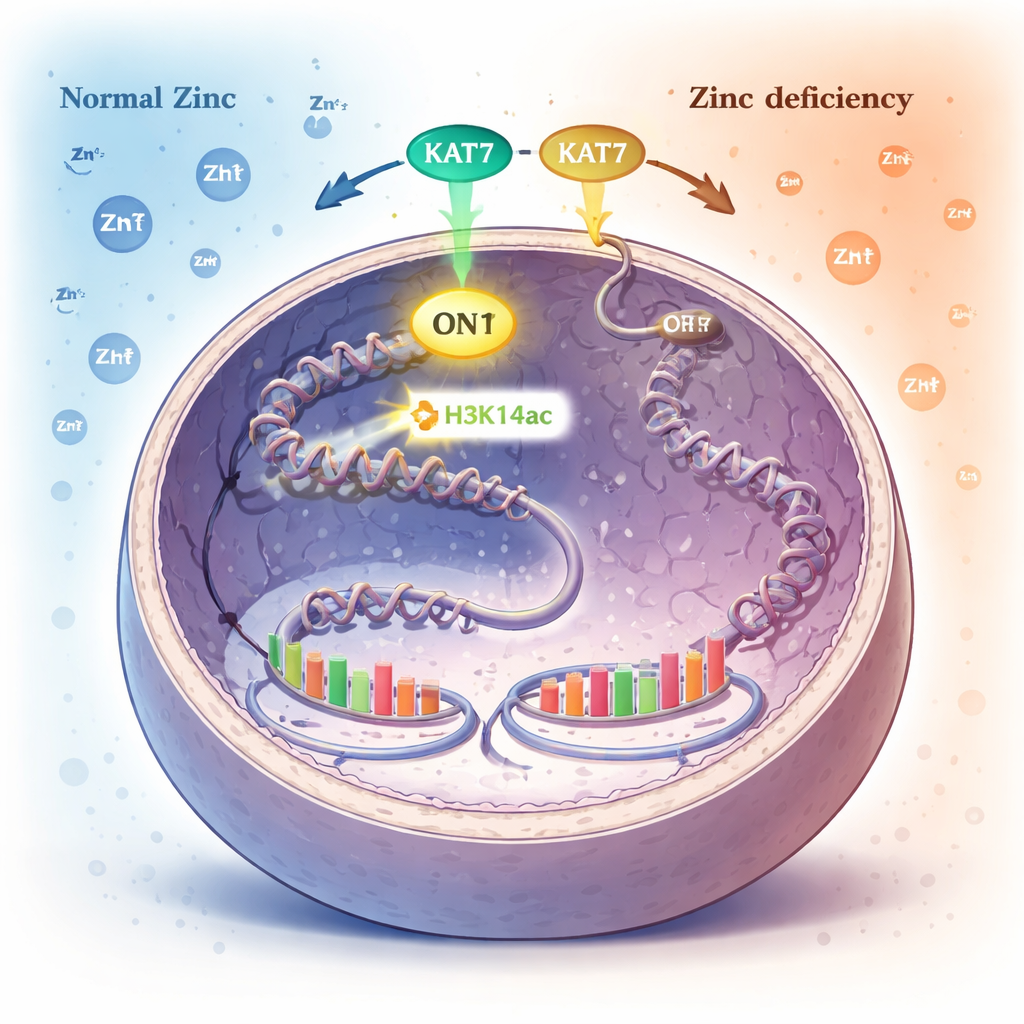
Un marcatore chimico sul confezionamento del DNA come allarme interno per lo zinco
Nel nucleo il DNA è avvolto attorno a spool proteici chiamati istoni. Le cellule controllano quali geni sono attivi aggiungendo o rimuovendo piccoli segni chimici su questi istoni. Uno di questi segni, l’acetilazione in un sito specifico sull’istone H3 (H3K14ac), è aggiunto da un enzima chiamato KAT7. Gli autori hanno scoperto che quando lo zinco diventa scarso, i livelli di questo marcatore H3K14ac cadono drasticamente, mentre molti altri marcatori istonici comuni rimangono invariati. Questo ha indicato H3K14ac, e l’enzima KAT7 che lo genera, come un sensore chiave dello stato dello zinco.
Come lo zinco mantiene attivo un enzima chiave
Disabilitando sistematicamente diversi enzimi, i ricercatori hanno mostrato che KAT7 è la principale fonte di H3K14ac nelle cellule umane. KAT7 contiene una piccola struttura che lega lo zinco all’interno del suo centro attivo. Quando le cellule sono state indotte in carenza di zinco, la capacità di KAT7 di aggiungere il marcatore H3K14ac è diminuita, nonostante la proteina rimanesse nel nucleo e continuasse ad associarsi ai suoi partner ausiliari. Test dettagliati con frammenti purificati di KAT7 hanno rivelato che lo zinco correttamente legato in questa regione è essenziale per la sua attività; perturbare il legame con lo zinco spegneva l’enzima e reintegrare con cura lo zinco ne ripristinava la funzione. In sostanza, KAT7 si comporta come un interruttore dipendente dallo zinco che controlla un marcatore istonico specifico.
Convertire la perdita di zinco in cambiamenti genici che ristabiliscono i livelli di zinco
Cosa provoca concretamente la perdita di questo marcatore istonico? Usando mappature su scala genomica, il gruppo ha mostrato che H3K14ac è particolarmente arricchito in regioni enhancers — porzioni regolatorie di DNA che modulano finemente i geni vicini. In condizioni di carenza di zinco, H3K14ac veniva rimossa da molti enhancers e, maggiore era la perdita, più intenso era il cambiamento nell’attività dei geni adiacenti. Un gene di spicco è stato ZIP10, che codifica per una proteina sulla superficie cellulare che importa zinco. Quando H3K14ac diminuiva sull’enhancer di ZIP10, i livelli di ZIP10 sulla membrana aumentavano, permettendo a più zinco di entrare nella cellula. Bloccare KAT7 o impedire la perdita di H3K14ac interferiva con questa risposta e riduceva l’assorbimento di zinco, anche dopo la reintroduzione dello zinco. Questo dimostra che le cellule convertono la scarsità di zinco in un segnale epigenetico che potenzia il macchinario di importazione dello zinco per ripristinare l’equilibrio.
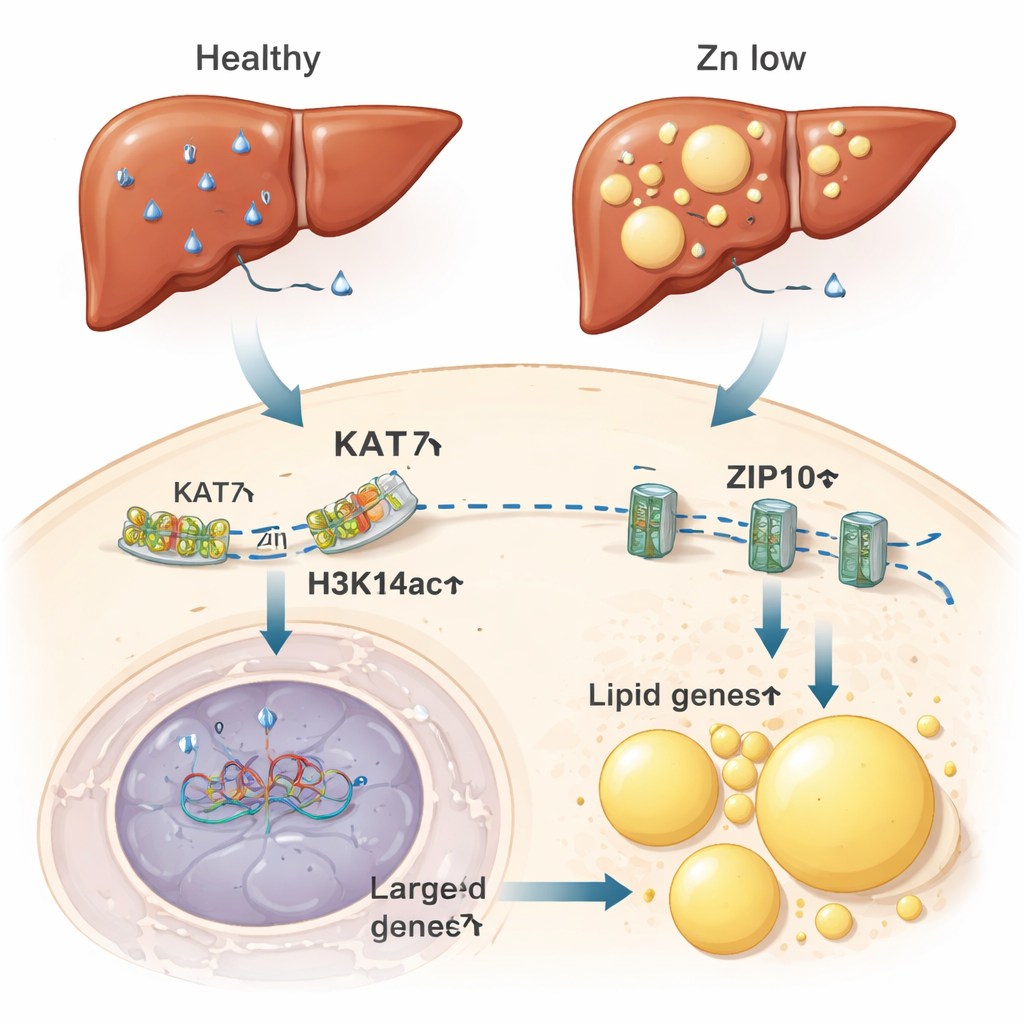
Dalle cellule affamate di zinco ai fegati grassi
I ricercatori si sono poi chiesti se questo interruttore sensibile allo zinco avesse conseguenze nell’animale intero. Nei topi nutriti con una dieta carente di zinco, il fegato — un hub centrale del metabolismo dello zinco e dei lipidi — mostrava livelli ridotti di zinco, minore H3K14ac e attività di KAT7 indebolita. Questi cambiamenti coesistevano con un’espressione aumentata di geni che guidano l’accumulo di grasso e la formazione di droplet lipidici, i microscopici pacchetti di grasso all’interno delle cellule. I fegati dei topi carenti di zinco accumulavano grasso in misura comparabile a quelli sottoposti a una dieta ricca di grassi. Notevolmente, ridurre semplicemente l’attività di KAT7 con un farmaco, anche senza cambiare lo zinco dietetico, era sufficiente a promuovere l’accumulo di grasso nelle cellule epatiche. Al contrario, somministrare zinco in più attenuava l’accumulo di grasso indotto da una dieta ricca di lipidi.
Cosa significa per il rischio di malattia nell’uomo
Mettendo i loro risultati in un contesto clinico, i ricercatori hanno riesaminato studi umani che misuravano i livelli di zinco nel tessuto epatico. In numerosi rapporti, le persone con fegato grasso e disturbi correlati avevano quantità di zinco nel fegato significativamente inferiori rispetto ai controlli sani. Insieme agli esperimenti sui topi, ciò suggerisce che una carenza cronica di zinco possa favorire la steatosi epatica silenziando KAT7, cancellando il marchio H3K14ac e aumentando in modo persistente l’espressione di geni che promuovono l’accumulo di grasso. In termini semplici, il lavoro rivela un circuito interno “zinco‑verso‑epigenetica”: quando lo zinco cala, un enzima dipendente dallo zinco perde potenza, alterando il confezionamento del DNA in modi che inizialmente aiutano le cellule a importare più zinco, ma che nel tempo possono anche spingere il fegato verso un accumulo di grasso dannoso.
Citazione: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
Parole chiave: carenza di zinco, epigenetica, fegato grasso, acetilazione degli istoni, trasportatori di zinco