Clear Sky Science · it
Approfondimenti meccanicistici nella termodinamica fuori equilibrio della fissazione dell'azoto tramite cavitazione acustica
Trasformare l'aria in fertilizzante utile con il suono
L'azoto presente nell'aria è essenziale per i fertilizzanti e la produzione alimentare, ma convertire questo gas ostinato in forme utili solitamente richiede impianti giganteschi, temperature estreme e alte pressioni. Questo studio esplora un approccio molto diverso: usare onde sonore intense per generare minuscole bolle esplosive nell'acqua che possono "fissare" l'azoto in condizioni lontane dall'equilibrio. Osservando e modellando ciò che avviene all'interno di questi punti caldi effimeri, i ricercatori mostrano come le bolle guidate dal suono potrebbero offrire una nuova via per produrre composti azotati senza catalizzatori tradizionali o reattori enormi.
Perché fissare l'azoto è così difficile
La nostra atmosfera è per lo più azoto molecolare, ma i suoi atomi sono legati da uno dei legami chimici più forti in natura. Rompere quel legame in modo efficiente è il motivo per cui il processo Haber–Bosch si affida a macchinari potenti e consuma grandi quantità di energia a livello globale. I metodi convenzionali devono trovare un equilibrio difficile: temperature abbastanza alte da attivare l'azoto, ma non così elevate da degradare i prodotti desiderati o spostare l'equilibrio a sfavore della reazione. Questo articolo sostiene che, invece di mantenere una temperatura costante, può essere più efficace sforare brevemente—usando esplosioni ultrarapide di calore—e poi raffreddare così rapidamente che i prodotti utili vengono intrappolati prima di decomporsi.
Usare gli ultrasuoni per creare minuscole camere di reazione
Quando ultrasuoni potenti attraversano l'acqua, generano bolle di gas microscopiche che crescono e poi collassano violentemente, un fenomeno noto come cavitazione acustica. Ogni bolla collassante si comporta come un reattore in miniatura e di breve durata. In frazioni di miliardesimi di secondo, il gas all'interno viene compresso a temperature superiori a 5000 kelvin per poi raffreddarsi nuovamente a tassi prossimi a 1012 kelvin al secondo. In queste condizioni, le molecole di azoto nella bolla possono scindersi in frammenti reattivi, che poi si combinano con frammenti derivati da ossigeno, idrogeno o acqua per formare nitrito, nitrato o ammonio. I nuovi prodotti vengono quindi proiettati nel liquido circostante, dove si accumulano nel tempo mentre si forma e collassa la generazione successiva di bolle. 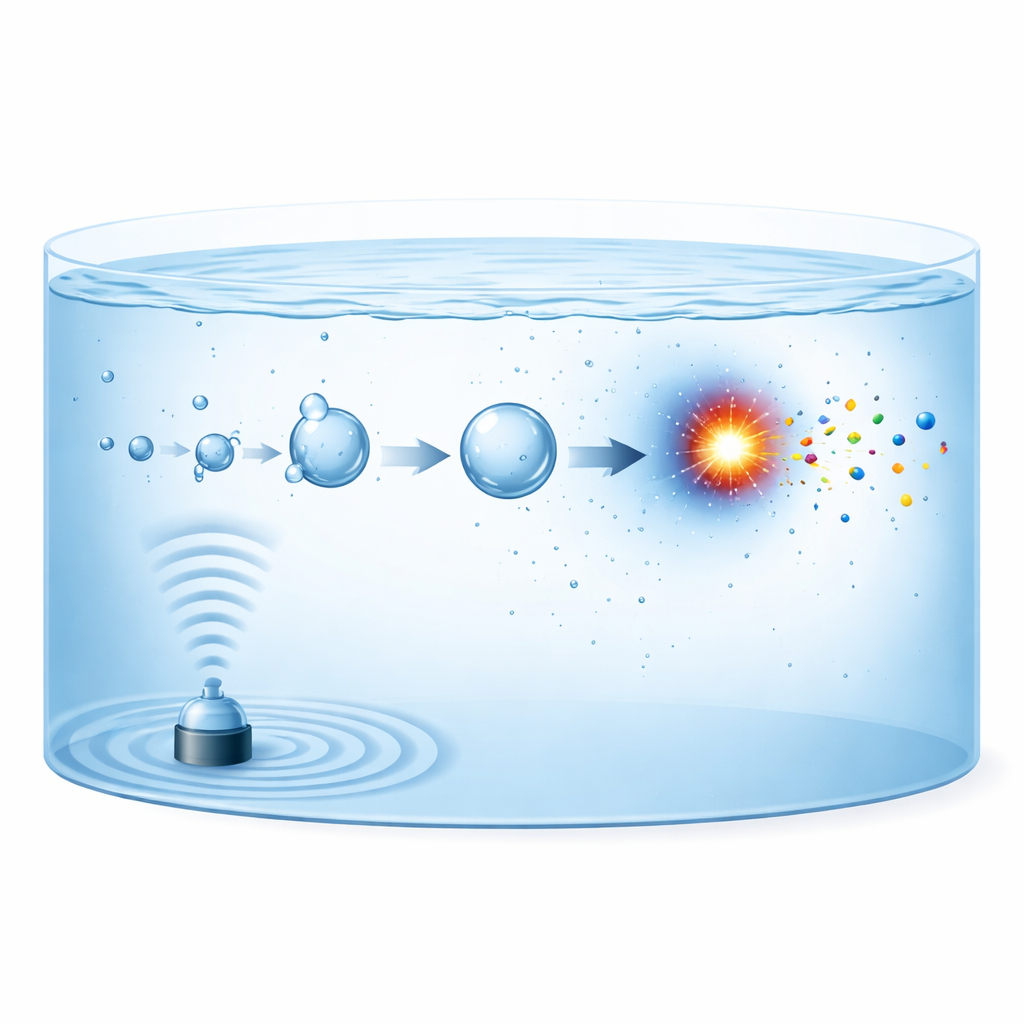
Regolare le bolle per scegliere tra diversi prodotti
Il team ha variato sistematicamente i gas che alimentano le bolle (azoto più ossigeno o idrogeno), la potenza e la frequenza degli ultrasuoni e la presenza di particelle solide che favoriscono la formazione delle bolle. Con miscele azoto–ossigeno, il sistema produceva principalmente prodotti ossidati come nitrito e nitrato; con miscele azoto–idrogeno, prevaleva l'ammonio. Piccole quantità di particelle di talco hanno agito come "semi" per le bolle, abbassando la soglia per la cavitazione e rendendo le reazioni più riproducibili. Modificando la pressione sonora e il tempo di reazione, i ricercatori sono riusciti a spostare l'equilibrio tra nitrito e nitrato, dimostrando che parte della chimica avviene all'interno della bolla in collasso e parte continua nel liquido circostante mentre i frammenti reattivi convertono lentamente il nitrito in nitrato più ossidato.
Scrutare l'impulso termico su scala nanometrica
Per comprendere perché condizioni così estreme e fugaci producono comunque prodotti stabili, gli autori hanno combinato misure sperimentali con simulazioni dettagliate e calcoli di chimica quantistica. Questi mostrano che, a temperature molto elevate, l'azoto può scindersi direttamente nella fase gassosa, aprendo percorsi normalmente inaccessibili. Ma gli stessi calcoli rivelano anche che mantenere il gas caldo renderebbe instabili i prodotti finali. La chiave è il raffreddamento rapido: il picco di temperatura della bolla attiva l'azoto, quindi il raffreddamento quasi istantaneo stabilizza frammenti intermedi e molecole finite come l'ammoniaca e l'acido nitroso prima che possano degradarsi o ritornare ad azoto. La modellizzazione di singole bolle, specialmente quando drogate con argon che aumenta le temperature di collasso, ha confermato che temperature massime più alte spostano la miscela di prodotti e aumentano i tassi complessivi di fissazione. 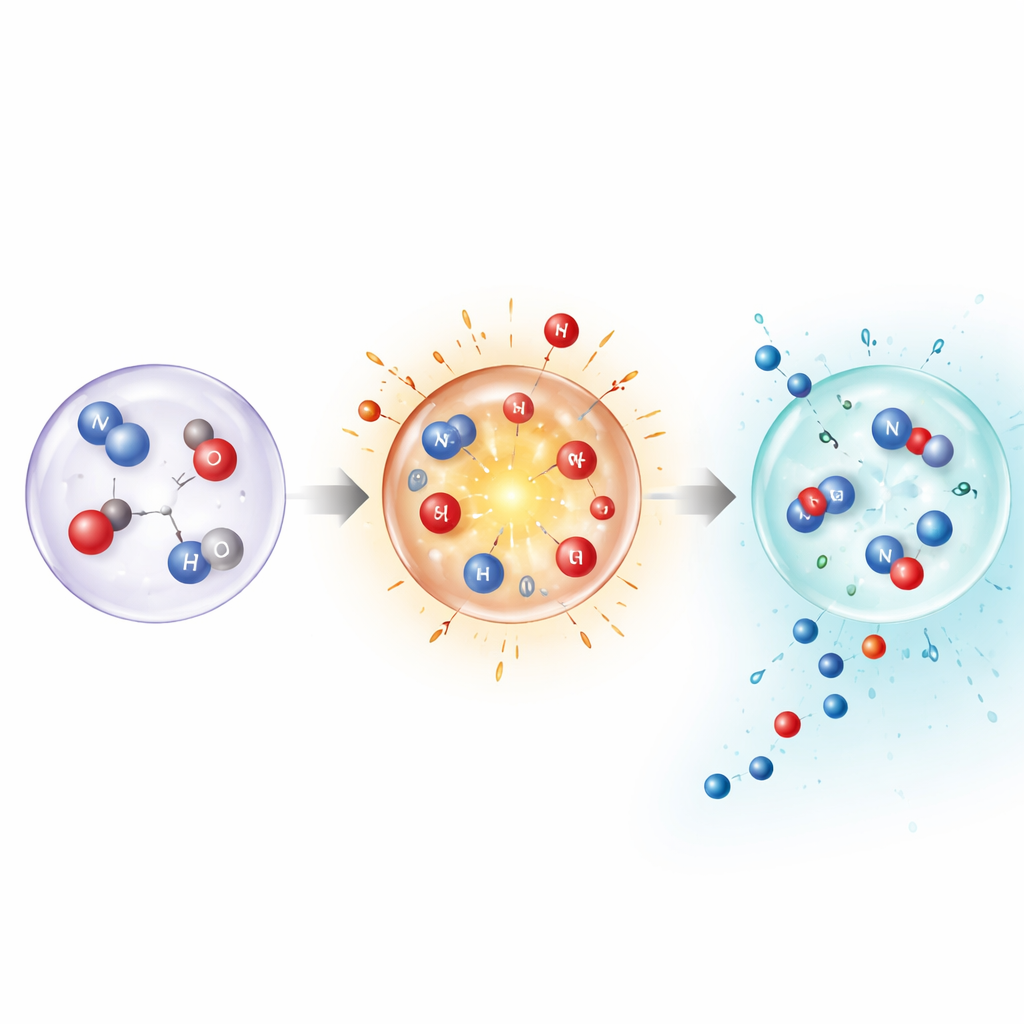
Uso energetico e possibilità future
Pur non essendo ancora efficiente quanto i migliori processi industriali, questo metodo guidato dal suono mostra prestazioni già paragonabili agli storici approcci ad arco elettrico e ad alcuni moderni sistemi a plasma, il tutto operando in condizioni ambientali complessive e senza catalizzatori solidi. È importante notare che gli stessi eventi di cavitazione scindono anche l'acqua, liberando idrogeno, ossigeno e perossido di idrogeno—sottoprodotti ricchi di energia che potrebbero essere recuperati insieme all'azoto fissato. Gli autori sottolineano che il loro allestimento è pensato per rivelare i meccanismi più che per massimizzare la resa, ma il lavoro stabilisce la cavitazione acustica come una via distinta per fissare l'azoto sfruttando cicli termici estremamente rapidi in bolle microscopiche. Per i non specialisti, la conclusione è che suono controllato con cura può trasformare acqua e aria ordinarie in ingredienti per fertilizzanti attraverso una sequenza di piccole esplosioni invisibili, suggerendo rotte più verdi e flessibili per produrre in futuro i vitali composti azotati.
Citazione: Pan, X., Preso, D.B., Liu, Q. et al. Mechanistic insights into the non-equilibrium thermodynamics of nitrogen fixation via acoustic cavitation. Nat Commun 17, 2682 (2026). https://doi.org/10.1038/s41467-026-69466-1
Parole chiave: fissazione dell'azoto, cavitazione acustica, sonochimica, produzione di fertilizzanti, chimica a ultrasuoni