Clear Sky Science · it
Tripla modulazione di STING, TGF-β e PD-L1 potenzia il segnale CXCL16–CXCR6 per una forte risposta antitumorale
Riscaldare i tumori “freddi”
L’immunoterapia oncologica ha trasformato il trattamento per alcuni pazienti, ma molti tumori continuano a non rispondere a questi farmaci potenti. Questo studio indaga perché certi tumori resistono agli attuali farmaci immunitari di tipo “checkpoint” e propone un attacco più intelligente, a tre punte, che riattiva le difese dell’organismo, richiama cellule T assassine di élite e le mantiene attive direttamente all’interno del tumore.
Perché i farmaci immunitari attuali non sono sufficienti
La maggior parte delle immunoterapie approvate mira a un singolo freno sulle cellule immunitarie, come la via PD-1/PD-L1. Una classe più recente di farmaci prova ad andare oltre bloccando anche il TGF-β, una molecola che sopprime fortemente l’immunità nei tumori avanzati. Un farmaco di questo tipo, YM101, combina il blocco di TGF-β e PD-L1 in un unico anticorpo e ha mostrato efficacia nei topi. Ma anche in animali geneticamente identici, alcuni tumori si riducevano a malapena. Confrontando tumori responsivi e resistenti, i ricercatori hanno trovato che il successo del trattamento andava di pari passo con una forte attivazione immunitaria “innata”, in particolare il signaling attraverso una via chiamata STING, che rileva DNA anomalo e innesca segnali di allarme simili a quelli antivirali.
Aggiungere una terza leva: la via STING
Sospettando che una debole attivazione innata fosse il tassello mancante, il gruppo ha combinato YM101 con un agonista di STING in forma di pillola chiamato MSA-2 in diversi modelli tumorali murini, inclusi tumori “freddi” difficili da trattare. L’approccio triplo — attivazione di STING più blocco di TGF-β e PD-L1 — ha ridotto i tumori in modo più efficace, esteso la sopravvivenza e spesso ha protetto i topi dalla ricomparsa del tumore dopo una nuova sfida, indicando memoria immunitaria duratura. Questo ha superato l’abbinamento più convenzionale di un agonista STING con il blocco di PD-L1 da solo, e ha anche potenziato la terapia con agonista STING quando veniva bloccato solo il TGF-β, rivelando che il TGF-β agisce come un importante freno sull’immunità mediata da STING. 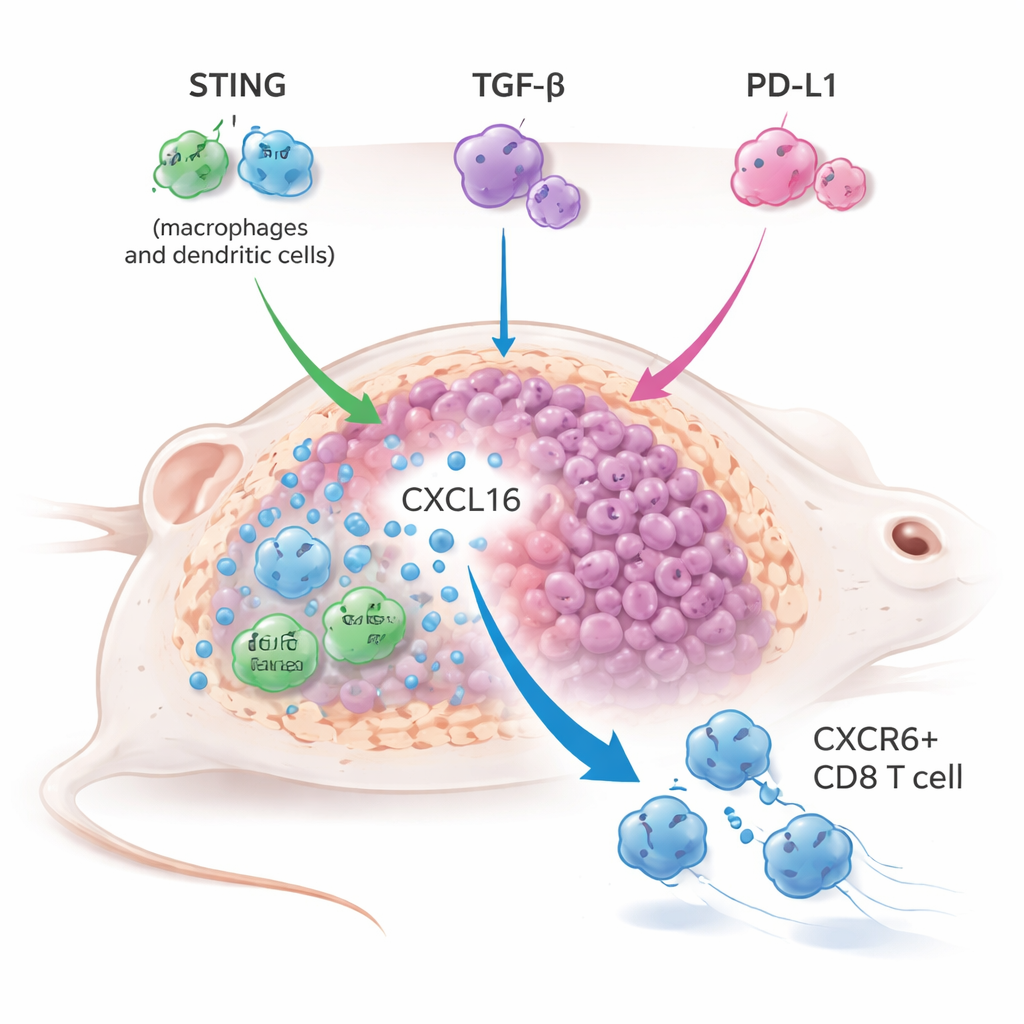
Reclutare una squadra specialistica di killer
Per capire come funzionasse questa strategia tripla, i ricercatori hanno usato sequenziamento dell’RNA a singola cellula e un dettagliato profiling immunitario dei tumori trattati. Hanno scoperto una marcata espansione di un sottogruppo di cellule T citotossiche caratterizzato dal recettore CXCR6. Queste cellule CD8+ CXCR6+ erano altamente armate, esprimendo alti livelli di granzimi, perforina e molecole infiammatorie, e mostravano forti segni di attivazione e proliferazione. Allo stesso tempo, macrofagi associati al tumore e cellule dendritiche aumentarono la produzione di una chemochina chiamata CXCL16, che si lega a CXCR6 e aiuta a trattenere queste cellule T nel tumore. Quando il legame CXCL16–CXCR6 veniva interrotto — o bloccando CXCL16 o eliminando geneticamente CXCR6 nelle cellule T — il trattamento combinato perdeva in gran parte la sua efficacia antitumorale, dimostrando che questo asse è centrale per il successo della terapia.
Come viene attivata la cascata del segnale
Approfondendo, il team ha chiesto come l’attivazione di STING e il blocco di TGF-β aumentino congiuntamente CXCL16. In cellule immunitarie umane e murine, gli agonisti di STING aumentavano fortemente CXCL16 e la citochina antivirale IFN‑β, mentre l’aggiunta di TGF-β riduceva nettamente entrambe. I ricercatori hanno mostrato che STING innesca il signaling IFN‑I, che attiva il fattore di trascrizione STAT1; STAT1 poi si lega direttamente alla regione di controllo del gene CXCL16, attivandone l’espressione. Il TGF-β interrompe questa catena interferendo con un passaggio chiave nel signaling di STING, probabilmente tramite una proteina chiamata HDAC4 e specie reattive dell’ossigeno, attenuando l’attivazione di IRF3 e la produzione a valle di IFN‑β e CXCL16. Bloccare il TGF-β rimuove questo freno, permettendo agli agonisti STING di accendere pienamente la via STAT1–CXCL16 nelle cellule mieloidi e così fornire alle cellule T CXCR6+ i segnali necessari per restare e combattere nel tumore.
Costruire un farmaco di precisione unico
Per rendere questo complesso regime più pratico e mirato al tumore, i ricercatori hanno ingegnerizzato un singolo «conjugato anticorpo‑stimolante immunitario» chiamato Y101S. Questa molecola combina l’anticorpo bifunzionale che blocca TGF-β/PD-L1 con un agonista STING legato tramite un linker clivabile. Y101S si indirizza alle cellule mieloidi positive per PD-L1 nel tumore, viene internalizzato e quindi rilascia il farmaco STING all’interno di queste cellule. In diversi tumori murini, Y101S ha eguagliato o superato l’efficacia di somministrare YM101 più un agonista STING libero ad alto dosaggio, nonostante contenesse solo una piccolissima frazione di quella dose di STING. Ha aumentato macrofagi e cellule dendritiche CXCL16+, espanso le cellule CD8+ CXCR6+, indotto memoria immunitaria durevole e concentrato i segnali infiammatori nei tumori risparmiando gli organi sani, con un profilo di sicurezza favorevole nei topi. 
Cosa significa per il futuro del trattamento del cancro
Per i non specialisti, il messaggio chiave è che attaccare il cancro con uno o due interruttori immunitari potrebbe non essere sufficiente — specialmente quando i tumori silenziano attivamente i sistemi di allarme precoci. Questo lavoro mostra che combinare l’attivazione di STING con il blocco di TGF-β e PD-L1 può rimodellare l’ambiente tumorale, attirare e sostenere in modo potente un gruppo specializzato di cellule T citotossiche e ottenere risposte più profonde e durature nei modelli preclinici. L’anticorpo‑farmaco a tripla azione Y101S incarna questa strategia in un unico medicinale mirato e offre una road map per le prossime generazioni di immunoterapie rivolte ai tumori che attualmente resistono agli anticorpi checkpoint standard.
Citazione: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Parole chiave: immunoterapia oncologica, via STING, blocco del TGF-beta, anticorpo anti–PD-L1, CXCL16 CXCR6 cellule T