Clear Sky Science · it
Cooperatività positiva tra i domini leganti RAS e ricchi di cisteina regola la cinetica del legame di RAF alla membrana tramite ri-legame laterale
Perché questa piccola danza molecolare è importante
All’interno delle nostre cellule, decisioni di vita o morte riguardo crescita, divisione e sopravvivenza vengono spesso prese sulla superficie della membrana cellulare. Un protagonista chiave in queste decisioni è una proteina chiamata RAF, che aiuta a trasmettere segnali di crescita ed è frequentemente alterata nei tumori. Questo studio svela, con dettagli cinetici senza precedenti, come RAF si ancora alla membrana cellulare, quanto a lungo vi resta e perché ammassi densi di un’altra proteina, RAS, possono mantenere RAF attivo più a lungo del previsto.
Segnali che si incontrano sulla superficie cellulare
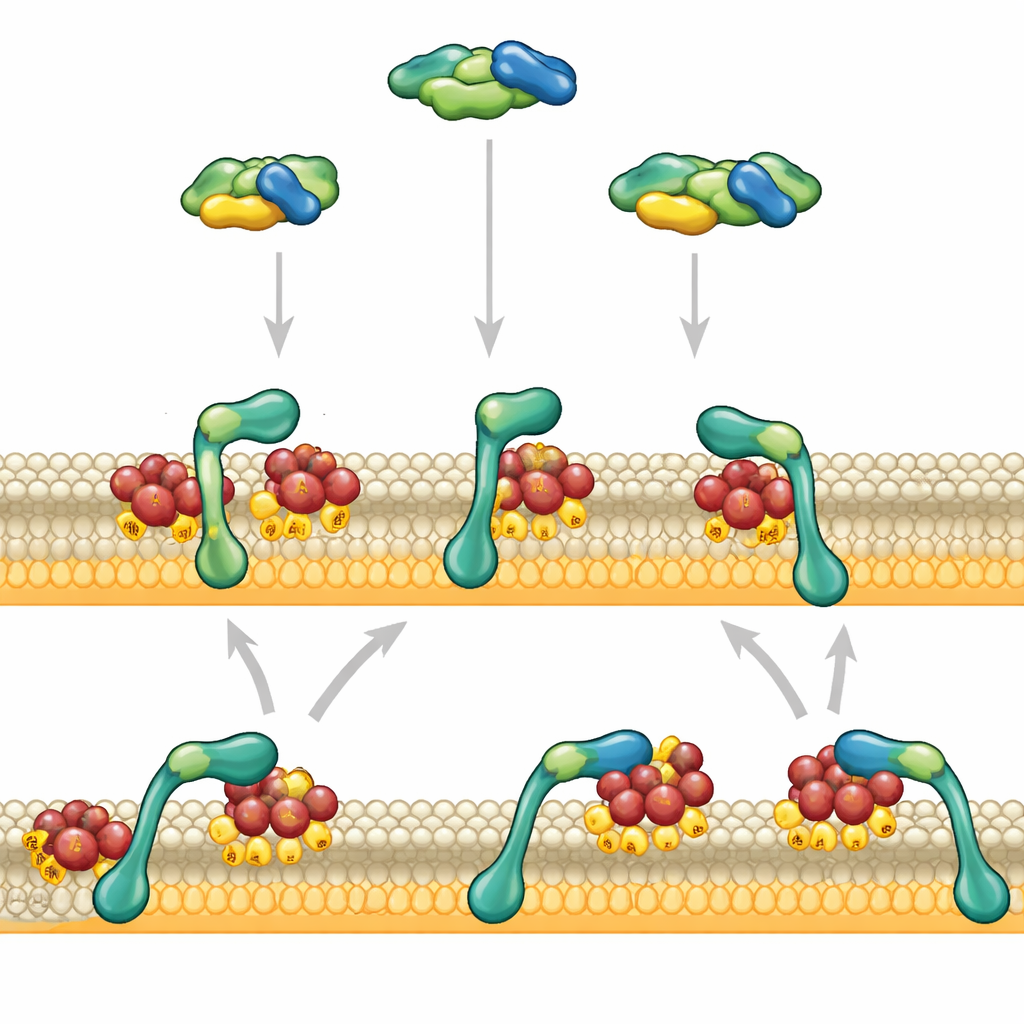
RAF opera in un’importante autostrada di segnalazione nota come via MAPK, che collega segnali esterni come i fattori di crescita a cambiamenti nell’attività genica. Nella sua forma di riposo, RAF galleggia nell’interno cellulare in una conformazione ripiegata e auto-inibita. Viene attivato solo quando incontra RAS, un piccolo interruttore molecolare ancorato alla faccia interna della membrana cellulare. RAS deve trovarsi nello stato “on” ed essere inserito nel giusto tipo di lipidi affinché RAF venga reclutato e attivato. Poiché le molecole di RAF sono relativamente scarse rispetto a molti altri componenti di segnalazione, il modo esatto in cui si legano alla membrana e evitano un distacco prematuro influenza fortemente se una cellula risponderà debolmente o in modo marcato a un segnale di crescita.
Due mani per afferrare la membrana
Gli autori si sono concentrati su due regioni sull’estremità frontale di RAF: una che afferra RAS e una che preferisce i lipidi della membrana carichi negativamente. Utilizzando membrane artificiali e proteine purificate, hanno osservato singoli frammenti di RAF legarsi a superfici decorate da RAS con microscopia avanzata. Quando la regione legante RAS agiva da sola, toccava brevemente la membrana e si staccava nell’ordine di circa un secondo. La regione che ama i lipidi, da sola, si attaccava a malapena. Ma quando queste due regioni erano collegate, il comportamento cambiava radicalmente: RAF si legava ora in modo forte e rimaneva sulla membrana per decine di secondi, specialmente quando la membrana conteneva molti lipidi caricati negativamente simili a quelli delle cellule reali.
Cooperazione che rallenta l’uscita
Questo cambiamento drammatico non derivava dal fatto che RAF trovasse la membrana più rapidamente, ma dal fatto che la lasciava più lentamente. Prima, il segmento legante RAS di RAF riconosce RAS attivato e ancora RAF alla membrana. Solo dopo questo primo saluto la regione legante i lipidi si impegna pienamente con i lipidi circostanti, rallentando il movimento laterale di RAF e ancorandolo più saldamente. Questo secondo contatto a sua volta stabilizza l’interazione originale RAS–RAF, creando un circuito di retroazione positiva tra contatti proteina–proteina e proteina–lipide. Esperimenti che modificavano il breve linker che connette le due regioni hanno mostrato che il loro stretto coordinamento spaziale è cruciale: rendere il linker più flessibile o più lungo indeboliva la capacità di RAF di restare sulla membrana.
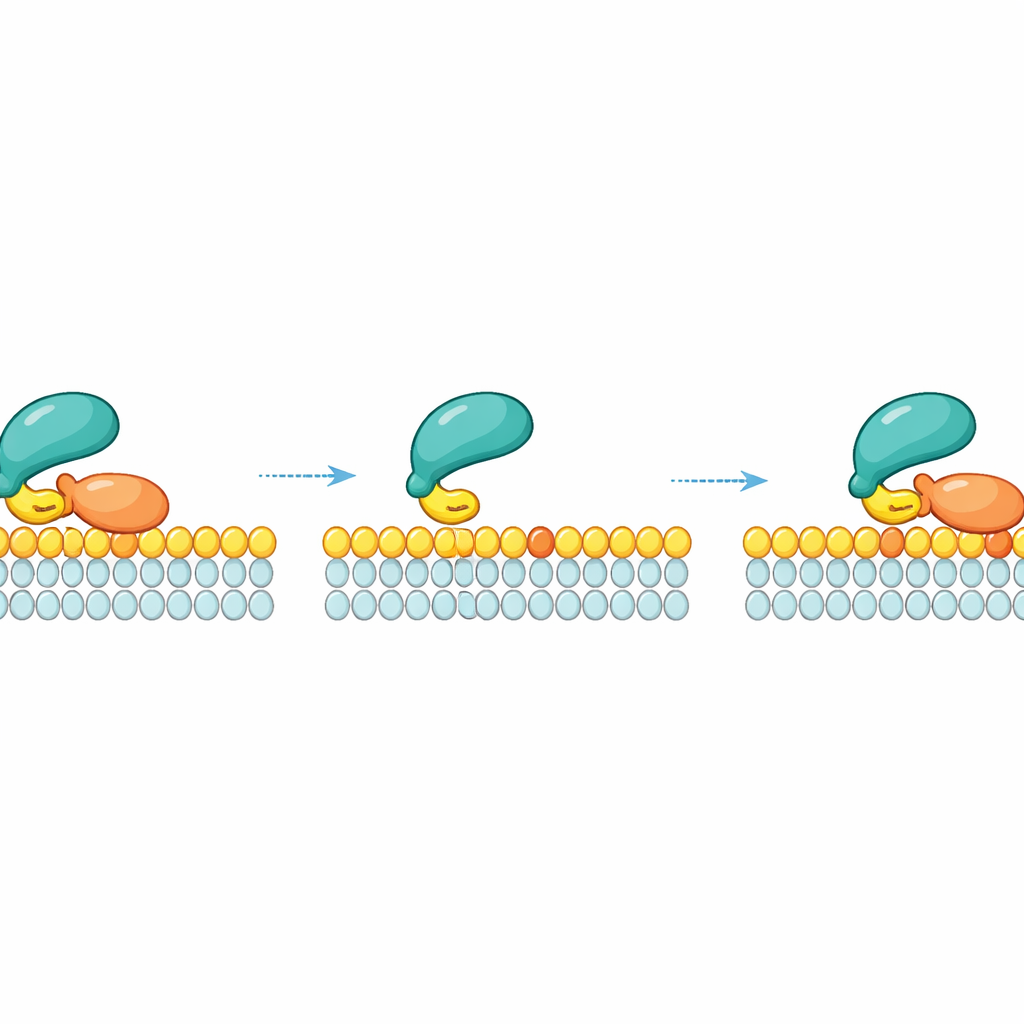
Ri-legame laterale: scorrere invece di cadere
Un’intuizione chiave del lavoro è che RAF non si stacca semplicemente nel fluido circostante una volta che lascia una particolare molecola di RAS. Invece, dopo il distacco da RAS, RAF può rimanere brevemente agganciato alla membrana tramite il suo debole contatto con i lipidi e scivolare lateralmente. In questo stato transitorio può “riafferrare” una molecola di RAS vicina nello stesso frammento di membrana. Questo ri-legame laterale crea una rete di sicurezza cinetica: ad alta densità locale di RAS—come nei nanoclustere dove le molecole di RAS sono strettamente impaccate—RAF ha molte possibilità di riattaccarsi a RAS prima di allontanarsi. Misurazioni e simulazioni hanno mostrato che più alta è la densità di RAS attivo sulla membrana, più a lungo RAF rimane legato alla membrana grazie a questi ripetuti riagganci locali.
Da visite prolungate ad attivazione affidabile
Il tempo esteso che RAF trascorre sulla membrana ha conseguenze importanti. L’attivazione di RAF non è un singolo evento ma una sequenza multistep che include cambiamenti conformazionali, rimozione di marcatori inibitori e l’accoppiamento di due molecole di RAF in un dimero attivo. Lo studio suggerisce che solo le molecole di RAF che permangono sulla membrana abbastanza a lungo possono completare questa sequenza, una forma di “controllo cinetico” che aiuta le cellule a evitare attivazioni accidentali da segnali fugaci e deboli. Rivelando come l’interazione tra legame a RAS, impegno dei lipidi e ri-legame laterale determini la residenza di RAF sulla membrana, il lavoro delinea una strategia generale con cui le cellule possono usare molte piccole e deboli interazioni sulle membrane per sintonizzare finemente vie di segnalazione potenti.
Citazione: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Parole chiave: RAS, chinasi RAF, segnalazione sulla membrana cellulare, ri-legame laterale, controllo cinetico