Clear Sky Science · it
Sequenziamento della metilazione e idrossimetilazione del DNA in concomitanza con caratteristiche cromatiniche
Leggere le annotazioni chimiche delle nostre cellule
Ogni cellula del corpo contiene lo stesso DNA, eppure le cellule cerebrali, quelle della pelle e le cellule staminali si comportano in modo molto diverso. Una ragione è che le cellule scrivono sulle molecole di DNA e sulle proteine che le avvolgono delle "annotazioni" chimiche che aiutano a spegnere o accendere i geni. Fino ad oggi i ricercatori hanno faticato a leggere insieme più di queste annotazioni sullo stesso tratto di DNA, lasciando un vuoto nella comprensione di come agiscano in combinazione. Questo studio presenta un nuovo modo di leggere contemporaneamente sia il codice genetico sia le marcature chimiche chiave, rivelando come si combinano per controllare interruttori genetici importanti chiamati enhancer.
Perché il DNA ha bisogno dei segni a matita
Il DNA non agisce da solo. È avvolto intorno a proteine chiamate istoni per formare la cromatina, e sia il DNA sia gli istoni possono essere decorati con piccoli gruppi chimici. Due marche importanti sul DNA sono i gruppi metile e idrossimetile aggiunti alla lettera C (citosina). Questi segni influenzano quanto strettamente il DNA è impacchettato e se i geni vicini sono attivi. In termini generali, i segni di metilazione sono spesso associati al silenziamento genico, mentre i segni di idrossimetilazione tendono ad apparire dove i geni sono attivi. Ma l’effetto di questi marchi dipende dal loro contesto locale: esattamente dove si trovano nel genoma e accanto a quali marcature istoniche.
Il problema delle mappe separate
I metodi di sequenziamento esistenti possono mappare metilazione e idrossimetilazione su tutto il genoma, e altri metodi mappano le marcature istoniche che segnalano regioni attive o silenti. Tuttavia, queste misurazioni sono di solito effettuate in esperimenti separati e poi confrontate al computer. Questo ci dice quali caratteristiche tendono a trovarsi nello stesso quartiere, ma non se coesistono davvero sullo stesso pezzo di DNA in una singola cellula. Tentativi precedenti di combinare queste misure si basavano su trattamenti chimici aggressivi che danneggiavano il DNA e, cosa cruciale, non potevano distinguere in modo affidabile metile da idrossimetile nella stessa lettura. Di conseguenza, ai ricercatori mancava un quadro molecolare chiaro di come le combinazioni di marche cooperino.
Un nuovo metodo di lettura multilivello
Gli autori hanno sviluppato un metodo chiamato 6-base-CUT&Tag che può leggere tutte e quattro le basi del DNA più due stati chimici della citosina—normale, metilata e idrossimetilata—su frammenti di DNA fisicamente legati a specifiche caratteristiche della cromatina. Innanzitutto usano anticorpi come ganci molecolari per estrarre il DNA avvolto attorno agli istoni che portano una marcatura specifica, per esempio un segnale di cromatina attiva. Un enzima ingegnerizzato inserisce poi adattatori speciali, trasformando ogni frammento catturato in un piccolo anello che resiste ai passaggi di purificazione che distruggono pezzi sfuggenti. Un processo chimico e enzimatico raffinato converte quindi i diversi stati della citosina in segnali di sequenza distinti, che i sequenziatori moderni possono leggere. In questo modo, una singola lettura riporta da dove proviene il frammento, quale marcatura istonica portava e quali citosine su di esso erano metilate o idrossimetilate.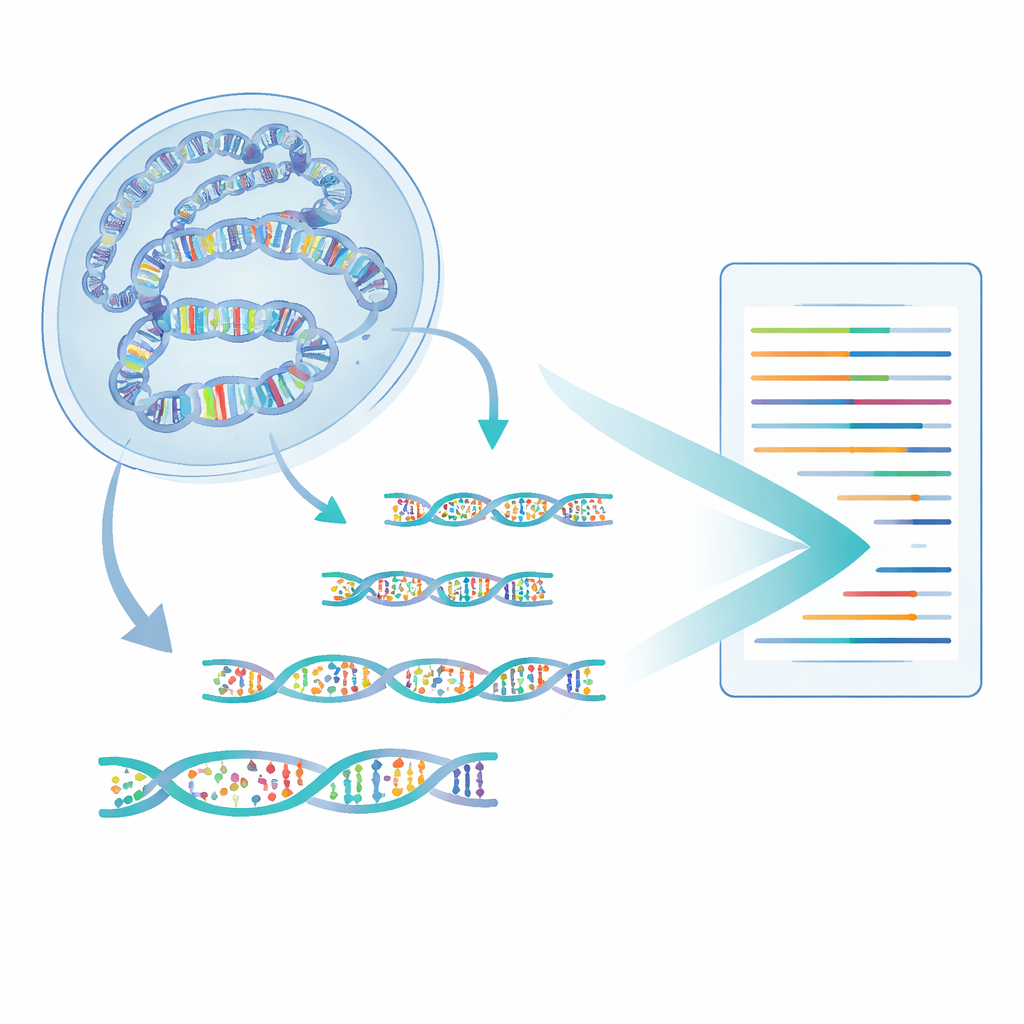
Zoom sugli interruttori genici
Usando cellule staminali embrionali di topo come caso di studio, il gruppo ha applicato il 6-base-CUT&Tag a diverse marcature istoniche chiave che etichettano tipi differenti di DNA regolatorio. Si sono concentrati sugli enhancer—tratti di DNA che agiscono come interruttori per controllare quando e dove i geni si attivano. Gli enhancer possono trovarsi in stati “attivo”, “primed” (preparato) o “poised” (pronto), distinti da marcature istoniche particolari. I ricercatori hanno scoperto che gli enhancer contrassegnati solo da un tag istonico chiamato H3K4me1 (spesso considerato "primed") presentavano i livelli più alti sia di metilazione sia di idrossimetilazione del DNA, specialmente se esaminati direttamente sui nucleosomi legati a H3K4me1. Al contrario, gli enhancer con segni aggiuntivi di forte attività o repressione portavano meno di queste marche sul DNA o mostravano uno spostamento verso l’idrossimetilazione, suggerendo una cancellazione in corso della metilazione.
Decodificare gli stati degli enhancer con maggiore dettaglio
Poiché tutti i tipi di enhancer condividono la marcatura H3K4me1, il team si è chiesto se il modello dettagliato delle marche del DNA specificamente sul DNA marcato H3K4me1 potesse da solo distinguere i diversi stati degli enhancer. Hanno addestrato un modello di apprendimento automatico usando i dati 6-base-CUT&Tag per classificare gli enhancer come attivi, primed o poised, basandosi esclusivamente sulla quantità di metile e idrossimetile presenti in quella singola caratteristica istonica. Questo modello ha superato un modello altrimenti identico addestrato su dati standard a livello di intero genoma non limitati a nessuna marcatura istonica. In altre parole, leggere le marche del DNA nel contesto immediato in cui si verificano fornisce un quadro più nitido rispetto alla media su tutto il DNA nella cellula.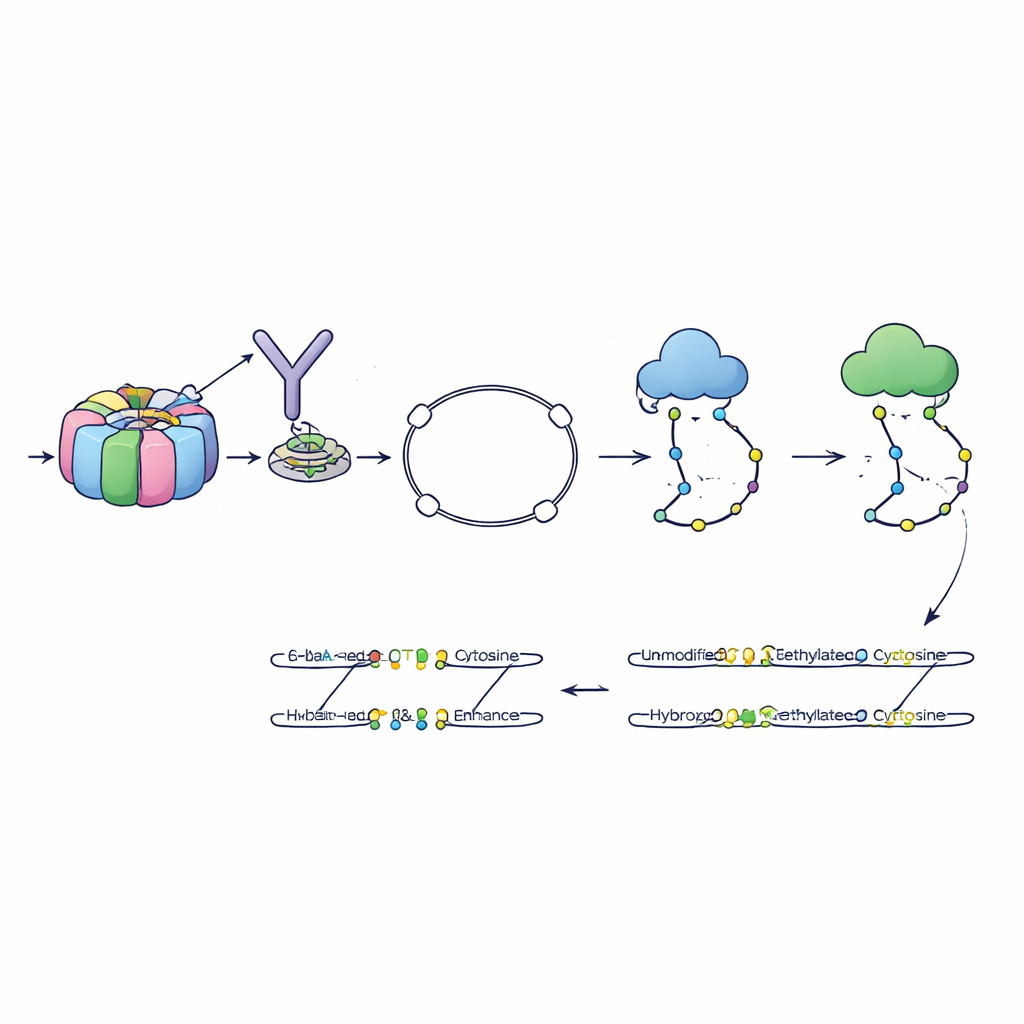
Cosa significa per la comprensione dell’identità cellulare
Per chi non è specialista, il messaggio chiave è che questo metodo permette ai ricercatori di leggere più strati di informazione—sequenza del DNA, marche del DNA e marche istoniche—sulla stessa molecola. Questa vista dettagliata rivela come combinazioni particolari di etichette chimiche definiscano lo stato di prontezza degli interruttori genici nelle cellule staminali. Poiché il 6-base-CUT&Tag è più efficiente e meno dannoso rispetto agli approcci precedenti, può scoprire schemi sottili che prima erano nascosti. Col tempo, questa lettura multilivello della cromatina potrebbe aiutare a spiegare come le cellule ricordano la propria identità, come cambiano durante lo sviluppo o nella malattia e come potremmo indirizzare in modo più preciso il codice regolatorio nelle terapie.
Citazione: Araujo Tavares, R.d.C., Dhir, S., He, X. et al. Sequencing DNA methylation and hydroxymethylation at co-occurring chromatin features. Nat Commun 17, 2591 (2026). https://doi.org/10.1038/s41467-026-69429-6
Parole chiave: epigenetica, metilazione del DNA, cromatina, enhancer, cellule staminali