Clear Sky Science · it
La carenza di MDA5 ritarda l’invecchiamento ematopoietico modulando inflammaging e proteostasi nei topi
Perché mantenere giovane il sangue è importante con l’età
Con l’avanzare dell’età, il sistema che produce le nostre cellule del sangue si deteriora lentamente. Le cellule staminali nel midollo osseo che normalmente rimpiazzano globuli rossi, cellule immunitarie e piastrine diventano più inclini all’infiammazione e più propense a generare certi tipi cellulari a scapito di altri. Questo cambiamento contribuisce ad anemia, immunità indebolita e aumentato rischio di cancro nella vecchiaia. Lo studio riassunto qui esplora un attore sorprendente in questo processo: un sensore antivirale chiamato MDA5. Disattivando questa singola molecola nei topi, i ricercatori hanno scoperto di poter mantenere le cellule staminali ematopoietiche funzionalmente più giovani più a lungo.
Un sensore nato per combattere i virus che si ritorce contro con l’età
MDA5 è un sensore dell’immunità innata che rileva l’RNA a doppio filamento, un motivo molecolare comune nei virus ma prodotto anche dai nostri genomi, in particolare da elementi genetici mobili la cui attività aumenta con l’età. Quando MDA5 riconosce tale RNA, innesca una cascata di segnali infiammatori e risposte antivirali. Il gruppo si è chiesto se questa attivazione costante a basso livello negli animali più anziani potesse alimentare l’“inflammaging” – l’infiammazione persistente e latente che accompagna l’invecchiamento – nel midollo osseo. Confrontando topi normali con topi privi di MDA5, hanno misurato molte molecole di segnalazione immunitaria nel fluido del midollo. I topi anziani privi di MDA5 presentavano livelli nettamente più bassi di citochine infiammatorie chiave, inclusi interferone-β e interleuchina-1, e mostravano una minore attivazione di regioni genomiche infiammatorie nelle staminali, indicando un ambiente più tranquillo e meno infiammato.
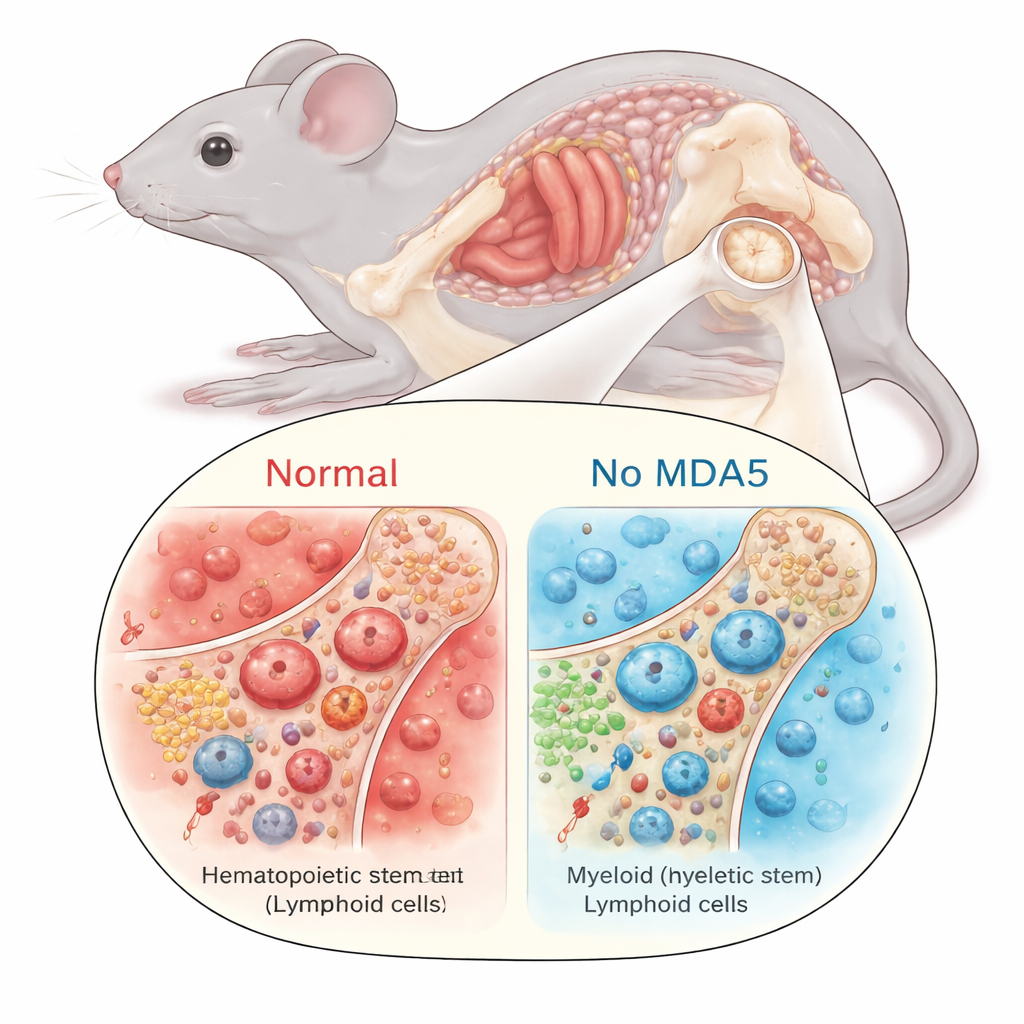
Comportamento più giovanile delle cellule staminali del sangue invecchiate
Con meno infiammazione nel midollo, le cellule staminali ematopoietiche si comportavano in modo diverso. Nell’invecchiamento normale, queste HSC tendono ad accumularsi in numero ma a perdere qualità: si dividono più spesso, perdono la capacità rigenerativa a lungo termine e sviluppano un bias verso la produzione di cellule mieloidi (come alcuni globuli bianchi) anziché linfoidali che supportano l’immunità adattativa. Nei topi anziani privi di MDA5, questo schema tipico era attenuato. Le loro HSC si espandevano meno, mostravano un bias mieloide ridotto e restavano più quiescenti – trascorrendo più tempo in uno stato di riposo invece che nel ciclo cellulare. Quando i ricercatori trapiantarono numeri uguali di cellule staminali in topi riceventi irradiati, le HSC anziane senza MDA5 furono più efficaci nel ricostruire il sistema ematopoietico in contesti non competitivi, indicando riserve funzionali superiori rispetto alle HSC normali di pari età.
Metabolismo e controllo della qualità delle proteine restano più giovanili
Oltre ai conteggi e al comportamento cellulare, i ricercatori hanno esaminato il funzionamento interno di queste staminali. Usando una combinazione di espressione genica, accessibilità della cromatina, profilazione dei metaboliti e analisi a singola cellula, hanno riscontrato che la perdita di MDA5 preservava un profilo metabolico e di mantenimento proteico più giovanile. Le HSC anziane prive di MDA5 avevano marcatori redox più sani, come livelli inferiori di glutatione ossidato e livelli più alti di NAD e NADP, molecole legate alla resilienza cellulare. All’interno di queste cellule, le proteine mal ripiegate e non ripiegate – un segno distintivo dell’invecchiamento e dello stress – erano ridotte, mentre i marcatori dell’autofagia, il processo con cui le cellule riciclano componenti danneggiati, aumentavano. La sintesi proteica era diminuita e gli amminoacidi si accumulavano, coerente con uno spostamento verso un controllo più accurato della qualità delle proteine piuttosto che una produzione rapida e soggetta a errori.
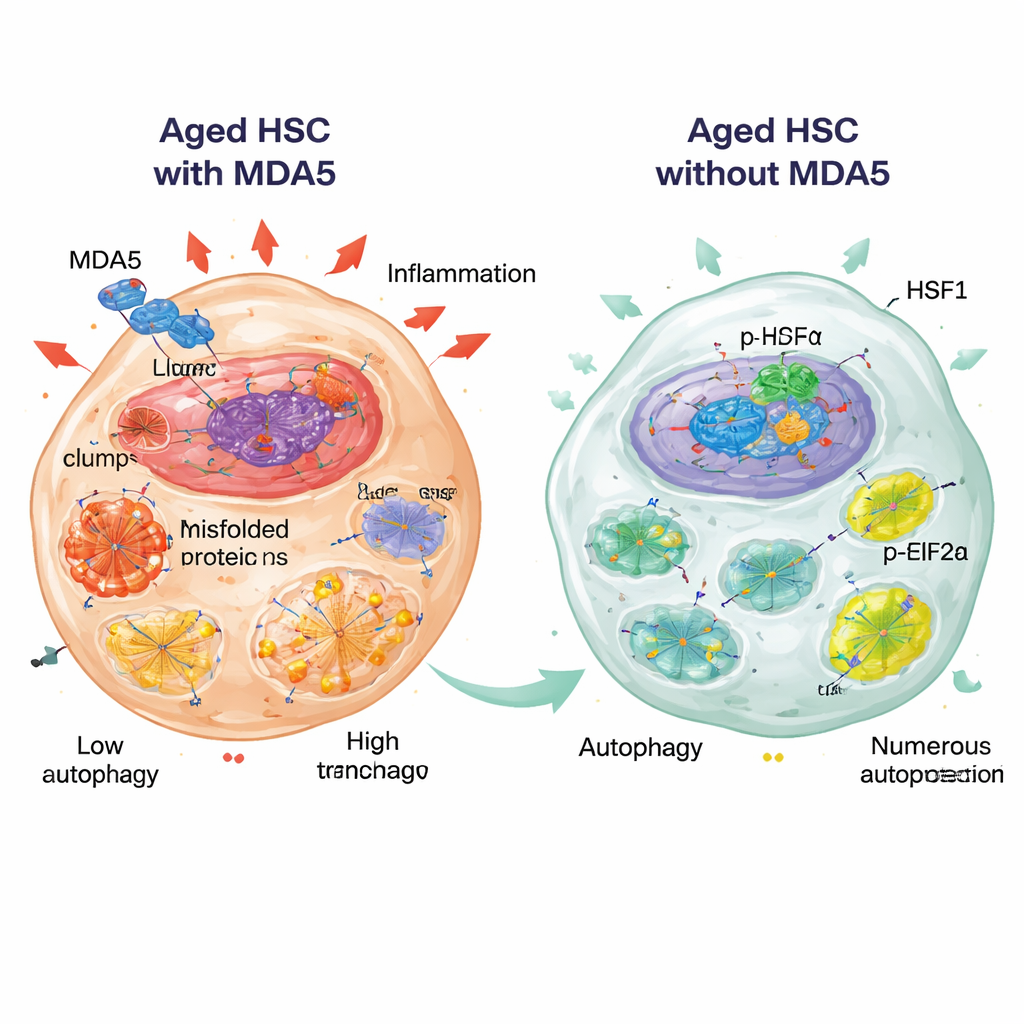
HSF1 e eIF2α: guardiani della proteostasi
Due regolatori molecolari sono emersi come centrali in questo stato protettivo: HSF1, un fattore di trascrizione maestro che aumenta la produzione di chaperoni e altri fattori protettivi delle proteine, ed eIF2α, un fattore di traduzione la cui forma fosforilata (p-eIF2α) rallenta la sintesi proteica durante lo stress. Nelle HSC anziane prive di MDA5, i livelli proteici di HSF1 e la sua localizzazione nucleare erano elevati, e p-eIF2α risultava aumentato, coerente con un programma attivo di protezione dallo stress. Gli autori hanno osservato che MDA5 può avvicinarsi a HSF1 e che, quando sovraespresso, può trattenere HSF1 nel citoplasma, suggerendo che MDA5 attivo potrebbe limitare le benefiche funzioni nucleari di HSF1. Importante, quando hanno attivato farmacologicamente HSF1 in HSC normali anziane usando una piccola molecola, queste cellule sono diventate più quiescenti e hanno mantenuto meglio la capacità di formare colonie attraverso ripetuti cicli in coltura, mimando parzialmente le caratteristiche giovanili osservate in assenza di MDA5.
Che cosa significa per l’invecchiamento sano del sangue
Complessivamente, questi risultati dipingono uno scenario in cui l’attivazione cronica di un sensore antivirale, MDA5, spinge gradualmente le cellule staminali ematopoietiche verso infiammazione, stress metabolico e danno proteico. Rimuovere MDA5 nei topi interrompe questo circolo: i segnali infiammatori nel midollo sono attenuati, le HSC restano più riposate e meno sbilanciate, e i loro sistemi interni di controllo della qualità delle proteine rimangono robusti. Sebbene disattivare direttamente MDA5 nelle persone sarebbe rischioso a causa del suo ruolo nella difesa dalle infezioni, questo lavoro sottolinea il principio più ampio che mirare all’infiammazione legata all’età e rafforzare la proteostasi potrebbe aiutare a preservare la funzione delle cellule staminali del sangue nella terza età. A lungo termine, vie più sicure per modulare i percorsi correlati a MDA5 o per potenziare le risposte protettive guidate da HSF1 ed eIF2α potrebbero offrire strategie per estendere il periodo di salute del nostro sistema ematico e immunitario.
Citazione: Bergo, V., Bousounis, P., To Vu, G. et al. Lack of MDA5 delays hematopoietic aging by modulating inflammaging and proteostasis in mice. Nat Commun 17, 1645 (2026). https://doi.org/10.1038/s41467-026-69424-x
Parole chiave: cellule staminali ematopoietiche, inflammaging, MDA5, proteostasi, sangue invecchiato