Clear Sky Science · it
Base strutturale e molecolare della regolazione allosterica e del collegamento catalitico della fosforibosilformilglicinamidina sintetasi umana
Perché questo enzima è importante per la salute
Ogni cellula del corpo dipende dalle purine, piccole molecole che alimentano reazioni, immagazzinano energia e trasportano informazioni genetiche. Le cellule tumorali, che si dividono rapidamente, sono particolarmente affamate di purine e spesso riorganizzano i percorsi di sintesi. Questo studio si concentra su un enzima umano chiamato FGAMS, un attore chiave nella costruzione delle purine da zero. Rivelando la struttura tridimensionale di FGAMS e come le sue parti si muovono e comunicano, gli autori mostrano come l'enzima venga acceso e spento e come possa essere preso di mira per rallentare la crescita tumorale.
I mattoni della vita sotto controllo
Le cellule producono purine attraverso una complessa catena di montaggio nota come via de novo, che richiede energia e diversi enzimi per assemblare un anello complesso. FGAMS esegue il quarto passaggio di questa sequenza e si trova al centro di un ammasso enzimatico più ampio chiamato purinosoma, che aiuta a convogliare gli ingredienti in modo efficiente. Poiché le cellule tumorali in rapida crescita spesso potenziano questa via, enzimi come FGAMS sono bersagli farmacologici interessanti: bloccarli può privare i tumori dei nucleotidi di cui hanno bisogno mentre le cellule sane ricorrono a percorsi di riciclo.
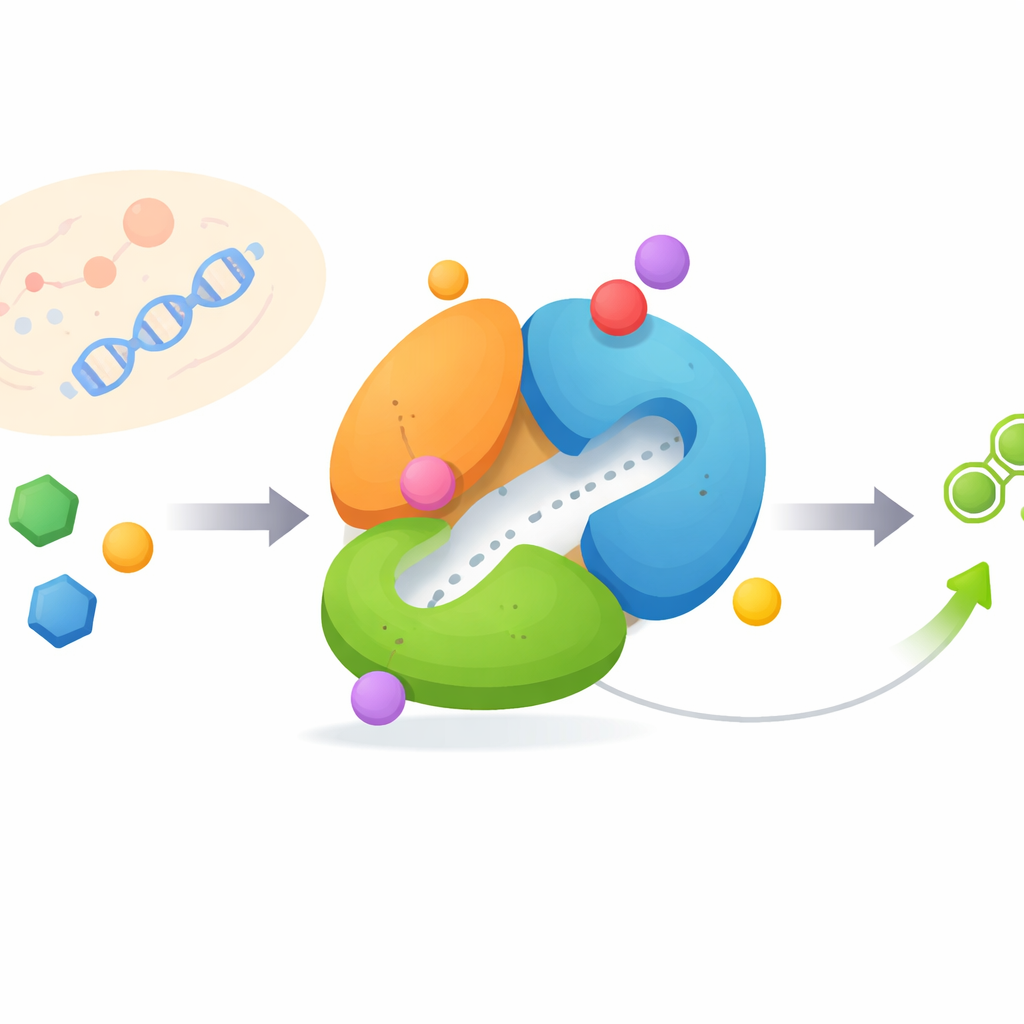
Una macchina molecolare che cambia forma
FGAMS è costituito da tre parti connesse, o domini, ognuna delle quali svolge un compito diverso e deve cooperare in un ordine preciso. Un dominio rimuove l'ammoniaca dall'amminoacido glutammina, un altro utilizza quell'ammoniaca per modificare una piccola molecola zuccherina, e un terzo dominio funge da hub regolatorio. Utilizzando la criomicroscopia elettronica ad alta risoluzione, i ricercatori hanno catturato FGAMS in tre stati di lavoro distinti: con una molecola trasportatrice di energia legata, con un intermedio di reazione a vita breve intrappolato, e con più substrati e intermedi presenti contemporaneamente. Il confronto tra questi stati ha rivelato che anse flessibili e un «braccio» N-terminale si muovono in modo drammatico, riconfigurando l'enzima man mano che la chimica procede.
Tunnel nascosto e porte molecolari
Un enigma chiave è stato come l'ammoniaca rilasciata in un dominio viaggi in sicurezza verso il sito distante dove viene utilizzata, senza diffondersi e causare danni. Le nuove strutture mettono in luce un tunnel interno precedentemente non osservato che collega i due siti, insieme a una serie di «porte» formate da specifici amminoacidi. Quando i substrati appropriati si legano e si forma l'intermedio, un'ansa centrale scatta in una posizione ordinata, tirando sul dominio N-terminale e riorganizzando anse vicine nel dominio catalitico. Questa coreografia apre due porte d'accesso così la glutammina può essere processata e rimodella temporaneamente una regione che stabilizza l'intermedio ad alta energia necessario per la rottura del legame.
Collegare la chimica attraverso il movimento
Man mano che la reazione procede, l'enzima non sta semplicemente in attesa; usa ogni passaggio chimico come segnale. Una volta che si forma un intermedio tioestere covalente nel dominio che genera ammoniaca, i movimenti precedenti vengono parzialmente invertiti. Questo rilassa l'ansa centrale e riposiziona le porte per chiudere le vie di fuga, mentre due porte aggiuntive alle estremità del tunnel si spalancano. Spostamenti sottili in una manciata di residui «collo di bottiglia» allargano il passaggio interno, permettendo a una molecola di ammoniaca di viaggiare attraverso il tunnel direttamente nel secondo sito attivo, dove reagisce con l'intermedio intrappolato per produrre il prodotto finale. Mutare i residui delle porte provoca perdite di ammoniaca o la separazione delle due metà della reazione, confermando che questo sistema di porte e canale è essenziale per una catalisi efficiente.
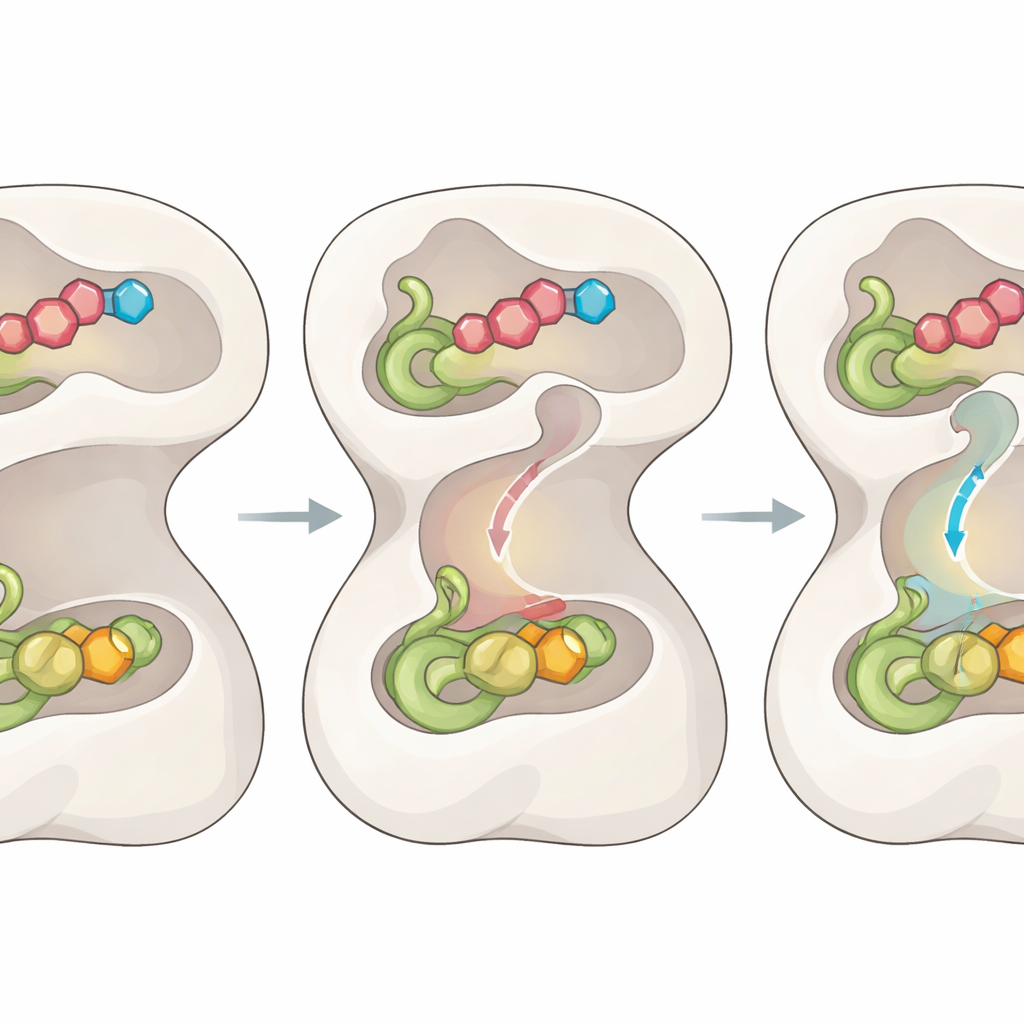
Dall'intuizione strutturale a vie terapeutiche
Seguendo FGAMS attraverso il suo ciclo catalitico, lo studio delinea un quadro dettagliato di come i movimenti dei domini, le anse flessibili, le porte interne e un tunnel transitorio siano tutti collegati per coordinare la chimica. Per un pubblico generale, il concetto fondamentale è che l'enzima funziona come una piccola fabbrica programmabile: apre le porte e la catena interna solo quando tutte le parti giuste sono al loro posto, garantendo velocità e sicurezza. Poiché FGAMS sostiene la produzione di purine nelle cellule tumorali ed è associato a una sopravvivenza peggiore nei tumori epatici, i progetti strutturali e i nuovi punti di controllo identificati offrono più punti d'appoggio per progettare farmaci che ostruiscano il tunnel, blocchino le porte o intrappolino intermedi chiave, potenzialmente dando origine a una nuova classe di terapie anticancro mirate.
Citazione: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Parole chiave: biosintesi delle purine, regolazione allosterica, canalizzazione dell'ammoniaca, metabolismo del cancro, struttura cryo-EM