Clear Sky Science · it
Regolazione a feedback negativo della segnalazione STING mediante Golgifagia diretta da TAX1BP1
Come le cellule evitano una reazione immunitaria eccessiva
Il nostro sistema immunitario deve percorrere una linea sottile: riconoscere rapidamente virus invasori e DNA danneggiato, ma anche spegnere quell’allarme prima che l’infiammazione incontrollata danneggi i tessuti sani. Questo studio svela come un aiutante cellulare poco noto, TAX1BP1, funzioni da freno integrato su una potente via di allarme chiamata cGAS–STING. Spiegando come le cellule smontano questo allarme una volta compiuto il suo compito, il lavoro getta luce sulle malattie autoimmuni, sulla difesa antivirale e su possibili terapie antitumorali.
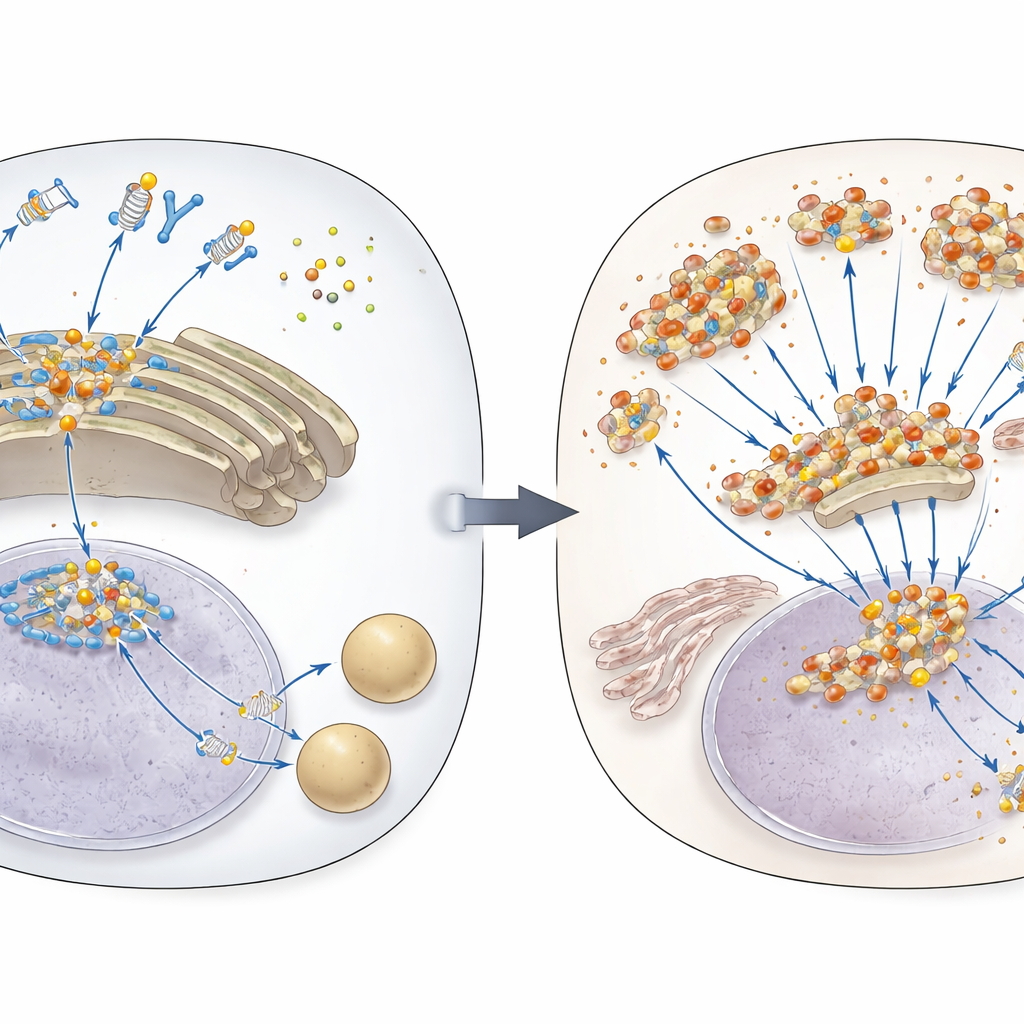
Il sistema di allarme del DNA cellulare
Quando DNA estraneo o fuori posto compare nel fluido interno delle cellule, una proteina sensore chiamata cGAS lo rileva e produce una piccola molecola messaggera. Quel messaggero attiva STING, una proteina a scatto che si trova sulle membrane interne. STING quindi viaggia verso un hub di smistamento cellulare chiamato Golgi, dove si aggrega e innesca la produzione di molecole antivirali note come interferoni di tipo I, insieme ad altri segnali infiammatori. Poiché questa risposta è così potente, le cellule normalmente degradano STING dopo un breve picco di attività, inviandolo nei centri di riciclo cellulare chiamati lisosomi. Finora, il modo in cui STING veniva indirizzato a questo passo di spegnimento era stato compreso solo parzialmente.
Un freno cellulare con molti compiti
In precedenza TAX1BP1 era conosciuto come un multitasker che aiuta il sistema di smaltimento cellulare, l’autofagia, a riconoscere materiale indesiderato. Può legarsi sia al carico marcato per la rimozione sia ai sacchi in formazione che lo ingloberanno. Gli autori si sono chiesti se TAX1BP1 potesse anche contribuire a contenere l’allarme cGAS–STING. Usando cellule di tipo immunitario umano e macrofagi di topo privi di TAX1BP1, hanno osservato che l’attivazione di cGAS o STING produceva molte più quantità di interferone e citochine infiammatorie rispetto alle cellule normali. Queste cellule carenti di TAX1BP1 risultavano inoltre più resistenti all’infezione da virus herpes simplex, coerentemente con il loro segnalamento antivirale iperattivato.
Pulire STING e un Golgi sotto stress
Approfondendo, i ricercatori hanno mostrato che in assenza di TAX1BP1, STING restava attivo più a lungo ed veniva degradato più lentamente. Microscopia e test biochimici hanno rivelato che STING attivo forma grandi aggregati e che questi ammassi si accumulano quando manca TAX1BP1. Allo stesso tempo, la struttura del Golgi si rigonfia e si frammenta in pezzi. Il gruppo ha scoperto che TAX1BP1, insieme a un altro fattore di riciclo chiamato p62, indirizza questi frammenti di Golgi danneggiati e gli aggregati di STING su di essi alla distruzione nei lisosomi — una forma specializzata di pulizia che gli autori definiscono “Golgifagia”. Questo processo è distinto dall’autofagia classica di tipo bulk e utilizza invece vie più selettive per catturare i pezzi sovraccarichi del Golgi.
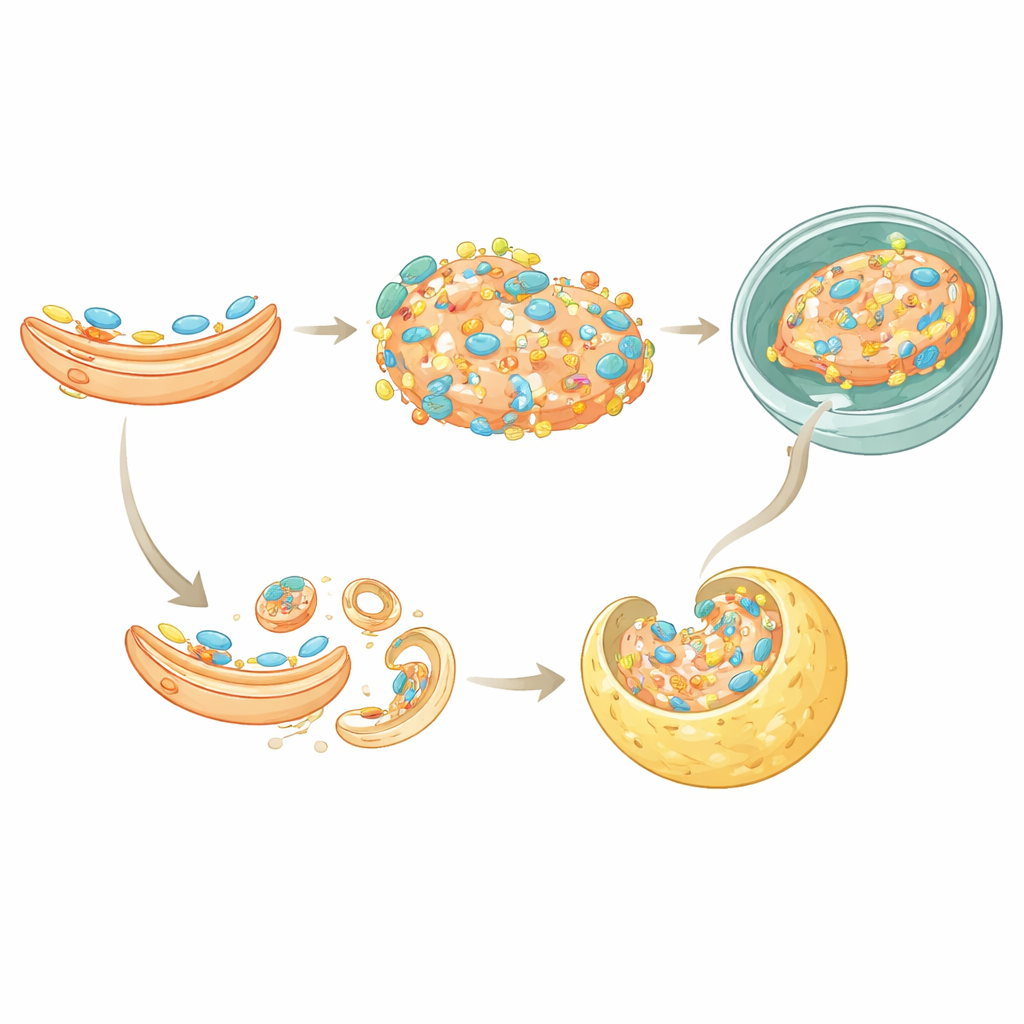
Due vie per spegnere l’allarme
Lo studio ha inoltre individuato un secondo meccanismo con cui TAX1BP1 contribuisce a silenziare STING. Normalmente, una volta che STING ha segnalato al Golgi, viene incapsulato in piccole vescicole che si spaccano e vengono riconosciute da un sistema di smistamento delle proteine chiamato ESCRT, che poi consegna STING ai lisosomi. TAX1BP1 si lega direttamente a STING e ne facilita l’interazione con un componente chiave di ESCRT, HGS. Quando TAX1BP1 è stato rimosso, il trasferimento di STING a questa machineria di smistamento è risultato meno efficiente e la sua degradazione rallentata. Tuttavia, una certa degradazione avveniva ancora, indicando che TAX1BP1 lavora insieme a p62 in questa via di microautofagia, offrendo alle cellule modalità parzialmente ridondanti per assicurare che STING non persista troppo a lungo.
Perché questo conta per salute e malattia
Per verificare l’importanza di questo freno in organismi viventi, i ricercatori hanno ingegnerizzato topi privi di TAX1BP1 in specifiche cellule immunitarie. Stimolati con una molecola che attiva STING, questi topi presentavano livelli più alti di interferone e citochine infiammatorie nel sangue rispetto ai topi normali. Infettati con un poxvirus, ospitavano meno virus, mostrando una resistenza aumentata. Nel complesso, questi risultati suggeriscono che TAX1BP1 mette in collegamento il momento dell’attivazione di STING al Golgi con uno spegnimento temporizzato tramite la distruzione mirata sia di STING sia delle membrane del Golgi danneggiate. In termini semplici, il messaggio è che le cellule non solo attivano un allarme quando rilevano DNA pericoloso, ma smontano attivamente parti della loro rete interna per assicurarsi che l’allarme si spenga. Comprendere e, potenzialmente, modulare questo freno interno potrebbe aiutare a progettare trattamenti per malattie infiammatorie croniche, migliorare le difese antivirali o modulare le risposte immunitarie nel cancro.
Citazione: Suklabaidya, S., Mohanty, S., Reider, I.E. et al. Negative feedback regulation of STING signaling by TAX1BP1-directed Golgiphagy. Nat Commun 17, 2762 (2026). https://doi.org/10.1038/s41467-026-69422-z
Parole chiave: immunità innata, via STING, autofagia, apparato del Golgi, risposta antivirale