Clear Sky Science · it
Meccanismo molecolare d’azione della piccola molecola SMT-738 sul trasportatore di lipoproteine batterico LolCDE
Perché questo nuovo antibiotico è importante
All’aumentare delle infezioni ospedaliere che resistono ai nostri migliori antibiotici, i medici hanno urgente bisogno di farmaci in grado di uccidere i batteri pericolosi senza distruggere i microrganismi utili che ospitiamo. Questo studio chiarisce come una promettente sostanza sperimentale, chiamata SMT-738, blocchi una macchina di trasporto cruciale nella membrana esterna di alcuni batteri difficili da trattare. Rivelando esattamente dove e come il composto inceppa il meccanismo, il lavoro indica la via per antibiotici più intelligenti che colpiscano i superbug risparmiando gran parte del microbioma intestinale.
L’armatura esterna dei batteri nocivi
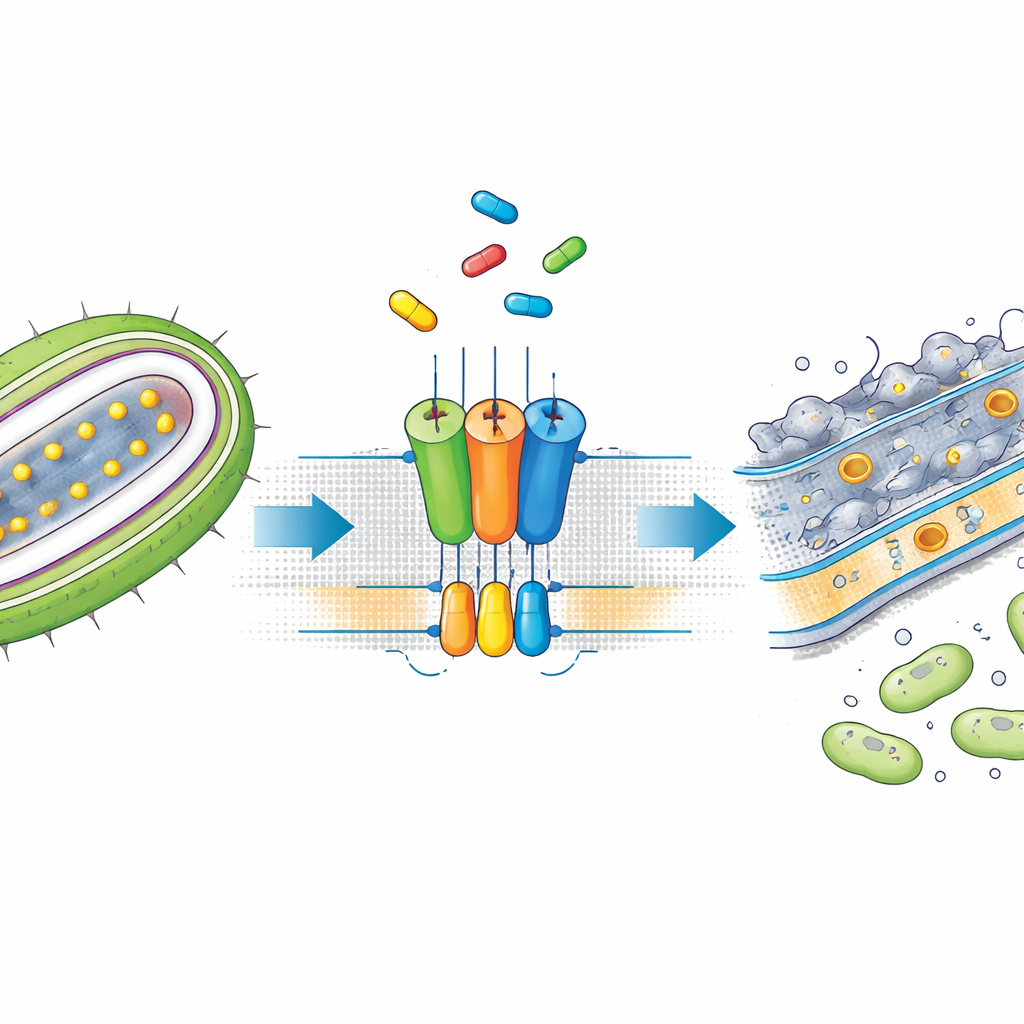
Molti dei patogeni ospedalieri più preoccupanti appartengono a un gruppo noto come batteri Gram-negativi. Sono difficili da eliminare perché si avvolgono in un’armatura esterna a doppio strato. Questo strato esterno è costruito e mantenuto da diverse macchine molecolari che spostano elementi costitutivi chiave dalla membrana interna, dove vengono sintetizzati, verso la superficie. Un carico importante sono le lipoproteine, che aiutano a mantenere l’integrità dell’involucro esterno e supportano processi come l’assorbimento di nutrienti e la resistenza agli antibiotici. Un sistema di trasporto chiamato via Lol, e in particolare una pompa denominata LolCDE, estrae le lipoproteine dalla membrana interna e le affida a chaperon che le portano alla superficie esterna. Poiché questi passaggi sono essenziali, rappresentano bersagli attraenti per nuovi antibiotici.
Una piccola molecola che ferma il nastro trasportatore
SMT-738 è emerso da screening precedenti come un potente inibitore dei patogeni Gram-negativi appartenenti alla famiglia Enterobacteriaceae, incluse ceppi multi-resistenti di Escherichia coli e Klebsiella pneumoniae. Tuttavia il suo preciso meccanismo d’azione non era chiaro. Gli autori hanno prima dimostrato che SMT-738 impedisce il rilascio di una lipoproteina di prova da parte di LolCDE in batteri ingegnerizzati, confermando che il composto blocca effettivamente il passaggio di trasporto. Importante, quando i batteri portavano certe mutazioni nei geni del complesso LolCDE, diventavano resistenti a SMT-738, suggerendo che il farmaco agisca legandosi direttamente a questa pompa. Queste osservazioni hanno preparato il terreno per un’analisi strutturale approfondita di come il composto interagisca con il trasportatore.
Inceppare la pompa dall’interno
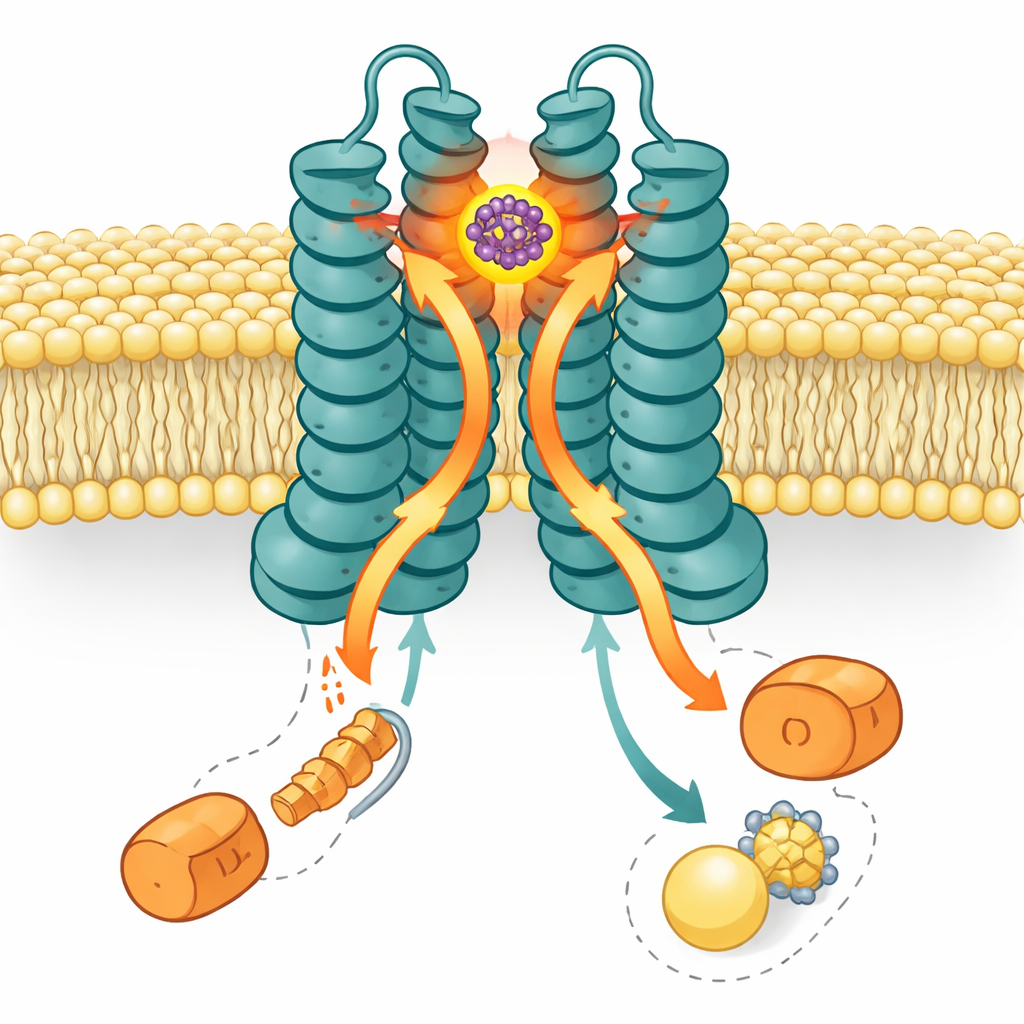
Usando la microscopia crio-elettronica ad alta risoluzione, i ricercatori hanno ottenuto un’immagine tridimensionale di LolCDE con SMT-738 bloccato in posizione. La struttura mostra il farmaco incastrato in una tasca all’estremità periplasmatica — il lato rivolto allo spazio tra la membrana interna e quella esterna — tra due subunità centrali, LolC e LolE. Questo sito sovrappone l’area di docking normale per il carico di lipoproteine. Quando SMT-738 occupa questa tasca, gli amminoacidi circostanti in LolC e LolE si spostano fino a circa un nanometro. Questi movimenti generano collisioni steriche con dove la lipoproteina e le sue code lipidiche si collocherebbero normalmente, bloccando efficacemente l’ingresso del carico nella pompa. La mutazione di molte di queste residenze che fiancheggiano la tasca indeboliva il legame con il farmaco o conferiva resistenza ai batteri, corrispondendo perfettamente all’immagine strutturale.
Scatenare un collasso unilaterale
La storia non si ferma al sito di legame. LolCDE è alimentato da due copie di una subunità motrice chiamata LolD, che si trovano dal lato citoplasmatico e consumano ATP per fornire energia al trasporto. In modo sorprendente, nella struttura con SMT-738 legato, rimane attaccata solo una LolD; la partner si è dissociata. Gel elettroforetici biochimici e saggi ATPasici hanno confermato che il legame di SMT-738 provoca la perdita di una LolD e riduce drasticamente l’attività energetica della pompa. Simulazioni al computer del trasportatore in una membrana hanno rafforzato questa visione: mentre SMT-738 si insediava nella sua tasca, cambiamenti conformazionali si propagavano verso il basso, spingendo gli eliche di accoppiamento che collegano LolC e LolE a LolD. Questi spostamenti hanno imposto una collisione sfavorevole alla LolD legata a LolC, facendola staccare, mentre la LolD legata a LolE restava salda. Il risultato è una macchina asimmetrica, «bloccata», che non può più trasportare le lipoproteine.
Perché alcuni batteri vengono colpiti e altri risparmiati
SMT-738 presenta una caratteristica desiderabile: colpisce fortemente le Enterobacteriaceae resistenti ai farmaci ma lascia gran parte delle altre specie Gram-negativi presenti nell’intestino in larga parte intatte. Per capire questa selettività, il team ha confrontato le sequenze di LolE da batteri sensibili e resistenti e si è concentrato sulle posizioni che entrano in contatto con SMT-738. Due residui in LolE, in particolare uno corrispondente alla posizione D264 in E. coli, sono risultati determinanti. Nei patogeni sensibili, queste posizioni corrispondevano alla versione di contatto presente in E. coli, mentre in molti commensali intestinali resistenti erano sostituite da altri amminoacidi. Quando i ricercatori hanno ingegnerizzato E. coli per portare tali sostituzioni, i batteri sono diventati altamente resistenti a SMT-738 pur continuando a esprimere LolCDE. Le simulazioni hanno suggerito che questi cambiamenti alterano la flessibilità locale attorno alla tasca, riducendo la capacità di SMT-738 di legarsi. Interessante, un altro inibitore di LolCDE, la lolamicina, si appoggiava solo parzialmente a punti di contatto sovrapponibili e mostrava un diverso profilo di resistenza, suggerendo modi distinti di mirare la stessa pompa.
Nuovi progetti per antibiotici futuri
Combinando imaging strutturale, scansioni mutazionali, test biochimici e simulazioni al computer, questo lavoro mostra che SMT-738 non è semplicemente un tappo in un canale. Piuttosto, si ancora al lato periplasmatico della pompa LolCDE, blocca il sito di ingresso delle lipoproteine e poi innesca spostamenti a lunga distanza che fanno staccare una delle due unità motrici, congelando il trasportatore in uno stato inattivo. Questo meccanismo di «blocco allosterico» rappresenta un modo nuovo di disabilitare una macchina batterica e aiuta a spiegare perché SMT-738 può concentrarsi sui patogeni pericolosi risparmiando gran parte del microbioma. La mappa dettagliata della tasca di legame e il residuo chiave di selettività in LolE offrono ora un progetto razionale per progettare antibiotici di nuova generazione che sfruttino la stessa vulnerabilità con maggiore potenza e precisione.
Citazione: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Parole chiave: resistenza agli antibiotici, batteri Gram-negativi, trasporto di lipoproteine, inibitore di LolCDE, struttura cryo-EM