Clear Sky Science · it
La fotoliasi/criptocroma di Aspergillus nidulans rileva lo stress ossidativo e si sposta dai nuclei ai mitocondri
Come i funghi percepiscono luce e stress
La luce solare mantiene vive piante e funghi, ma porta anche pericoli come danni al DNA e composti ossigeno-reattivi nocivi. Questo studio esplora come una muffa comune, Aspergillus nidulans, utilizzi una singola proteina, chiamata CryA, per percepire sia la luce che lo stress ossidativo e per proteggersi. Capire questo “sensore doppio” non solo approfondisce la nostra conoscenza di come i microrganismi affrontano ambienti ostili, ma può anche chiarire come le cellule in generale coordinino i segnali tra il nucleo e i mitocondri produttori di energia.
Un enzima di riparazione attivato da luce blu con un ruolo nascosto
CryA appartiene a una famiglia di proteine note per riparare i danni al DNA causati dalla luce ultravioletta. Queste proteine, chiamate fotoliasi e criptochromi, usano una molecola assorbente della luce (un flavina) per sfruttare la luce blu e ripristinare basi del DNA danneggiate. I ricercatori hanno confermato che CryA possiede l’architettura classica di un enzima di riparazione del DNA, si lega ai cofattori usuali per la raccolta di luce e si raggruppa con fotoliasi note negli alberi evolutivi. Solo su queste basi, CryA sembrerebbe uno strumento di riparazione di routine. Tuttavia lavori precedenti avevano suggerito che influenzi anche lo sviluppo del fungo, comportandosi più come un interruttore regolato dalla luce che come un semplice meccanismo molecolare.
Un regolatore master dei geni sensibili alla luce
Per rivelare il lato regolatorio di CryA, il team ha seguito la sua localizzazione cellulare e come la variazione della sua quantità altera la crescita fungina. Hanno scoperto che in condizioni normali CryA si accumula nel nucleo, dove è conservato il DNA. Quando il gene cryA è stato rimosso, il fungo ha prodotto più strutture sessuali; quando CryA è stato sovraespresso, ha quasi completamente bloccato la formazione delle consuete spore asessuate, lasciando colonie pallide e vaporose. Test di espressione genica hanno mostrato che molti geni attivati dalla luce e legati allo sviluppo si sono attivati troppo in assenza di CryA e troppo poco quando CryA era sovraespresso. Nel complesso, questi risultati rivelano CryA come un elemento di retroazione negativa: la luce aumenta i livelli di cryA, CryA quindi entra nel nucleo e frena i geni indotti da luce e sviluppo, impedendo che la risposta sfugga al controllo. 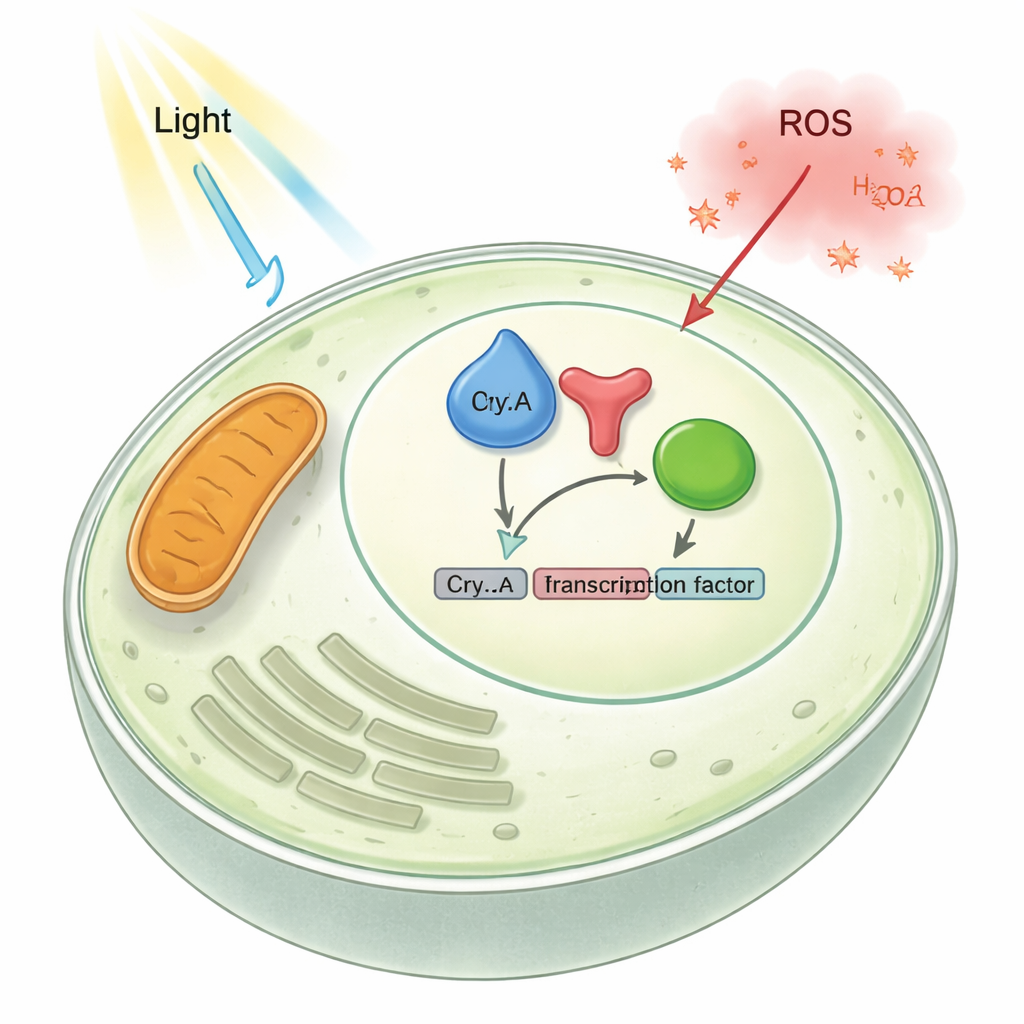
Interconnessione con le principali vie della luce e dello stress
Il fungo si affida già a un altro fotorecettore, un sensore della luce rossa chiamato fitocromo (FphA), e a una via di stress che termina in un fattore di trascrizione nominato AtfA. Usando test di interazione proteina–proteina in cellule vive e con proteine purificate, i ricercatori hanno mostrato che CryA si lega fisicamente sia a FphA sia ad AtfA nel nucleo. Quando cryA è stato eliminato, i geni normalmente attivati dalla luce rossa attraverso il fitocromo sono risultati più fortemente espressi; quando cryA era sovraespresso, sono diventati più difficili da attivare. Esperimenti sul cromatina hanno indicato che, in assenza di CryA, un gene chiave sensibile alla luce porta un maggior numero di marcatori istonici attivanti, suggerendo che CryA normalmente attenua l’attività di apertura della cromatina guidata dal fitocromo. Di fatto, CryA comprime sia il sensore di luce sia il fattore di trascrizione a valle, agendo come un freno condiviso per la segnalazione di luce e stress.
Un sensore rapido di stress che salta ai mitocondri
Lo stress ossidativo — un eccesso di specie reattive dell’ossigeno come il perossido d’idrogeno — rappresenta una minaccia costante per le cellule. Gli autori hanno riscontrato che tale stress, come la luce, aumenta l’espressione di cryA. Sorprendentemente, quando è stato aggiunto perossido d’idrogeno, CryA si è spostato dal nucleo ai mitocondri in meno di un minuto. Questo salto richiedeva una breve estensione flessibile all’estremità N-terminale della proteina e, in particolare, una singola cisteina amminoacidica al suo interno. Quando quella cisteina è stata sostituita con un altro residuo, CryA non è più riuscita a lasciare il nucleo in risposta allo stress. La troncare la coda N-terminale ha costretto CryA a localizzarsi permanentemente nei mitocondri. Questi ceppi ingegnerizzati hanno risposto in modo diverso agli ossidanti: versioni di CryA confinate al nucleo o solo ai mitocondri hanno modificato la resistenza del fungo al perossido d’idrogeno e al menadione e hanno rimodellato l’espressione dei geni antiossidanti. I risultati suggeriscono che CryA fa più che rilevare lo stress: potrebbe aiutare a coordinare la comunicazione tra mitocondri e nucleo in modo che le difese antiossidanti siano sintonizzate sul tipo e sul livello di danno. 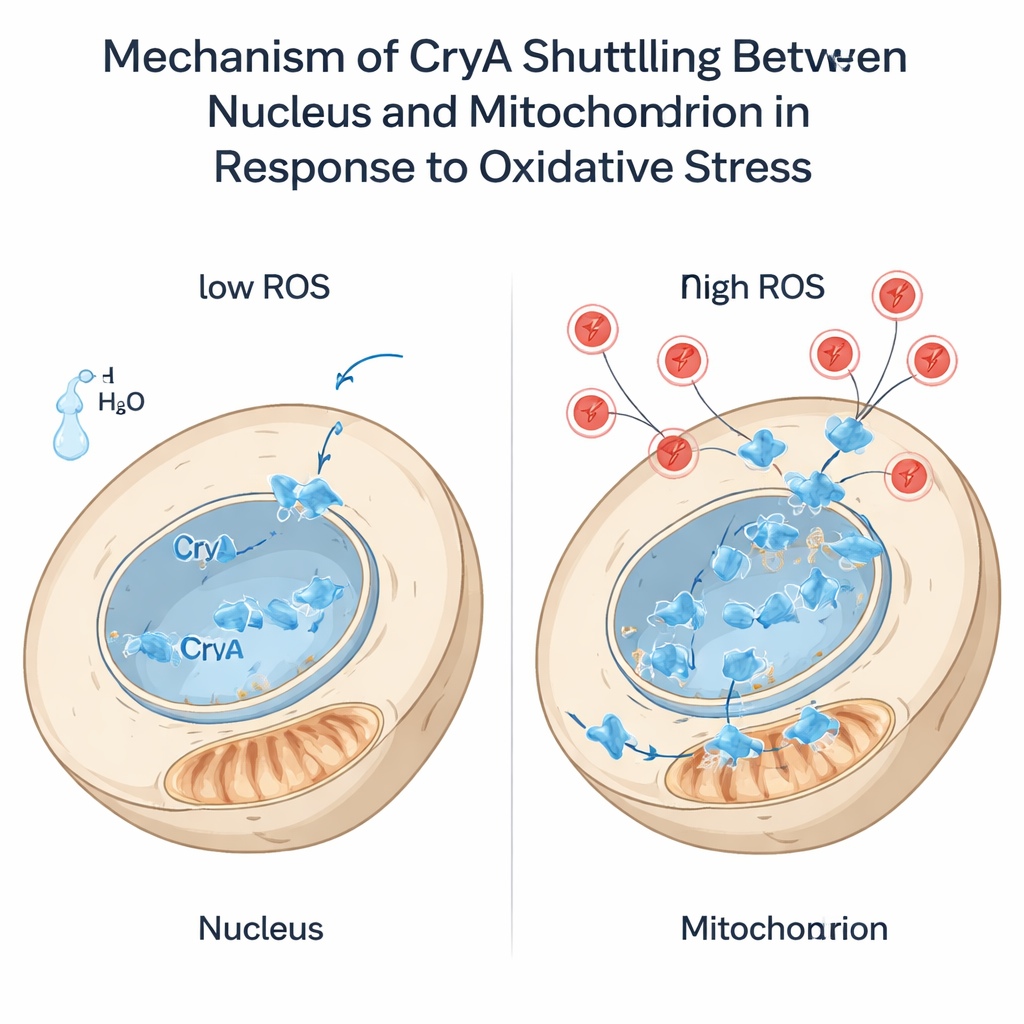
Perché è importante
Per un non specialista, CryA può essere pensata come un vigile del traffico cellulare che osserva sia la luce esterna sia lo stress ossidativo interno, quindi decide quando rallentare crescita, sviluppo e attività genica. Spostandosi tra nucleo e mitocondri e innestandosi su vie di segnalazione principali, impedisce al fungo di reagire in modo eccessivo a luce o stress pur consentendo una risposta protettiva rapida. Proteine e meccanismi simili esistono in molti organismi, quindi questo lavoro offre una finestra su come le cellule viventi integrano segnali ambientali con segnali di danno interni per sopravvivere in un mondo in continuo cambiamento.
Citazione: Landmark, A., Rudolf, T., Hundshammer, K. et al. The photolyase/cryptochrome of Aspergillus nidulans senses oxidative stress and shuttles from nuclei to mitochondria. Nat Commun 17, 1483 (2026). https://doi.org/10.1038/s41467-026-69403-2
Parole chiave: rilevamento della luce, stress ossidativo, criptocroma, mitocondri, sviluppo fungino