Clear Sky Science · it
Lattato derivato dai macrofagi guida il rimodellamento fenotipico dei fibroblasti dermici cutanei tramite la lattilazione della lisina 23 dell’istone H3 favorita da MCT1 nelle cicatrici ipertrofiche
Perché alcune cicatrici diventano spesse e rilevate
La maggior parte dei tagli e delle ustioni si trasforma col tempo in cicatrici sottili e piatte. Ma alcune ferite guariscono con fasce di tessuto spesse e rilevate, chiamate cicatrici ipertrofiche, che possono prudere, far male e limitare il movimento. Questo studio mette in luce un fattore inaspettato alla base di queste cicatrici ostinate: un comune prodotto metabolico chiamato lattato, prodotto dalle cellule immunitarie nella pelle rigida in fase di guarigione, che riprogramma le cellule riparatrici vicine facendole comportare in modo più aggressivo e favorendo la formazione di cicatrice.
Dalla riparazione normale alla cicatrice problematica
Nella guarigione sana delle ferite, le cellule della pelle collaborano per chiudere la lesione e ricostruire il tessuto. I fibroblasti, le principali cellule riparatrici dello strato più profondo della pelle, passano brevemente a una forma più attiva che produce collagene, la struttura proteica della pelle. Una volta che la ferita è sigillata, queste cellule si calmano di nuovo. Nelle cicatrici ipertrofiche, tuttavia, i fibroblasti rimangono bloccati in questo stato iperattivo, depositando troppo collagene in fasci spessi e disorganizzati. Gli autori hanno iniziato confrontando la pelle normale con il tessuto di cicatrice ipertrofica e hanno riscontrato un chiaro cambiamento metabolico: l’ambiente della cicatrice favoriva una chimica energetica rapida basata sul glucosio che genera grandi quantità di lattato, insieme a livelli elevati di una proteina di trasporto chiamata MCT1 che veicola il lattato nelle cellule. 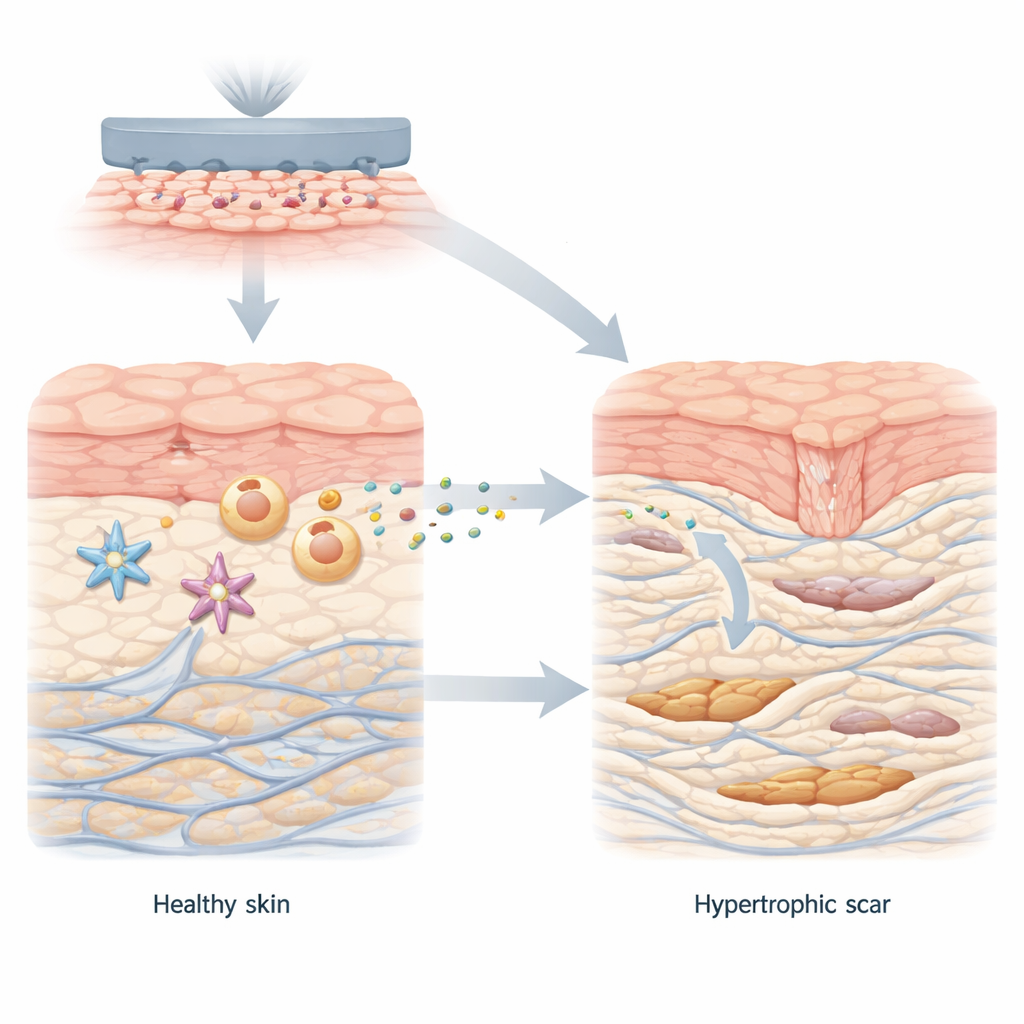
Le cellule immunitarie come inaspettate fabbriche di lattato
Per comprendere da dove provenisse tutto quel lattato, il gruppo ha esaminato diversi tipi cellulari della pelle umana e di modelli murini: macrofagi (cellule immunitarie che rimuovono residui e coordinano la guarigione), cellule dei vasi sanguigni e fibroblasti. Hanno coltivato queste cellule su materiali morbidi o rigidi che imitano la pelle normale e quella cicatriziale. Su superfici rigide, solo i macrofagi hanno cambiato il loro metabolismo verso un forte regime glicolitico, ovvero bramoso di zucchero, e hanno espulso grandi quantità di lattato, sia in colture in vitro sia nei tessuti cicatriziali reali. Quando i macrofagi sono stati rimossi dalle ferite in guarigione nei topi, i livelli di lattato tissutale sono diminuiti e la formazione della cicatrice si è attenuata. Questi risultati indicano i macrofagi, in particolare quelli che percepiscono un ambiente rigido, come le principali fabbriche di lattato che modellano il microambiente della cicatrice.
Il lattato come segnale che riorganizza i fibroblasti
Successivamente, i ricercatori hanno investigato come questo eccesso di lattato influisca sui fibroblasti. Quando i fibroblasti sono stati immersi in un fluido ricco di lattato proveniente da macrofagi coltivati su substrati rigidi, si sono moltiplicati più rapidamente, si sono mossi di più e hanno prodotto più collagene, tutti tratti distintivi dello stato aggressivo di miofibroblasto. Bloccare il trasportatore MCT1 sui fibroblasti o ridurre la produzione di lattato nei macrofagi ha ridotto nettamente questi cambiamenti. All’interno dei fibroblasti, il lattato in ingresso ha fatto più che alimentare la produzione di energia: ha innescato un segno chimico specifico sulle proteine istoniche, che avvolgono il DNA nel nucleo cellulare. Questo segno, chiamato lattilazione di H3K23, era molto più elevato nei fibroblasti che formano la cicatrice rispetto a quelli normali e agiva come un interruttore che attivava due geni chiave, HEY2 e COL11A1, che insieme amplificano i segnali di cicatrizzazione.
Un circuito di cicatrizzazione auto-rinforzante
Le proteine indotte da questo segno istonico formano un potente circuito di retroazione. HEY2 aumenta l’attività di una via che coinvolge YAP1 e SMAD2, nota per spingere i fibroblasti verso uno stato più contrattil e produttore di collagene. COL11A1, una proteina strutturale correlata al collagene, interagisce fisicamente con il trasportatore MCT1 sui fibroblasti, contribuendo a stabilizzarlo e a rendere più efficiente l’ingresso di lattato. In altre parole, il lattato che entra nella cellula modifica la regolazione genica in modo da aumentare ulteriormente l’assunzione di lattato e la produzione di collagene, bloccando i fibroblasti in un’identità pro-cicatriziale. 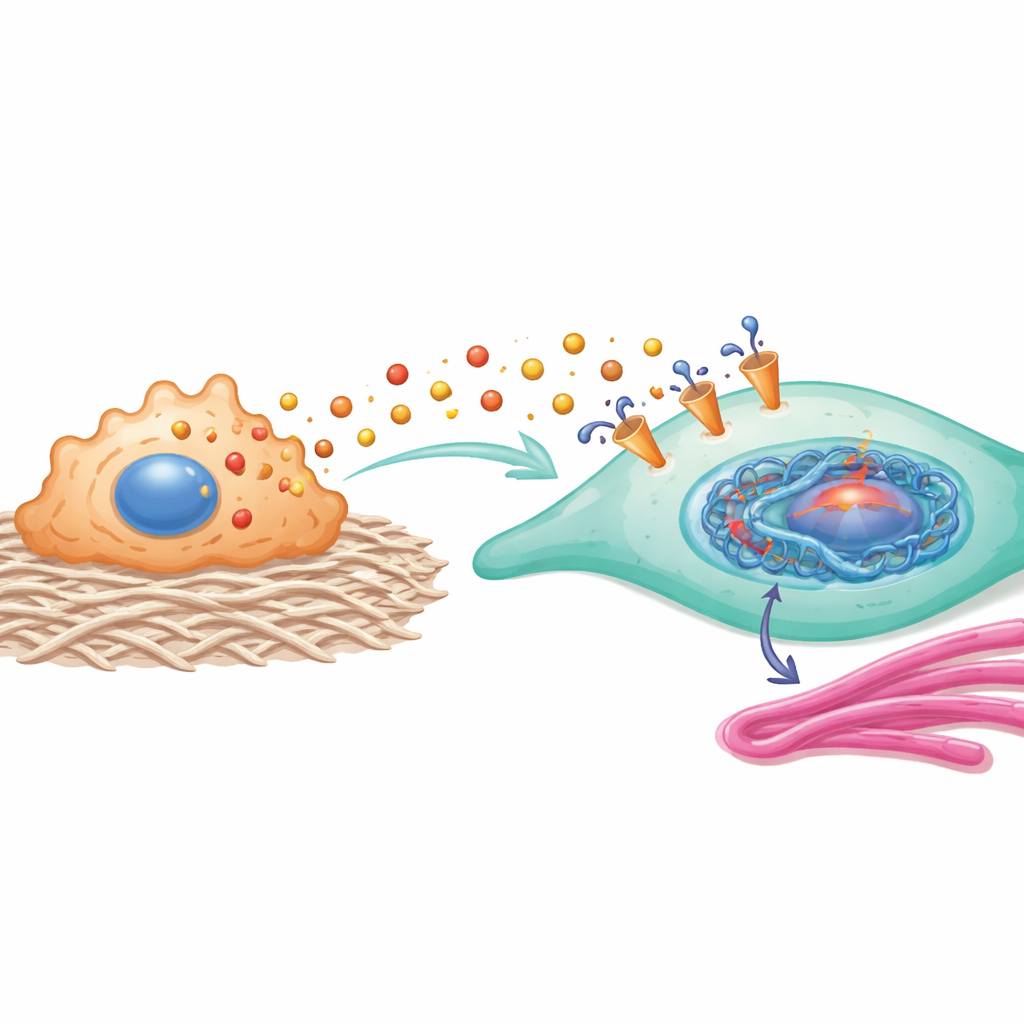
Attenuare il circuito per migliorare la guarigione
Per verificare se interrompere questo circuito può migliorare la guarigione, il team ha usato topi in cui MCT1 poteva essere rimosso selettivamente dai fibroblasti, oltre a un farmaco che blocca MCT1. In entrambi i casi, le ferite si sono chiuse più rapidamente, la pelle neoformata appariva più organizzata e le fibre di collagene erano più sottili e meglio allineate, con meno caratteristiche tipiche della cicatrice ipertrofica. Anche il segno istonico specifico e i suoi geni a valle sono diminuiti. La deplezione dei macrofagi, la principale fonte di lattato, o l’abbassamento chimico del lattato hanno prodotto effetti anti-cicatrice simili. Questi esperimenti dimostrano che la catena ferita rigida–macrofago–lattato–fibroblasto non è solo una correlazione ma un driver chiave della cicatrizzazione patologica.
Cosa significa per i trattamenti futuri delle cicatrici
Questo lavoro riconsidera il lattato, non più semplice prodotto di scarto metabolico, ma potente messaggero che collega meccanica, metabolismo e controllo genico nella guarigione delle ferite. Mostrando come il lattato derivato dai macrofagi, trasportato tramite MCT1, modifichi gli istoni e attivi un programma di cicatrizzazione auto-rinforzante nei fibroblasti, lo studio evidenzia diversi bersagli terapeutici promettenti. Farmaci che modulano la produzione di lattato, bloccano MCT1 o interferiscono con la specifica modificazione istonica potrebbero un giorno aiutare le ferite a guarire più rapidamente con cicatrici più piatte e meno visibili.
Citazione: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
Parole chiave: cicatrice ipertrofica, segnalazione del lattato, crosstalk macrofago–fibroblasto, lattilazione degli istoni, terapia della guarigione delle ferite