Clear Sky Science · it
La mioferlina è un componente delle vescicole di trafficking vRNP in fase avanzata per virus a RNA con involucro
Perché questo è importante per la salute quotidiana
L'influenza stagionale e altre infezioni respiratorie possono sembrare un problema di routine, ma insieme uccidono milioni di persone ogni anno in tutto il mondo. Molti di questi virus, inclusi l'influenza A e il virus respiratorio sinciziale (RSV), eludono già vaccini e antivirali mutando rapidamente. Questo studio invece guarda a qualcosa che i virus non possono facilmente cambiare: la macchina cellulare umana che sfruttano per uscire dalle cellule infette. Svelando un punto debole condiviso in questa macchina, il lavoro indica la strada verso futuri farmaci che potrebbero attenuare contemporaneamente un'ampia gamma di virus respiratori.
Una via di consegna cellulare sfruttata dai virus
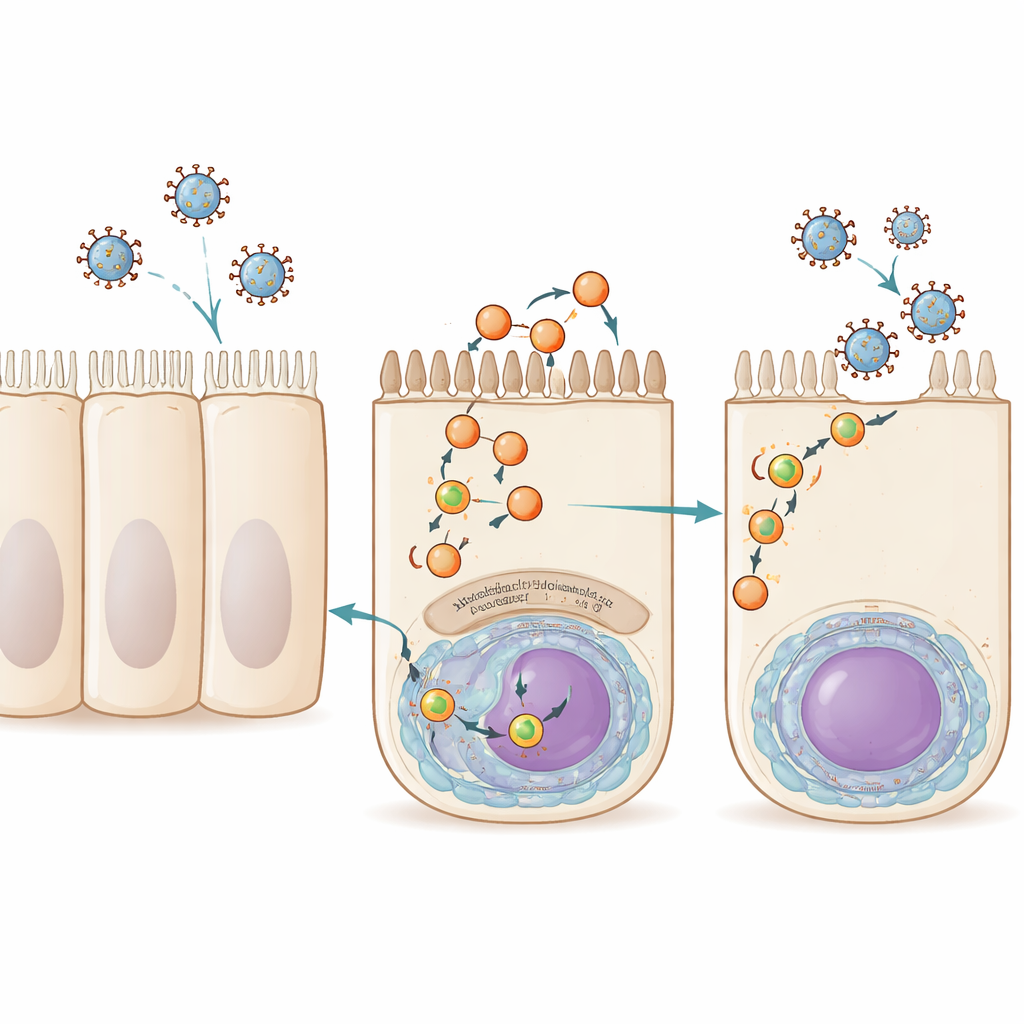
Le cellule delle nostre vie respiratorie riciclano continuamente porzioni della loro membrana esterna tramite un processo chiamato riciclaggio. Piccole bolle di membrana, o vescicole, trasportano carico dall'interno della cellula verso la superficie, guidate da una famiglia di proteine note collettivamente come Rab11. Il virus dell'influenza A, l'RSV e un virus correlato chiamato virus di Sendai sfruttano tutti questa via nelle fasi avanzate dell'infezione. Caricano il loro materiale genetico, impacchettato in complessi ribonucleoproteici, su vescicole contenenti Rab11 che li portano al lato superiore (rivolto alle vie aeree) della cellula, dove nuove particelle virali gemmano e si diffondono. Finora Rab11 era l'unico fattore ospite chiaramente condiviso da queste vescicole di trafficking, lasciando una grande lacuna nella nostra comprensione di come si formano e funzionano.
Scoprire un nuovo attore: la mioferlina
I ricercatori hanno cominciato chiedendosi quali proteine umane si associano fisicamente con la macchina di impacchettamento del genoma dell'influenza in diversi momenti dell'infezione. Hanno ingegnerizzato un virus dell'influenza A il cui polimerasi portava un tag molecolare, quindi hanno usato la spettrometria di massa per catalogare le proteine umane legate a questo complesso in fase precoce e tardiva dell'infezione. Tra centinaia di candidati, una si è distinta nei tempi tardivi: la mioferlina, una grande proteina associata alla membrana precedentemente collegata allo sviluppo muscolare, all'endocitosi e alla riparazione della membrana. Quando il team ha ridotto i livelli di mioferlina in cellule derivate dal polmone usando piccoli RNA interferenti o l'ha bloccata con un inibitore small-molecule, le cellule producevano comunque RNA virale e proteine virali normalmente, ma rilasciavano molte meno particelle influenzali infettive. Questo indicava che la mioferlina non è necessaria per la copia del genoma virale, ma è cruciale per le fasi successive quando i nuovi virus vengono assemblati ed escono dalla cellula.
La mioferlina viaggia con il carico virale
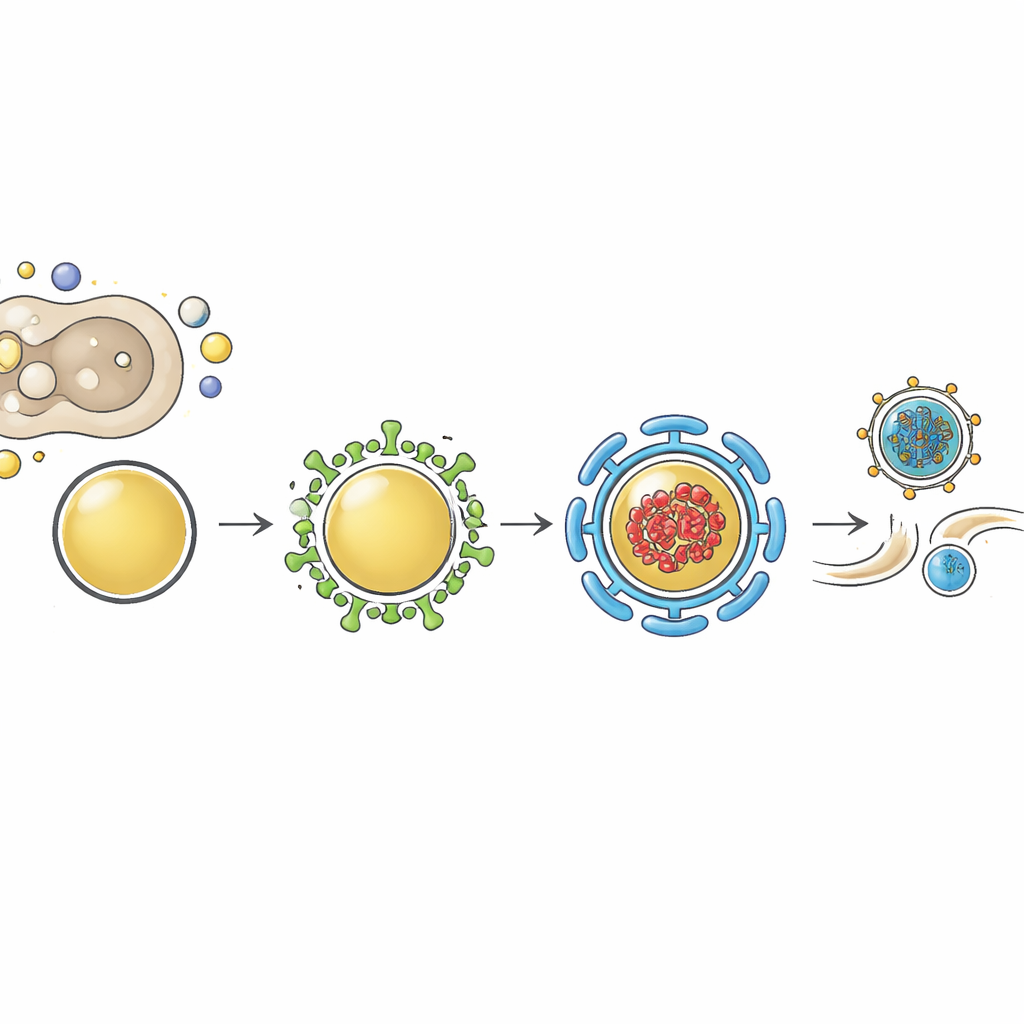
L'imaging ad alta risoluzione ha rivelato dove si trova la mioferlina durante l'infezione. Nelle cellule non infette, la mioferlina si sovrappone in gran parte alle vescicole di riciclaggio positive per Rab11, sia vicino al nucleo sia verso il bordo della cellula, e la perdita di una o dell'altra proteina altera la distribuzione normale dell'altra. Durante l'infezione da influenza, la rete di Rab11 viene rimodellata in modo drammatico in vescicole ingrandite e irregolari che trasportano i ribonucleoproteine virali. La mioferlina è mantenuta in queste vescicole rimodellate e mostra una forte colocalizzazione con il genoma virale e Rab11. Quando il team ha usato un farmaco che costringe i complessi del genoma virale e le loro vescicole portatrici ad aggregarsi, la mioferlina è stata trascinata negli stessi aggregati, confermando che è un componente intrinseco di queste strutture di trafficking in fase avanzata e non solo un semplice vicino occasionale.
Un hub condiviso per più virus respiratori
Lo studio ha poi chiesto se questa dipendenza dalla mioferlina sia unica per l'influenza o più ampiamente condivisa. Ridurre la mioferlina in cellule polmonari infettate con RSV o virus di Sendai ha nuovamente causato un forte calo delle particelle infettive rilasciate, senza ridurre i livelli di RNA virale. L'imaging a singola molecola ha mostrato i genomi di entrambi i virus raggruppati insieme con la mioferlina e Rab11 in punti citoplasmatici che probabilmente rappresentano hub di trasporto piuttosto che fabbriche di replicazione. Questo schema supporta un quadro unificante: diversi virus respiratori a RNA con involucro, nonostante stili di vita diversi, convergono sullo stesso sistema di vescicole Rab11–mioferlina quando è il momento di spostare i loro genomi completati verso la superficie cellulare per l'impacchettamento e l'uscita.
Come la mioferlina modella le vescicole che trasportano i virus
La mioferlina è composta da molteplici domini «C2» che possono legare membrane e proteine partner. Lavori precedenti avevano mostrato che uno di questi domini coinvolge una famiglia di proteine rimodellanti la membrana chiamate EHD. In questo studio, EHD1 ed EHD2 marcati fluorescentemente sono stati trovati all'interno delle stesse vescicole rimodellate che trasportano i genomi dell'influenza e Rab11, soprattutto quando queste vescicole venivano sperimentalmente aggregate. Ridurre i livelli di EHD2, come ridurre la mioferlina, ha abbassato i rendimenti dell'influenza senza influire sulla replicazione del genoma. Inoltre, la rimozione della mioferlina ha fatto diminuire i livelli proteici di EHD2, suggerendo che la mioferlina aiuta a stabilizzare o posizionare correttamente EHD2 sulle membrane. Gli autori propongono che la mioferlina si trovi sulle vescicole positive per Rab11 e recluti proteine EHD per scolpire le loro membrane, completando la formazione di «vesicole rivestite irregolarmente» specializzate ottimizzate per trasportare il carico virale verso i siti di gemmazione.
Cosa significa per le future strategie antivirali
Nel complesso, i risultati pongono la mioferlina come organizzatore centrale di una via di riciclaggio dell'ospite su cui molti virus respiratori con involucro fanno affidamento in un passaggio critico finale. Poiché mirare solo alle proteine virali spesso porta a resistenza rapida, i fattori dell'ospite riutilizzati da più virus rappresentano bersagli farmacologici attraenti. Interferire con la funzione della mioferlina, o con la sua partnership con Rab11 e le proteine EHD, potrebbe in principio rallentare o bloccare la diffusione di patogeni diversi, dall'influenza e l'RSV ad altri virus dipendenti da Rab11 come alcuni coronavirus. Rimane molto lavoro per tradurre questo concetto in terapie sicure, ma lo studio fornisce una mappa dettagliata di una via di fuga virale condivisa—e mette in luce la mioferlina come un promettente punto di strozzatura lungo quel percorso.
Citazione: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Parole chiave: influenza, virus respiratori, traffico vescicolare, fattori dell'ospite, mioferlina