Clear Sky Science · it
Difetti strutturali nei fibrille di amiloide-β guidano la nucleazione secondaria
Perché piccole imperfezioni nelle proteine cerebrali contano
Nell’Alzheimer e in malattie cerebrali correlate, certe proteine si aggregano in strutture lunghe e filamentose chiamate fibrille amiloidi. Queste fibrille non solo sono un segno della malattia; favoriscono anche la formazione di nuove particelle proteiche altamente tossiche che possono danneggiare le cellule cerebrali. Questo studio pone una domanda semplice ma cruciale: difetti strutturali rari all’interno delle fibrille amiloidi fungono da principali punti caldi che innescano una nuova crescita dannosa? La risposta potrebbe indicare nuovi modi per rallentare o fermare questi disturbi colpendo solo pochi siti critici invece dell’intera superficie proteica. 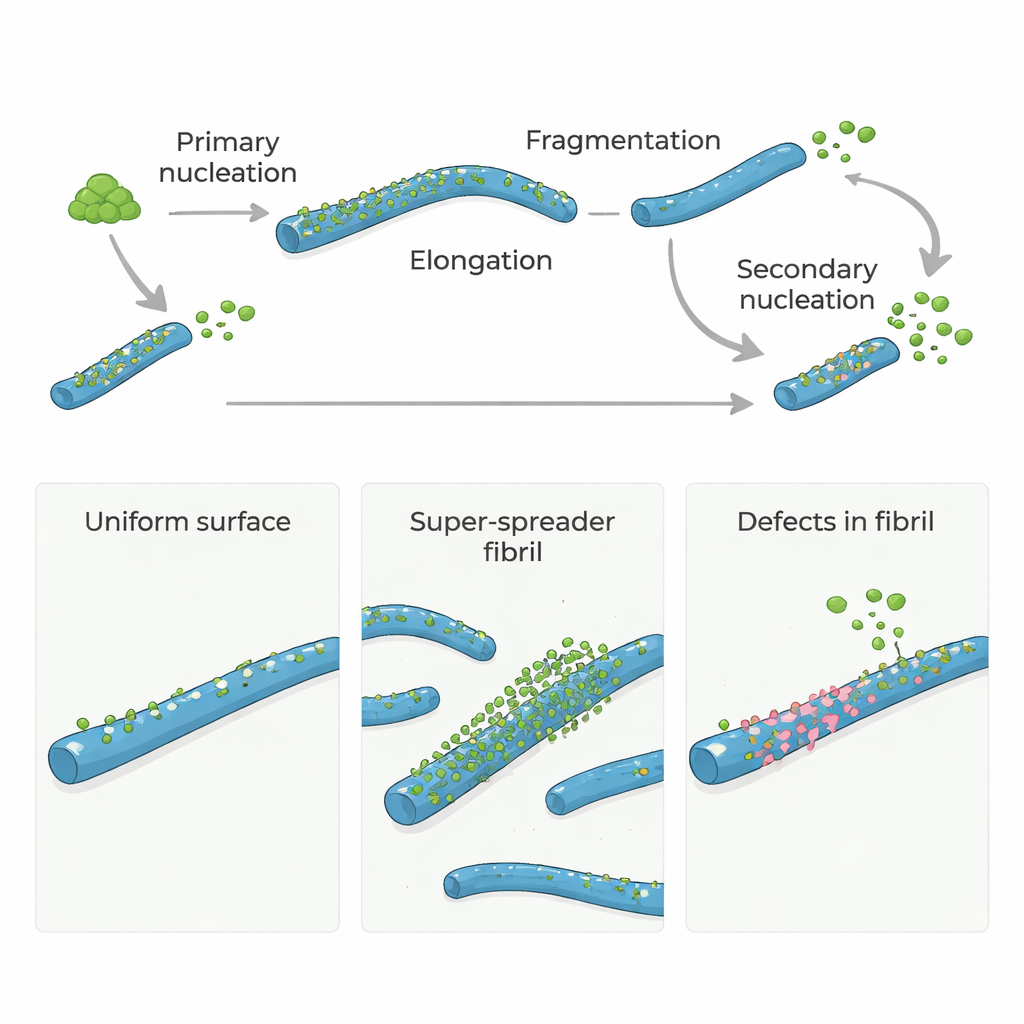
Da una proteina silenziosa a una reazione a catena incontrollata
Le proteine amiloide-β (Aβ), centrali nella malattia di Alzheimer, normalmente non formano aggregati molto rapidamente da sole. Per iniziare, alcuni monomeri devono assemblarsi lentamente nelle prime fibrille microscopiche, un passaggio chiamato nucleazione primaria. Una volta presenti queste fibrille iniziali, crescono rapidamente mentre altri monomeri si aggiungono alle loro estremità. Ancora più importante, fibrille esistenti possono indurre la comparsa di nuove fibrille sulle loro superfici in un processo noto come nucleazione secondaria. Questo passaggio guidato dalla superficie può inondare il sistema di nuove fibrille e di piccoli oligomeri tossici, trasformando un flusso lento in una reazione a catena fuori controllo.
Tutte le superfici delle fibrille sono altrettanto pericolose?
Molti modelli hanno supposto che l’intera superficie di una fibrilla amiloide sia ugualmente efficace nel catalizzare la nucleazione secondaria. Tuttavia, esperimenti recenti hanno suggerito che solo una piccola frazione della superficie è davvero attiva. Per investigare questo, gli autori hanno usato un «chaperone» molecolare naturale chiamato Brichos, noto per bloccare la nucleazione secondaria di Aβ40 e Aβ42 (due forme chiave di amiloide-β). Misurando con cura quanto Brichos marcato con fluorescenza si lega alle fibrille, hanno rilevato che si lega saldamente ma in numeri molto bassi: circa una molecola di Brichos ogni 100–150 molecole di Aβ in una fibrilla. Eppure questa copertura sparsa è stata sufficiente a sopprimere oltre il 90% della nucleazione secondaria, il che significa che solo siti rari e localizzati — più che l’intera superficie — dominano la produzione di nuovi assemblati tossici.
Indagare il ruolo dei difetti nascosti
Questi risultati suggerivano che i siti cruciali di nucleazione potrebbero essere difetti strutturali — piccole irregolarità formate durante la crescita delle fibrille, come strati disallineati o core interni parzialmente esposti. Per testare direttamente questa idea, i ricercatori hanno coltivato fibrille di Aβ40 in due condizioni diverse. Un gruppo, le fibrille «controllo», è stato formato in condizioni tipiche fortemente sovrasature che favoriscono una crescita rapida e l’intrappolamento cinetico di difetti. L’altro gruppo è stato creato usando un protocollo di ricottura a temperatura controllata: le fibrille sono state fatte crescere con una forza motrice effettiva molto bassa, vicino al loro limite di solubilità, dove le strutture incorrette possono dissolversi o ripararsi prima di solidificarsi. La crio-microscopia elettronica ad alta risoluzione ha mostrato che entrambi i gruppi di fibrille apparivano essenzialmente identici nella forma generale e nella torsione, indicando che il processo di ricottura non ha cambiato la morfologia di base. 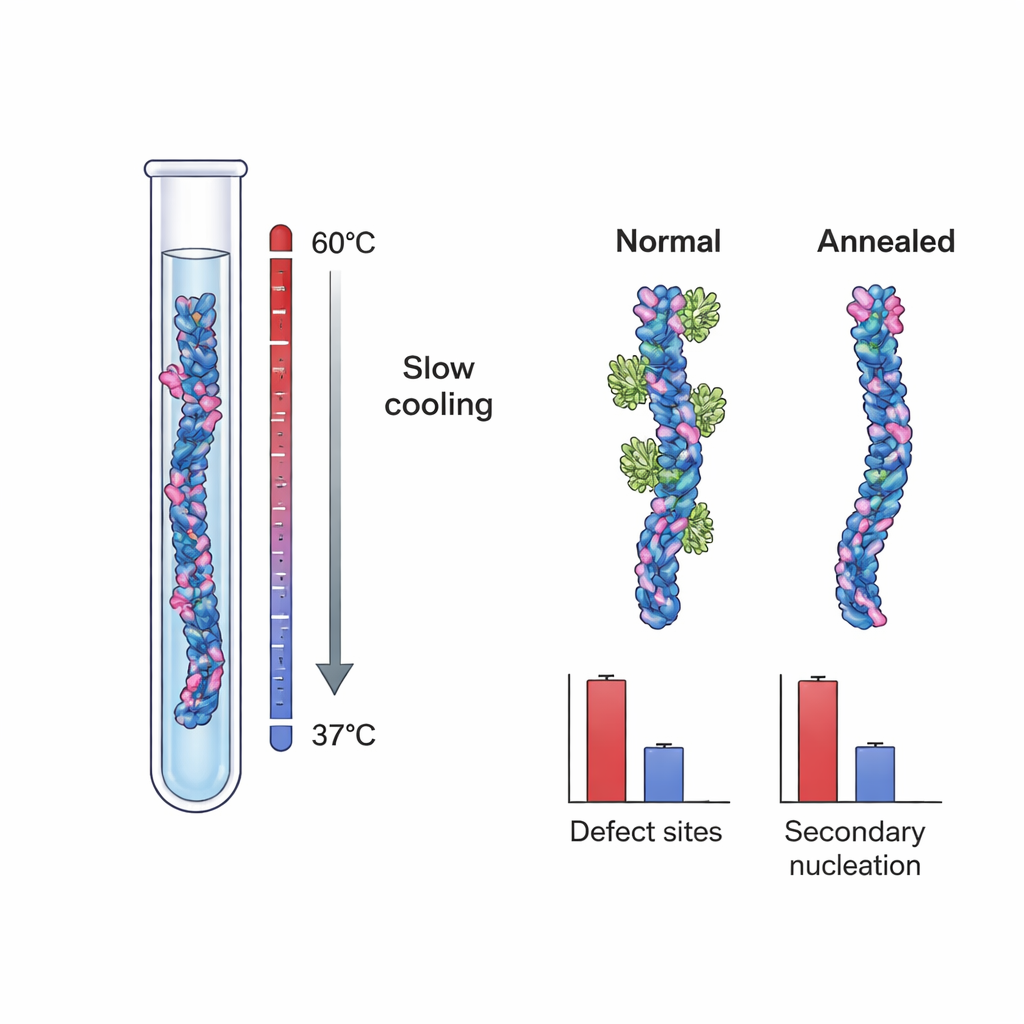
Meno difetti, meno siti di crescita pericolosi
Quando il team ha misurato il legame di Brichos a questi due tipi di fibrille, ha scoperto una differenza sorprendente. Le fibrille di controllo Aβ40 avevano circa un sito di legame per Brichos ogni ~100 monomeri, indicando ancora siti rari ma importanti. Le fibrille ricotte, invece, avevano solo circa un sito ogni ~800 monomeri — una riduzione della frequenza dei siti di quasi il 90%. In test separati in cui queste fibrille venivano aggiunte come «semi» a soluzioni fresche di Aβ40, le fibrille ricotte erano molto meno efficaci nell’innescare nuova aggregazione, anche quando la loro massa totale era bilanciata con quella delle fibrille di controllo. La modellizzazione cinetica dettagliata ha mostrato che questa diminuzione della potenza di semina non poteva essere spiegata semplicemente da differenze nella lunghezza delle fibrille. Al contrario, coincideva quantitativamente con il numero ridotto di siti di legame per Brichos, supportando con forza l’idea che i difetti di crescita agiscano come i principali motori della nucleazione secondaria.
Un principio generale con potenziale terapeutico
Combinando argomentazioni termodinamiche, una rianalisi di lavori precedenti e confronti tra diverse proteine che formano amiloidi, gli autori sostengono che i difetti di crescita rari sono probabilmente centrali per la nucleazione secondaria in molti sistemi, non solo per l’Aβ legato all’Alzheimer. Questi difetti espongono parzialmente il nucleo interno strettamente impacchettato della fibrilla, offrendo un’impalcatura pronta dove nuovi oligomeri e fibrille possono formarsi molto più facilmente rispetto a una superficie liscia. Riconoscere questi difetti come i colpevoli chiave apre nuove strade per la progettazione di farmaci. Invece di tentare di bloccare ogni possibile interazione sulla superficie di una fibrilla, le terapie potrebbero mirare a schermare o riparare solo questi scarsi siti difettosi, o a ridurre le condizioni che li generano. In termini pratici, ciò potrebbe significare abbassare la concentrazione effettiva di proteine amiloidogeniche nel cervello o progettare molecole, ispirate al Brichos, che riconoscano e neutralizzino i punti caldi di nucleazione guidata da difetti. Se avessero successo, tali strategie potrebbero tagliare la principale fonte di oligomeri tossici e rallentare la progressione delle malattie legate all’amiloide.
Citazione: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Parole chiave: fibrille amiloidi, morbo di Alzheimer, nucleazione secondaria, aggregazione proteica, chaperone Brichos