Clear Sky Science · it
L'esaurimento di ossigeno nei condensati biomolecolari è dominato dalla densità macromolecolare
Tasche invisibili all’interno delle cellule viventi
All’interno delle nostre cellule molte reazioni chimiche dipendono da un apporto costante di ossigeno. Ma le cellule non sono semplici sacche di liquido: contengono minuscoli compartimenti a forma di goccia, chiamati condensati biomolecolari, che si formano senza membrane. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: queste gocce modificano la quantità di ossigeno disponibile in diverse parti della cellula e, in tal caso, perché? La risposta mette in discussione le idee correnti sul comportamento delle piccole molecole in questi microambienti affollati.

Gocce senza pareti
I condensati biomolecolari sono aggregati morbidi e dalle proprietà liquide di proteine e acidi nucleici che si assemblano e si dissolvono su richiesta. Organizzano la biochimica concentrando alcune molecole ed escludendone altre, pur non avendo una membrana che li circondi. Studi precedenti hanno mostrato che molti piccoli metaboliti e composti simili a farmaci vengono attratti all’interno di queste gocce, tipicamente perché l’interno si comporta un po’ come un solvente oleoso rispetto al fluido acquoso della cellula. L’ossigeno, tuttavia, è un caso speciale: è una piccola molecola gassosa che alimenta la respirazione ma può anche promuovere reazioni secondarie dannose. Se i condensati arricchiscono o riducono l’ossigeno potrebbe quindi influenzare l’efficienza degli enzimi e l’entità dei danni ossidativi vicino o all’interno di queste gocce.
Misurare l’ossigeno in compartimenti minuscoli
Per sondare i livelli di ossigeno all’interno dei condensati, i ricercatori hanno costruito un sistema modello semplice ma regolabile usando proteine di progettazione flessibili che formano facilmente gocce in soluzione salina. Hanno prima creato fasi macroscopiche grandi facendo ruotare i campioni in una centrifuga e poi hanno inserito microelettrodi elettrochimici sottilissimi per leggere direttamente le concentrazioni di ossigeno attraverso il confine tra la fase ricca di proteine e quella povera. Queste misure hanno rivelato che i livelli di ossigeno diminuiscono quando la sonda entra nella fase densa di proteine: le gocce escludono parzialmente l’ossigeno anziché assorbirlo.
Illuminare l’ossigeno con coloranti speciali
Poiché gli elettrodi disturbano le piccole gocce, il gruppo ha utilizzato la microscopia a imaging della vita di fosforescenze, un metodo ottico che impiega coloranti speciali la cui emissione dura meno quando è presente più ossigeno. Monitorando il tempo di emissione dentro e fuori singole gocce, e correggendo con attenzione come l’ambiente della goccia altera il comportamento di base del colorante, hanno potuto inferire le concentrazioni di ossigeno senza disturbare fisicamente i condensati. In un’ampia gamma di condizioni, i dati ottici concordavano con le misure elettrochimiche: l’ossigeno è costantemente più basso all’interno dei condensati rispetto alla soluzione circostante. Simulazioni al calcolatore con un modello molecolare a grana grossa hanno supportato questo quadro, mostrando che l’ossigeno trascorre relativamente poco tempo nelle regioni proteiche dense.
La densità, non la “untuosità”, determina i livelli di ossigeno
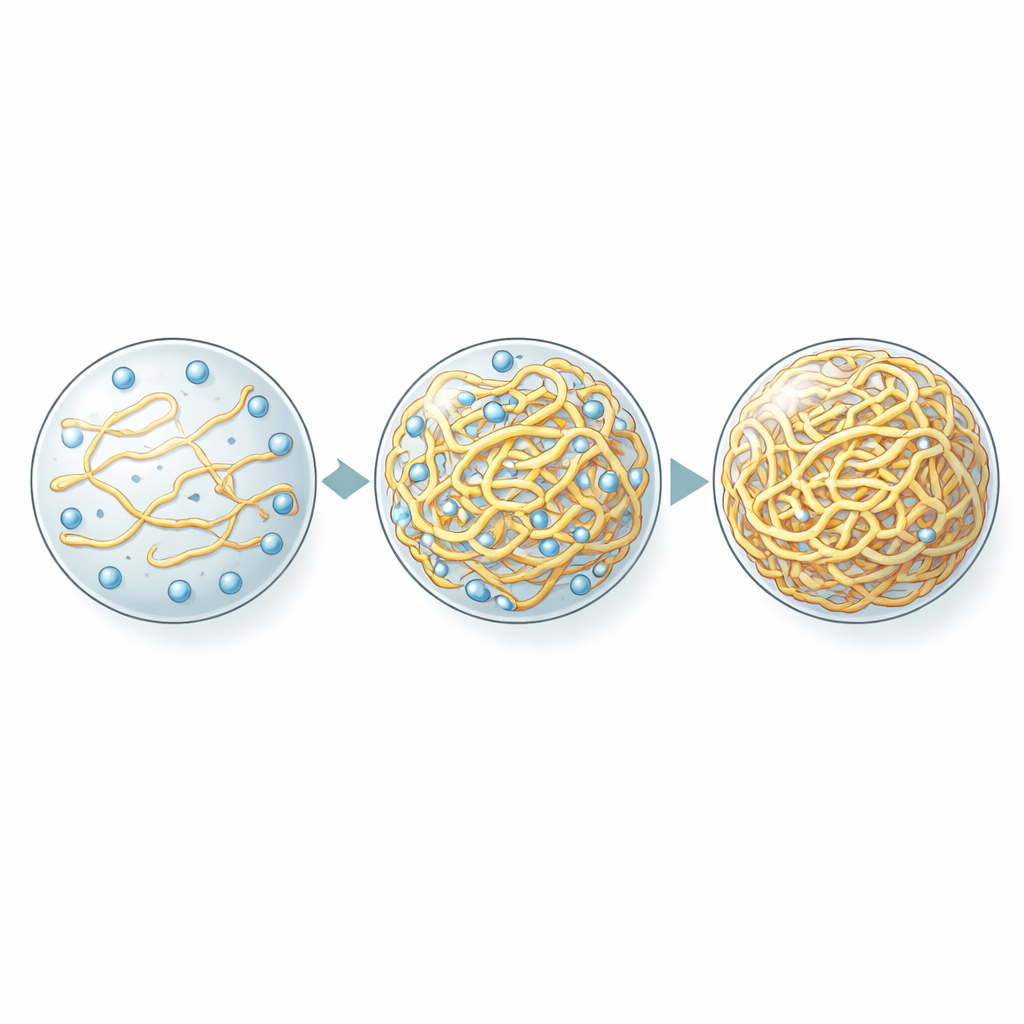
Il sospetto più ovvio per il controllo dell’assorbimento di ossigeno è l’idrofobicità — la «untuosità» dell’interno della goccia — che era stata precedentemente identificata come il fattore chiave per come molte altre piccole molecole si partizionano nei condensati. Per testare ciò, gli autori hanno modificato sistematicamente le sequenze proteiche per cambiare sia il numero di unità ripetute sia il carattere idrofobico, poi hanno misurato l’ossigeno nelle gocce risultanti. Sorprendentemente, i livelli di ossigeno non seguivano l’andamento dell’essere più oleoso o acquoso. Al contrario, essi correlarono fortemente e inversamente con la quantità di proteina impaccata nella fase densa. Varianti che formavano condensati più affollati trattenevano meno ossigeno, anche quando nel complesso risultavano meno idrofobiche. Altri piccoli coloranti oleosi si comportavano diversamente: continuavano a preferire gocce più idrofobiche, confermando che l’ossigeno rompeva le regole abituali.
Nuova prospettiva sui gradienti di ossigeno a nanoscale
Questi risultati portano a una visione riveduta di come i condensati modellano il loro ambiente chimico. Per le piccole molecole che non aderiscono fortemente alle proteine impalcatura, la semplice densità delle macromolecole diventa il fattore dominante: più volume occupano le proteine, meno spazio rimane per l’ossigeno disciolto. Ciò significa che le cellule possono generare gradienti di ossigeno su distanze da nanometri a micrometri semplicemente formando o dissolvendo condensati, o modificando quanto sono strettamente impaccate queste gocce. In termini pratici, il lavoro suggerisce che gli organelli senza membrana possono modulare sottilmente la disponibilità di ossigeno per reazioni vicine — potenzialmente accelerando alcune, rallentandone altre o proteggendo componenti sensibili — tramite un effetto fisico di affollamento piuttosto che attraverso legami chimici specifici.
Citazione: Garg, A., Brasnett, C., Marrink, S.J. et al. Oxygen depletion in biomolecular condensates is dominated by macromolecular density. Nat Commun 17, 2603 (2026). https://doi.org/10.1038/s41467-026-69376-2
Parole chiave: condensati biomolecolari, partizionamento dell'ossigeno, affollamento macromolecolare, separazione di fase, microambienti cellulari