Clear Sky Science · it
Meccanismo di roaming modulato dal solvente in bromoformio rivelato da scattering X a femtosecondi in soluzione
Perché molecole piccole in acqua e aria sono importanti
Il bromoformio è una piccola sostanza prodotta naturalmente che ha un grande impatto ambientale. Quando la luce solare colpisce questa molecola nell’atmosfera o negli spruzzi oceanici, può rilasciare atomi di bromo che contribuiscono alla distruzione dell’ozono, lo scudo che ci protegge dai raggi ultravioletti dannosi del Sole. Questo studio pone una domanda apparentemente semplice ma di vasta portata: l’ambiente liquido che circonda il bromoformio cambia ciò che accade nei primi bilionesimi di secondo dopo l’irraggiamento, e quindi modifica la quantità di bromo che alla fine contribuisce all’azione distruttiva sull’ozono?
La luce che spezza una molecola
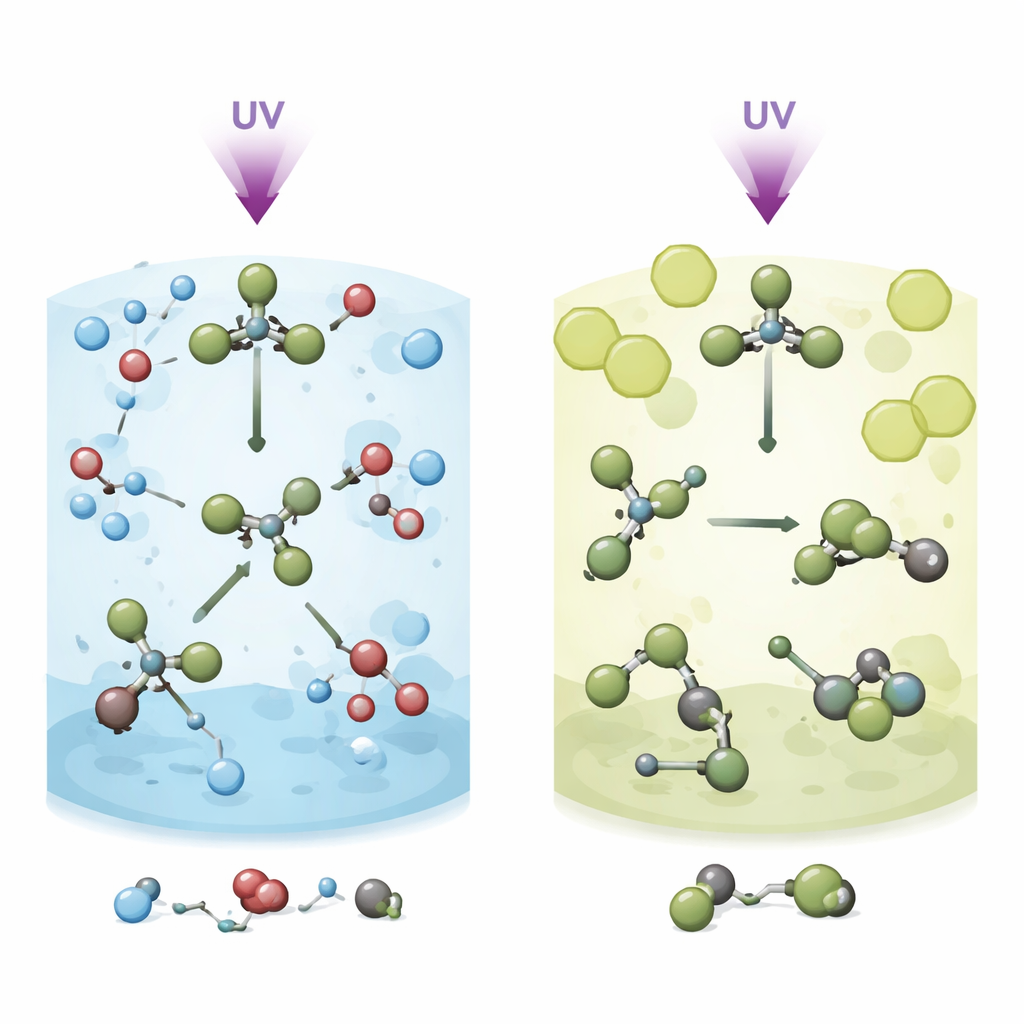
I ricercatori iniziano irraggiando il bromoformio disciolto in due liquidi diversi con impulsi estremamente brevi di luce ultravioletta: metanolo, che è polare e chimicamente reattivo, e metilcicloesano, che è apolare e relativamente inerte. La luce indebolisce rapidamente uno dei legami carbonio–bromo del bromoformio, facendo sì che la molecola inizi a disfarsi. Ma invece di allontanarsi semplicemente, un atomo di bromo rimane a lungo nelle vicinanze e “ronza” attorno al frammento rimanente, CHBr2. Questo moto di roaming crea una forma fugace e riorganizzata chiamata isomero. Il nodo centrale è cosa succede a questo intermedio di roaming nei diversi solventi e come quella scelta controlli se il bromoformio rilascia atomi di bromo liberi o viene deviato verso altri prodotti.
Fare film molecolari con raggi X
Per osservare questi eventi, il gruppo usa scattering X a risoluzione temporale femtosecondo presso l’European X‑ray Free‑electron Laser. In sostanza registrano un film a luce stroboscopica di come cambiano le distanze interatomiche in tempo reale, con risoluzione sia a scala di picosecondi sia sub‑picosecondi. Confrontando i pattern di scattering misurati con pattern generati al computer per molte strutture possibili, ricostruiscono come lunghezze di legame e angoli all’interno del bromoformio evolvono dopo l’eccitazione. Tecniche avanzate di analisi e simulazioni accelerate dal machine learning aiutano a separare percorsi di reazione sovrapposti e ad assegnare durate precise a specie di vita breve.
Due solventi, due destini molto diversi
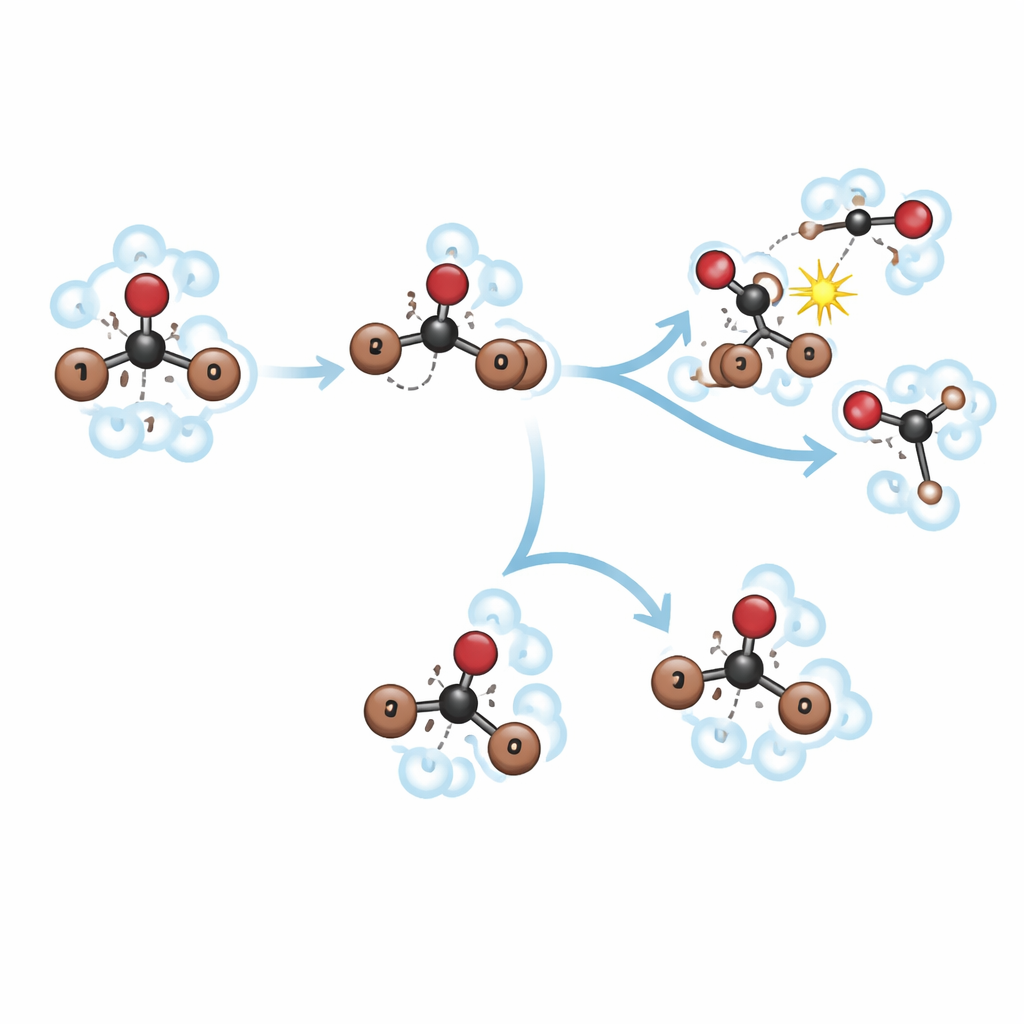
Nel metanolo l’intermedio di roaming è presente ma di breve durata. Nel giro di circa 150 femtosecondi il legame carbonio–bromo iniziale si rompe, formando CHBr2 e un bromo in roaming. Nei successivi ~400 femtosecondi questo isomero caldo e vibrante si allunga e si piega ripetutamente, portando i frammenti a frequenti contatti con le molecole di metanolo vicine. Invece di stabilizzarsi in una forma riorganizzata stabile, la struttura in roaming viene rapidamente intercettata dal metanolo in una reazione di “metanolisi”. Questo produce nuove molecole, CH3OCHBr2 e HBr, mentre frammenti liberi CHBr2 e Br provenienti da una via di dissociazione parallela e più diretta continuano a reagire più lentamente nell’arco di alcuni picosecondi. La stretta “gabbia” molecolare del solvente e i suoi gruppi ossidrilici reattivi agiscono insieme per indirizzare il bromoformio lungo questa via di reazione chimica piuttosto che verso un isomero di lunga vita.
Quando il liquido si ritrae e lascia continuare il roaming
Nel metilcicloesano la storia cambia in modo drammatico. Lo stesso impulso ultravioletto crea ancora il moto di roaming nell’ordine di 150 femtosecondi, ma il liquido apolare circonda il bromoformio più sciolto e non reagisce facilmente con esso. Qui il bromo in roaming e il frammento CHBr2 hanno spazio per riorientarsi e stabilizzarsi in una struttura isomerica invece di interagire immediatamente con le molecole del solvente. La dissociazione diretta in frammenti separati CHBr2 e Br continua a verificarsi e compete con la formazione dell’isomero, ma ora l’isomero riorganizzato sopravvive per tempi molto più lunghi. Le simulazioni mostrano che la gabbia del solvente più grande e più morbida nel metilcicloesano favorisce questo comportamento di roaming simile al gas, mentre la gabbia angusta e fortemente interagente del metanolo convoglia lo stesso intermedio direttamente verso la reazione chimica.
Cosa significa per l’ozono e oltre
Complessivamente, questi esperimenti e calcoli rivelano che il roaming è un passo iniziale universale quando il bromoformio assorbe luce ultravioletta in ambienti liquidi, ma è il solvente circostante a decidere cosa succede dopo. In contesti simili al metanolo il roaming serve principalmente a guidare reazioni rapidissime con il liquido, limitando la formazione di isomeri di lunga vita e influenzando come e quando compaiono prodotti contenenti bromo. In ambienti simili al metilcicloesano, il roaming invece alimenta una forma riorganizzata di lunga durata che può poi rilasciare bromo su scale temporali diverse. Filmando direttamente questi moti ultrarapidi, il lavoro mostra che il carattere microscopico delle goccioline, degli aerosol e di altri ambienti in fase condensata può controllare fortemente i percorsi chimici di molecole rilevanti per l’ozono, aiutando gli scienziati a costruire modelli più accurati della fotochimica atmosferica e in soluzione.
Citazione: Su, P., Zhang, J., Wang, H. et al. Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering. Nat Commun 17, 2514 (2026). https://doi.org/10.1038/s41467-026-69374-4
Parole chiave: bromoformio, meccanismo di roaming, fotochimica ultrarapida, effetti del solvente, deplezione dello strato di ozono