Clear Sky Science · it
Ordini concorrenti di legami a idrogeno guidano l’anomala tensione superficiale dell’acqua
Perché la superficie dell’acqua è più strana di quanto sembri
La superficie dell’acqua permette agli insetti di camminare sulle pozze, determina la forma delle gocce di pioggia e controlla come si formano e scoppiano le bolle. Eppure, quando gli scienziati misurano quanto “stretta” sia quella superficie — la tensione superficiale — scoprono che l’acqua si comporta in modo sorprendentemente anomalo man mano che si raffredda, soprattutto quando viene portata sotto il suo punto di congelamento normale. Questo articolo utilizza avanzate simulazioni al computer per rivelare come l’organizzazione nascosta delle molecole d’acqua alla superficie spieghi questo mistero di lunga data.
Due tipi nascosti di acqua liquida
Pur sperimentando l’acqua come un liquido semplice e uniforme, le sue molecole possono disporsi localmente in due modi contrastanti. Una disposizione è più affollata e disordinata; gli autori la chiamano stato ρ. L’altra è più aperta e simmetrica, con ogni molecola circondata in una configurazione approssimativamente tetraedrica a quattro legami; questa è chiamata stato S. Lavori precedenti suggerivano che l’equilibrio tra questi due schemi locali aiuti a spiegare molte delle proprietà anomale dell’acqua allo stato bulk. Qui gli autori chiedono come questa stessa immagine a due stati si manifesti all’interfaccia aria–acqua, dove nasce la tensione superficiale.
Come la superficie allinea le molecole
Al confine tra aria e acqua, le molecole non percepiscono più forze uguali in tutte le direzioni. Questa rottura della simmetria favorisce le molecole in stato ρ i cui atomi di idrogeno e i dipoli molecolari possono facilmente inclinersì in una direzione preferenziale. Le simulazioni mostrano che vicino alla temperatura ambiente e leggermente al di sotto, lo strato più superficiale dell’acqua diventa popolato da queste molecole ρ allineate, mentre le molecole in stato S sono più comuni appena sotto la superficie e nel volume. Poiché le molecole ρ si dispongono fortemente in linea, generano uno squilibrio di forze — un’anisotropia degli stress — che produce una tensione superficiale relativamente elevata rispetto a liquidi ordinari come il benzene.
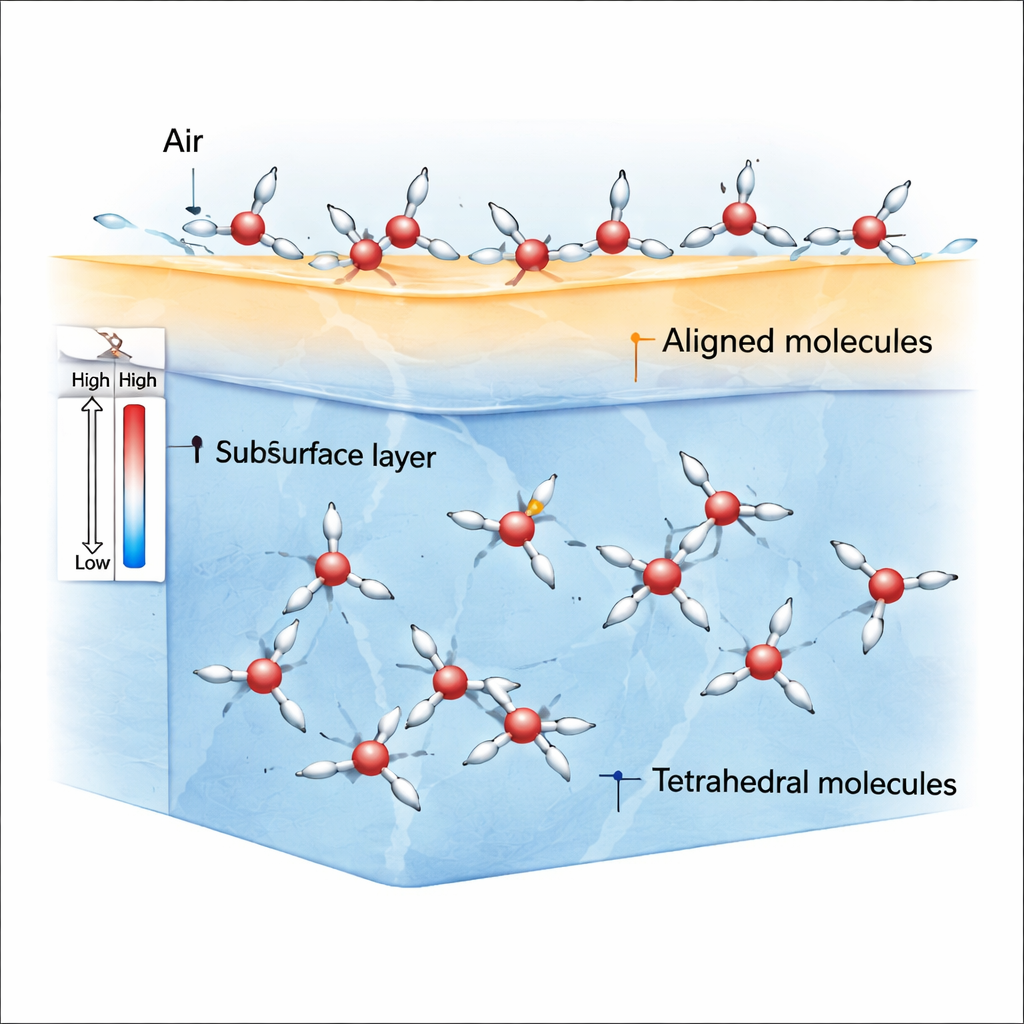
Perché il raffreddamento prima rallenta, poi accelera l’irrigidimento superficiale
Nella maggior parte dei liquidi semplici, il raffreddamento tende a irrigidire costantemente la superficie, facendo aumentare la tensione superficiale in modo quasi lineare. L’acqua segue questo comportamento solo a temperature più elevate. Avvicinandosi a circa –0,15 °C (275 K), l’aumento della tensione superficiale inizia a rallentare. Le simulazioni mostrano che questo rallentamento avviene perché le molecole ρ alla superficie hanno già raggiunto il massimo allineamento possibile; un ulteriore raffreddamento cambia poco il loro contributo. Allo stesso tempo, le molecole S nella sottosuperficie restano per lo più orientate in modo casuale, pertanto contribuiscono poco ad aumentare lo stress superficiale. Il risultato netto è una sorta di plateau: la temperatura continua a scendere, ma la tensione superficiale cresce soltanto lentamente.
Il profondo sopraraffreddamento scatena un secondo irrigidimento
Quando l’acqua viene raffreddata molto più a fondo, ben sotto il suo punto di congelamento in un regime di forte sopraraffreddamento (intorno a 250 K e al di sotto), il suo comportamento cambia di nuovo. La frazione di strutture tetraedriche dello stato S aumenta bruscamente, persino vicino alla superficie. Elemento cruciale, queste molecole S non sono più orientate in modo casuale. I loro dipoli cominciano ad allinearsi lungo la direzione perpendicolare alla superficie, guidati dalle interazioni tra dipoli molecolari vicini e da una regione di pressione negativa appena sotto la superficie. Quando ciò avviene, l’acqua in stato S, che prima aveva addolcito la tensione superficiale, comincia ora a rafforzarla. Questo contributo ordinato aggiuntivo produce un rinnovato e più rapido aumento — l’incremento “rientrante” — della tensione superficiale a basse temperature.
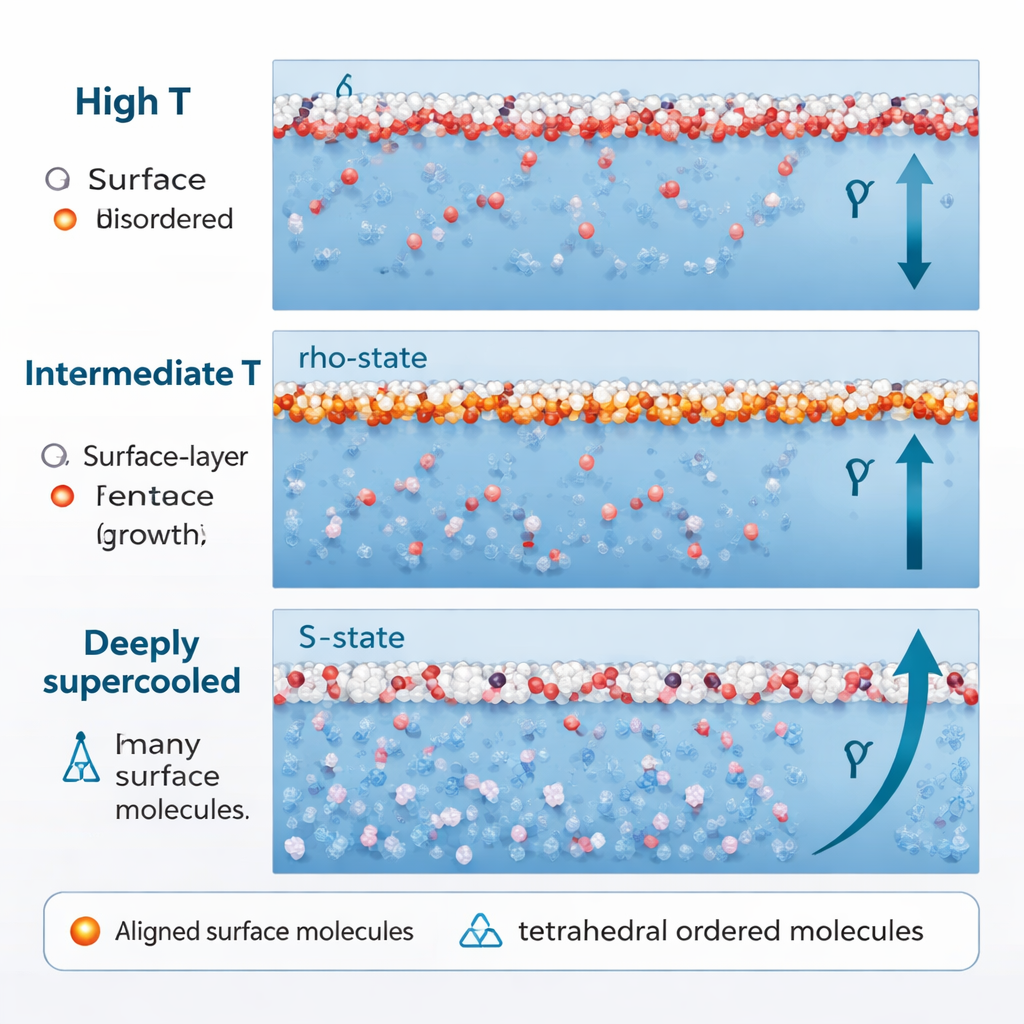
Dai rompicapi superficiali al ghiaccio e oltre
Gli stessi raggruppamenti tetraedrici dello stato S che irrigidiscono la superficie a basse temperature assomigliano anche ai primi mattoni di alcune forme di ghiaccio, e le simulazioni li rilevano arricchiti vicino all’interfaccia. Ciò significa che il confine aria–acqua può agire come culla per la formazione del ghiaccio, contribuendo a spiegare perché il congelamento spesso inizia alle superfici. Più in generale, il lavoro fornisce un legame concreto a livello molecolare tra come le molecole d’acqua si dispongono e si orientano e quanto intensamente la superficie tira verso l’interno. Questa visione strutturale–meccanica non solo risolve la strana curva della tensione superficiale dell’acqua in funzione della temperatura, ma offre anche una mappa per comprendere e controllare i fenomeni interfacciali in altri liquidi che formano reticoli, dal sopraraffreddamento dell’acqua nelle nubi ai materiali impiegati in tecnologia e biologia.
Citazione: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Parole chiave: tensione superficiale dell'acqua, legame a idrogeno, acqua soproraffreddata, struttura del liquido, nucleazione del ghiaccio