Clear Sky Science · it
STING sinergizza con TOX sopprimendo l’espressione di HO-1 per indurre ferroptosi nelle cellule CD8+ infiltranti il tumore e la resistenza all’immunoterapia
Perché questa ricerca è importante per il trattamento del cancro
Le immunoterapie oncologiche moderne funzionano liberando i linfociti T citotossici dell’organismo, eppure molti tumori riescono comunque a disattivare queste cellule. Questo studio svela un interruttore di autodistruzione nascosto all’interno dei linfociti CD8+ che i tumori sfruttano, e mostra come spegnere quell’interruttore possa rendere l’immunoterapia molto più efficace.
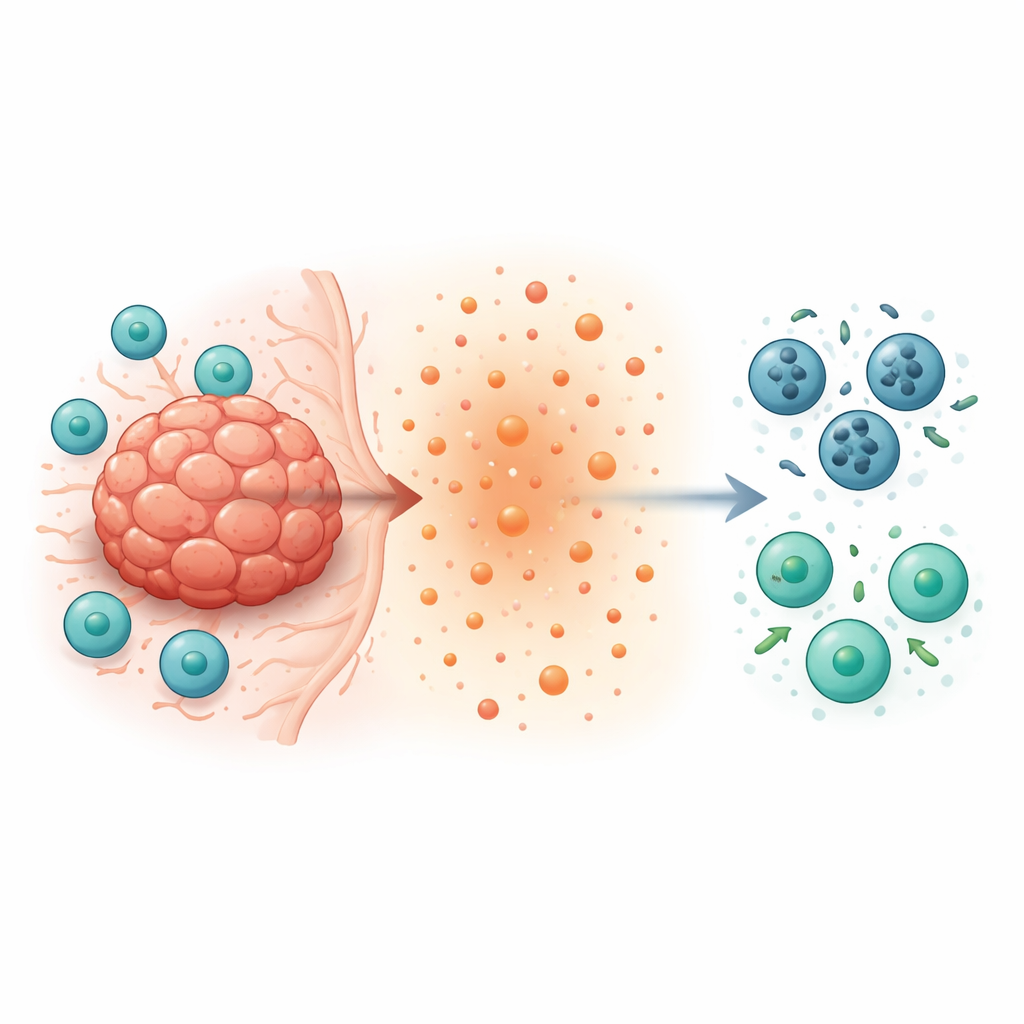
Una via della morte nascosta dentro i linfociti che combattono il tumore
All’interno di un tumore, i linfociti CD8+ dovrebbero cercare e distruggere le cellule tumorali. Invece spesso diventano scarsi, rallentati e di breve durata. Gli autori si sono concentrati su due molecole all’interno dei linfociti—STING, un sensore del danno al DNA, e TOX, una proteina associata all’esaurimento dei T cell. Hanno creato topi i cui linfociti CD8+ erano privi di STING, TOX o di entrambi, e poi hanno impiantato diversi tipi di tumori. Sorprendentemente, i topi i cui T cell erano privi di STING o di TOX eliminavano i tumori molto meglio. I loro tumori crescevano più lentamente, contenevano molti più CD8+ e questi producevano quantità maggiori di molecole citotossiche come l’interferone-gamma e la granzyme B. Ciò indicava l’esistenza di un programma interno che di nascosto sabota i T cell all’interno dei tumori.
Come la morte cellulare indotta dal ferro indebolisce l’immunità
Analizzando l’attività genica nei linfociti infiltranti il tumore, i ricercatori hanno scoperto che i T cell normali all’interno dei tumori erano predisposti a una forma particolare di morte cellulare chiamata ferroptosi. A differenza dell’apoptosi, la ferroptosi è scatenata dall’eccesso di ferro e dall’accumulo di lipidi ossidati nelle membrane cellulari. Nei normali CD8+ esposti a cellule tumorali, i geni che favoriscono l’accumulo di ferro e il danneggiamento lipidico risultavano attivati, mentre i geni protettivi erano abbassati. Al contrario, i T cell privi di STING o TOX mostravano il quadro opposto: esprimevano più enzimi protettivi come HO-1 e GPX4, avevano livelli di ferro più bassi, meno perossidazione lipidica, mitocondri più sani e resistevano alla ferroptosi. Test di laboratorio hanno confermato che bloccare chimicamente la ferroptosi manteneva vivi i T cell normali, mentre la rimozione di STING o TOX li rendeva naturalmente resistenti.
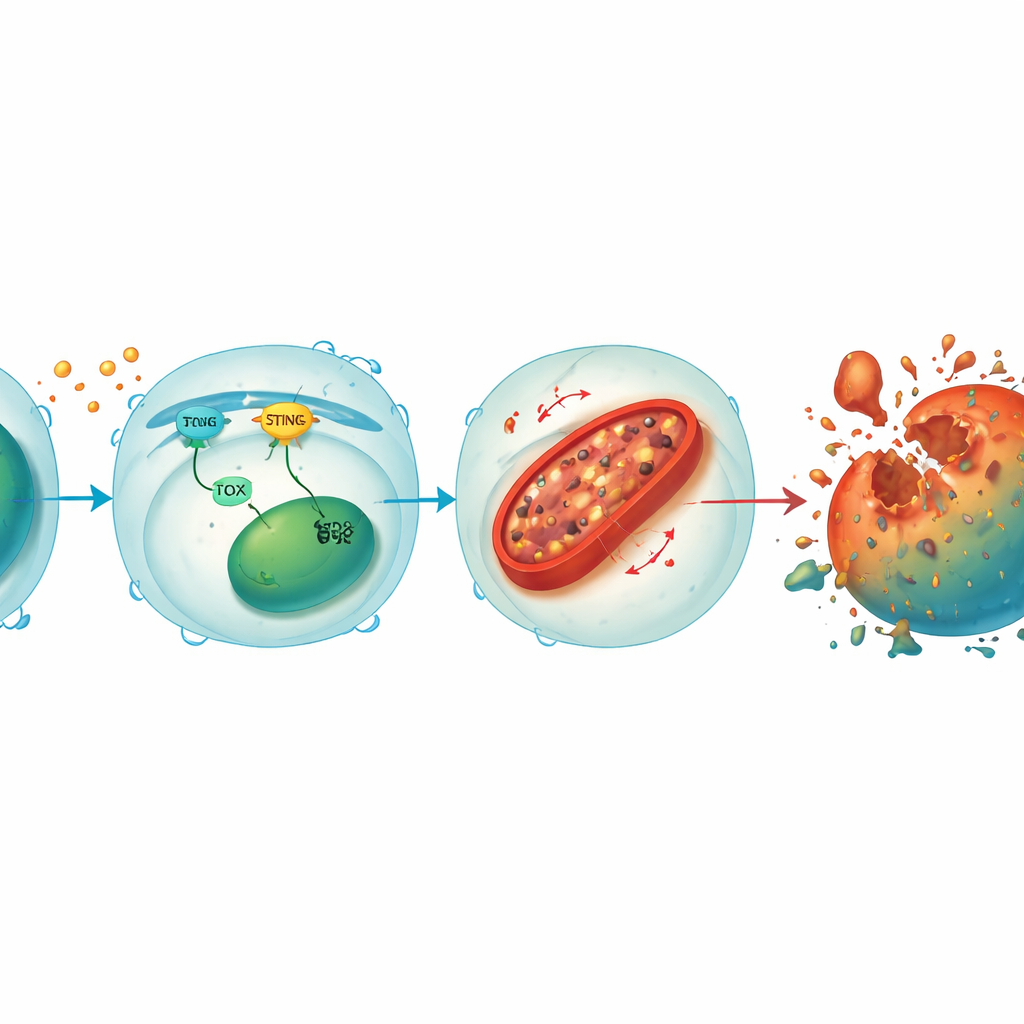
Un circuito che collega i segnali di stress al danno mitocondriale
Approfondendo, il gruppo ha scoperto che STING e TOX formano un circuito autoreinforzante all’interno dei CD8+ T cell. Quando segnali tumorali o virali attivano STING, questo induce fattori a valle che aumentano TOX, e TOX a sua volta contribuisce a mantenere l’attività di STING. Insieme sopprimono HO-1, un enzima che normalmente aiuta a contenere il ferro cellulare. Con HO-1 silenziato, il ferro si accumula nei mitocondri—le centrali energetiche della cellula—portando a livelli elevati di specie reattive dell’ossigeno e all’ossidazione dei lipidi di membrana. Questo danno mitocondriale prosciuga la produzione di energia e infine spinge il linfocita verso la ferroptosi. Ripristinare STING o TOX nei T cell knock-out riportava sovraccarico di ferro e morte cellulare, mentre abbassare ulteriormente HO-1 rendeva vulnerabili anche i T cell protetti, sottolineando HO-1 come freno centrale di questa via distruttiva.
Come il lattato prodotto dal tumore tira il grilletto
Il microambiente tumorale è ricco di lattato, un sottoprodotto del metabolismo alterato del cancro. Lo studio mostra che questo lattato non è solo rifiuto metabolico—aiuta attivamente a far scattare l’interruttore della ferroptosi nei linfociti. Rispetto ad altre cellule, i CD8+ erano particolarmente sensibili al lattato. Quando il lattato entrava nelle cellule attraverso specifici trasportatori, provocava accumulo di ferro, rimpicciolimento mitocondriale, perdita di DNA mitocondriale e maggior danno ossidativo. Contemporaneamente, il lattato aumentava l’attività di STING e TOX e sopprimeva ulteriormente HO-1. I T cell privi di STING o TOX erano molto più resistenti al danno indotto dal lattato. Bloccare un trasportatore chiave del lattato con un farmaco (AZD3965) proteggeva i CD8+ dalla ferroptosi nei topi, aumentava la loro presenza all’interno dei tumori e rallentava la crescita tumorale, imitando il beneficio della delezione genetica di STING nei T cell.
Trasformare una vulnerabilità in un vantaggio terapeutico
Questi approfondimenti meccanicistici hanno implicazioni pratiche. Quando i ricercatori usarono la terapia cellulare adoptiva—iniettando nei topi T cell attivati in laboratorio—trovarono che i linfociti progettati per essere privi di STING o TOX esercitavano un controllo tumorale molto più efficace rispetto ai T cell normali. Inoltre, combinare questi T cell «resistenti alla ferroptosi» con trattamenti esistenti come gli inibitori dei checkpoint PD-1 o TIM-3, la chemioterapia con cisplatino, o un farmaco attivante STING produceva una riduzione tumorale nettamente superiore rispetto a qualsiasi singola terapia. Infine, in campioni tumorali di pazienti con carcinoma cervicale, livelli più alti di TOX e più bassi di HO-1 nei linfociti infiltranti il tumore erano associati a una sopravvivenza peggiore, suggerendo che questa via influenza anche gli esiti clinici nelle persone.
Cosa significa per la cura del cancro in futuro
In termini concreti, lo studio rivela che i tumori possono costringere i nostri migliori linfociti antitumorali a ‘‘arrugginire’’ dall’interno guidando una forma di morte cellulare alimentata dal ferro. Un circuito lattato–STING–TOX riduce la protezione offerta da HO-1, danneggia i mitocondri e porta alla ferroptosi, assottigliando le fila dei CD8+ efficaci. Disgregare questo circuito—ingegnerizzando linfociti privi di STING o TOX, potenziando HO-1 o bloccando l’ingresso del lattato—mantiene i T cell vivi, energici e pronti ad attaccare. Questo lavoro indica la strada verso immunoterapie di nuova generazione che combinano modulazioni metaboliche e genetiche dei T cell con farmaci esistenti per superare la resistenza e fornire un controllo tumorale più duraturo.
Citazione: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Parole chiave: immunoterapia del cancro, linfociti T CD8, ferroptosi, microambiente tumorale, via STING TOX HO-1