Clear Sky Science · it
Seq-Scope-eXpanded: omica spaziale oltre la risoluzione ottica
Vedere le cellule con maggior nitidezza
I nostri corpi sono costituiti da innumerevoli piccole cellule, ciascuna animata da attività che di solito non riusciamo a percepire, anche con potenti microscopi. Questo articolo presenta Seq-Scope-X, una tecnologia che consente ai ricercatori di ingrandire il funzionamento interno dei tessuti con una chiarezza senza precedenti, mappando quali geni e proteine sono attivi in punti precisi dentro e fra le cellule. Questo livello di dettaglio potrebbe trasformare il modo in cui studiamosviluppo, il sistema immunitario e malattie come il cancro o il danno epatico.
Perché mappare le molecole nel loro luogo originale?
Le cellule non funzionano isolate: vivono in quartieri, formano strati e si specializzano in base alla posizione. I metodi tradizionali di sequenziamento sminuzzano i tessuti, perdendo questo contesto spaziale. Strumenti più recenti di “omica spaziale” mantengono le molecole nella loro sede, ma c’è sempre un compromesso. I metodi basati sull’imaging possono cogliere dettagli molto fini ma solitamente monitorano solo un set limitato di geni. I metodi basati sul sequenziamento possono leggere quasi ogni gene contemporaneamente, ma sfocano le caratteristiche fini, spesso diluendo i segnali su diversi micrometri — più grandi di molte strutture subcellulari. Gli autori hanno cercato di colmare questo divario: conservare la lettura ricca e non selettiva del sequenziamento, raggiungendo o persino superando la nitidezza dei moderni microscopi.
Allungare i tessuti per battere i limiti ottici
L’idea centrale di Seq-Scope-X è semplicemente ingegnosa: ingrandire delicatamente il tessuto stesso in modo che ogni nanometro originale di struttura diventi più facile da risolvere. Il gruppo prima ancora ancora le molecole di RNA — o speciali codici DNA legati ad anticorpi — in un idrogel morbido costruito attorno alla sezione di tessuto. Poi digeriscono il tessuto originario e fanno gonfiare il gel in una soluzione salina, allungando fisicamente tutto di circa tre volte pur mantenendo quasi intatte le posizioni relative. Questo gel espanso viene posato su un chip di sequenziamento ultra-denso rivestito di sonde di cattura. Riscaldando con cura l’assemblato, le molecole ancorate vengono rilasciate dal gel e riattaccate al chip, che può poi essere sequenziato per rivelare quali geni o proteine erano presenti in ogni piccola coordinata. 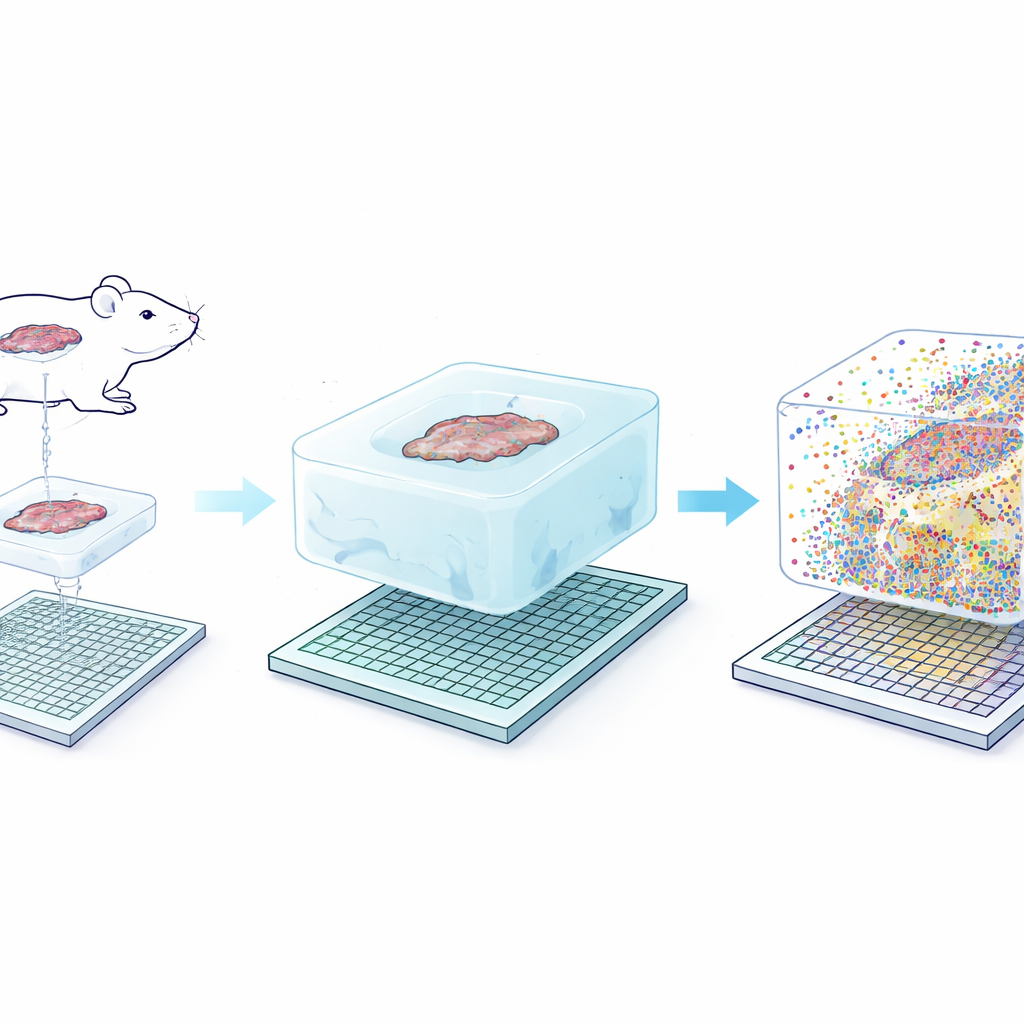
Da cellule sfocate a mappe subcellulari
Quando i ricercatori hanno applicato Seq-Scope-X al fegato di topo, hanno scoperto che il metodo affinava la risoluzione spaziale da circa 0,6 micrometri a circa 0,2 micrometri e aumentava il numero di posizioni misurabili per millimetro quadrato quasi di dieci volte. In termini pratici, ciò che prima appariva come macchie sfocate di segnale si è trasformato in contorni nitidi di singole cellule. Ancora più sorprendente, ammassi di RNA non ancora completamente processati (non spliced) si allineavano strettamente con i centri dei nuclei, mentre l’RNA maturo (spliced) tracciava il citoplasma circostante. Questo ha permesso agli autori di delineare i confini cellulari usando solo l’RNA e di separare le letture geniche nucleari e citoplasmatiche per quasi ogni epatocita nel tessuto, qualcosa che i metodi basati sul sequenziamento precedenti potevano solo suggerire.
Cellule con personalità divise
Con questa nuova chiarezza, il gruppo ha scoperto una forma inattesa di “doppia vita” molecolare all’interno delle cellule del fegato. Lungo il ben noto gradiente dai vasi sanguigni sul lato portale del lobulo epatico a quelli sul lato centrale, gli epatociti si specializzano in compiti metabolici differenti. Seq-Scope-X ha mostrato che, in molte cellule, il profilo genico nel nucleo non corrispondeva al profilo nel citoplasma circostante. Circa un terzo degli epatociti sembrava avere un profilo nucleare allineato con una zona e un profilo citoplasmatico allineato con una zona adiacente. Metodi di imaging indipendenti, inclusi MERFISH e saggi di fluorescenza per RNA a singola molecola, hanno confermato che singoli trascritti possono concentrarsi o nel nucleo o nel citoplasma. Complessivamente, questi risultati suggeriscono che gli epatociti possono spostare dinamicamente i loro ruoli metabolici nel tempo, con il nucleo che si prepara a uno stato futuro mentre il citoplasma riflette lo stato attuale. 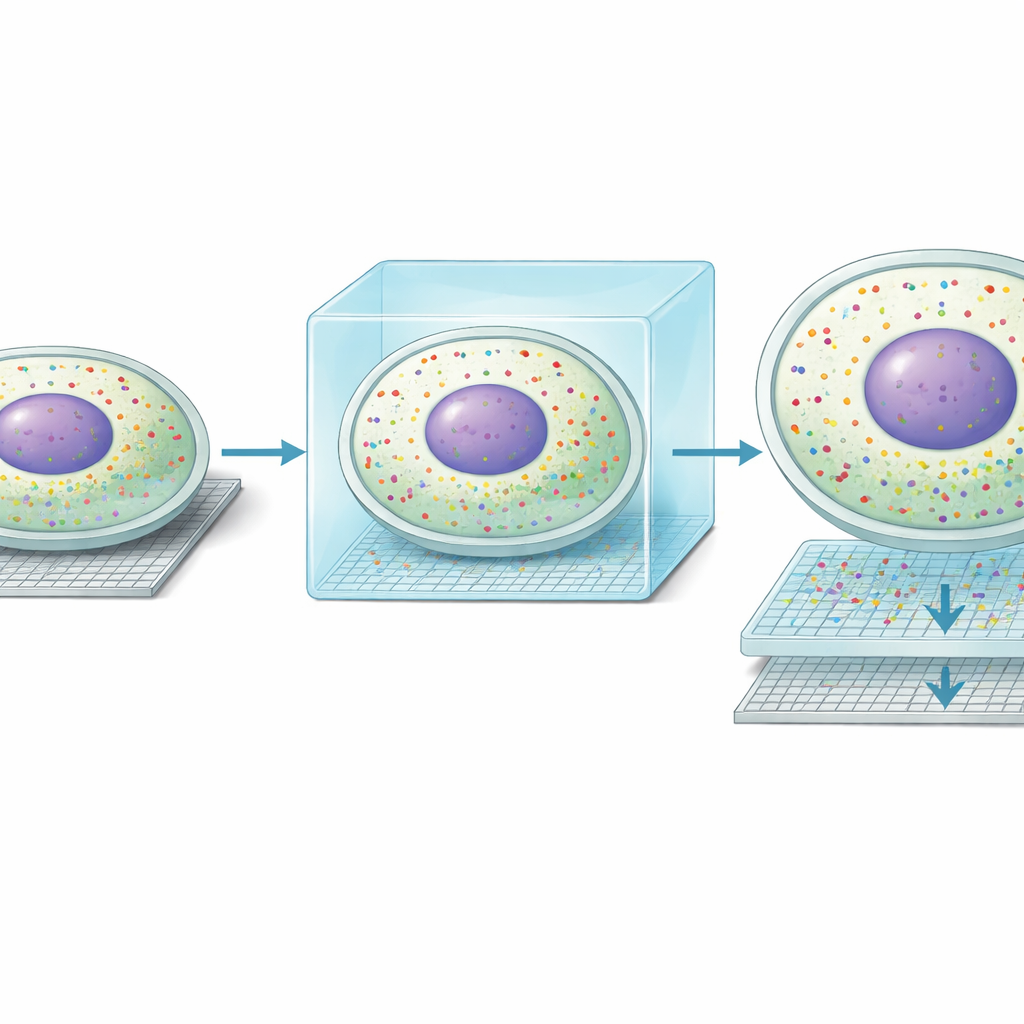
Oltre il fegato: cervello, intestino e tessuti immunitari
Gli autori hanno poi testato se Seq-Scope-X funziona in altri organi. Nel cervello, ha separato nettamente diversi tipi neuronali e cellule di supporto e ha rivelato schemi subcellulari di RNA attorno ai nuclei. Nel colon, ha risolto distinti sottotipi di cellule caliciformi e strati di colonociti lungo l’asse cripta-superficie, catturando di nuovo firme nucleari. Forse in modo più spettacolare, il gruppo ha adattato il metodo alle proteine usando anticorpi codificati con barcode DNA nella milza di topo e nella tonsilla umana. Seq-Scope-X è stato in grado di mappare simultaneamente oltre un centinaio di marcatori di superficie cellulare a risoluzione singola cellula, distinguendo sottogruppi strettamente affollati di cellule T e B e cellule mieloidi. Passando a una chimica del gel più espandibile, hanno spinto la risoluzione effettiva verso il vero nanoscalo, pur preservando l’architettura tissutale abbastanza da permettere una mappatura dettagliata.
Cosa significa per il futuro
Seq-Scope-X dimostra che ingrandire fisicamente i tessuti prima del sequenziamento può superare limiti di risoluzione di lunga data, offrendo un dettaglio quasi a livello microscopico pur leggendo migliaia di geni o tag proteici contemporaneamente. Per un osservatore non specialista, questo significa che gli scienziati possono ora costruire “atlanti molecolari” che non solo indicano dove si trovano le cellule, ma rivelano anche cosa sta accadendo all’interno di diverse parti di ciascuna cellula. Tali mappe potrebbero aiutare a spiegare come i tessuti rispondono a lesioni, come si organizzano le cellule immunitarie negli organi linfoidi e nei tumori, o come spostamenti sottili all’interno delle cellule preannunciano malattie. Sebbene siano necessari ulteriori perfezionamenti per aumentare la copertura e migliorare alcuni pannelli di colorazione, Seq-Scope-X apre una nuova e potente finestra sui paesaggi microscopici che sono alla base della salute e della malattia.
Citazione: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Parole chiave: trascrittomica spaziale, espansione dei tessuti, omica a singola cellula, proteomica spaziale, zonazione epatica