Clear Sky Science · it
IPA derivato dal microbiota protegge dalla colite regolando la chetogenesi mediata da HMGCS2 nell’intestino per favorire la guarigione mucosale
Perché i batteri intestinali sono importanti per un intestino sofferente
Quando il rivestimento dell’intestino è danneggiato, come nella malattia infiammatoria intestinale (MII) o dopo trattamenti medici intensi, l’organismo deve riparare rapidamente questa “pelle” interna per evitare che contenuti nocivi fuoriescano nel circolo sanguigno. Questo studio rivela come una singola molecola prodotta da batteri intestinali benefici possa aiutare l’intestino a guarire, indicando nuove strategie per trattare disturbi intestinali cronici senza sopprimere ampiamente il sistema immunitario.
Un segnale utile dai microbi amici
I ricercatori hanno iniziato confrontando le impronte chimiche nelle feci di persone con MII e volontari sani, oltre che in diversi modelli murini di colite. Tra centinaia di molecole, una è emersa in modo significativo: l’acido indolo-3-propionico (IPA), un prodotto di degradazione dell’amminoacido alimentare triptofano prodotto da certi batteri intestinali. I livelli di IPA erano costantemente più bassi nelle persone con morbo di Crohn e nei topi con colite rispetto ai corrispondenti sani. Ciò suggerisce che la perdita di IPA potrebbe far parte di ciò che va storto quando il rivestimento intestinale si infiamma e non riesce a ripararsi.
Rinforzare la parete protettiva dell’intestino
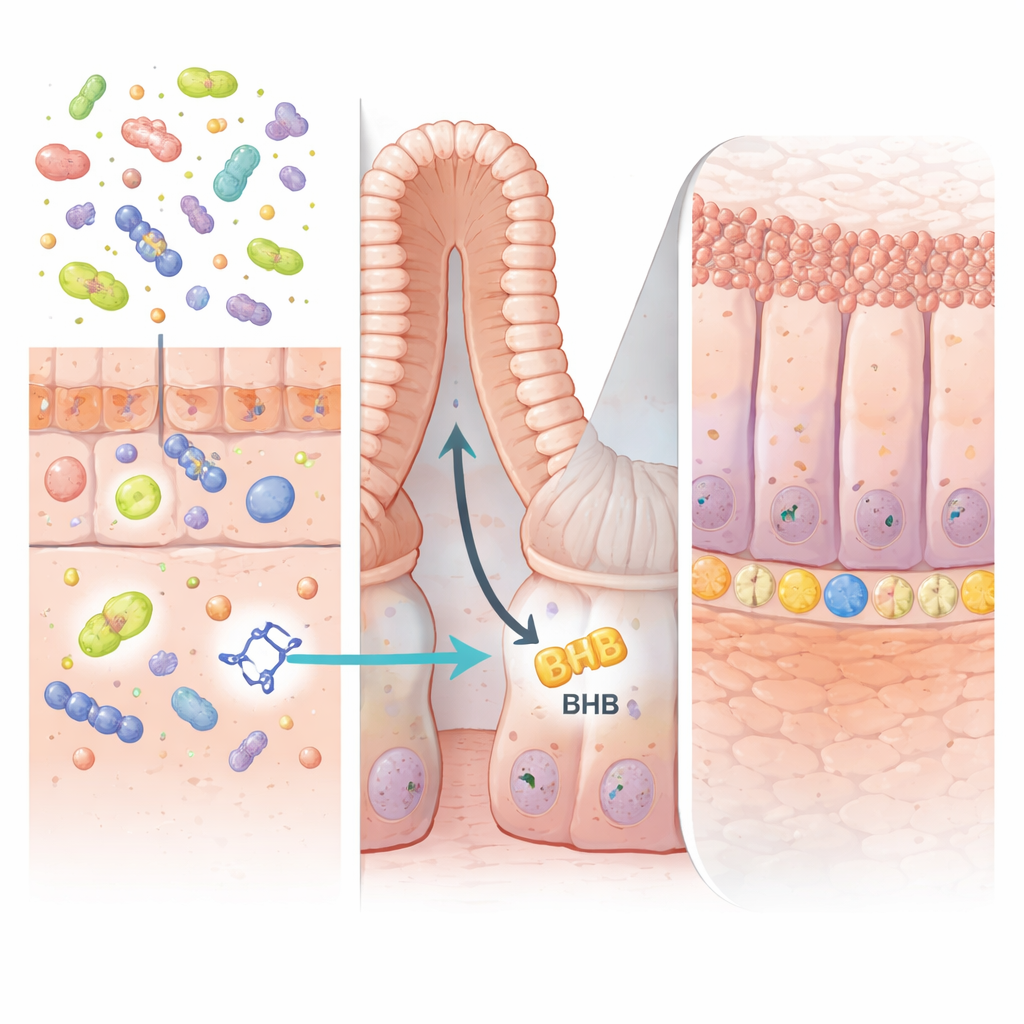
Per verificare se l’IPA fosse solo un marcatore della malattia o avesse un ruolo protettivo, il team ha somministrato IPA ai topi prima di indurre vari tipi di lesione intestinale, inclusa la colite chimica e il danno da radiazioni. I topi trattati con dosi adeguate di IPA avevano colon più lunghi e più sani, meno alterazioni infiammatorie al microscopio e uno strato di muco più spesso con giunzioni cellulari più strette. Mostravano una minore perdita di marcatori infiammatori e un numero maggiore di cellule caliciformi, produttrici dello strato di muco protettivo. Importante, questi benefici si osservavano anche in topi germ-free privi di microbiota residente, dimostrando che, una volta presente, l’IPA può agire direttamente sul rivestimento intestinale senza richiedere altri microbi.
Alimentare le cellule staminali con un tipo speciale di energia
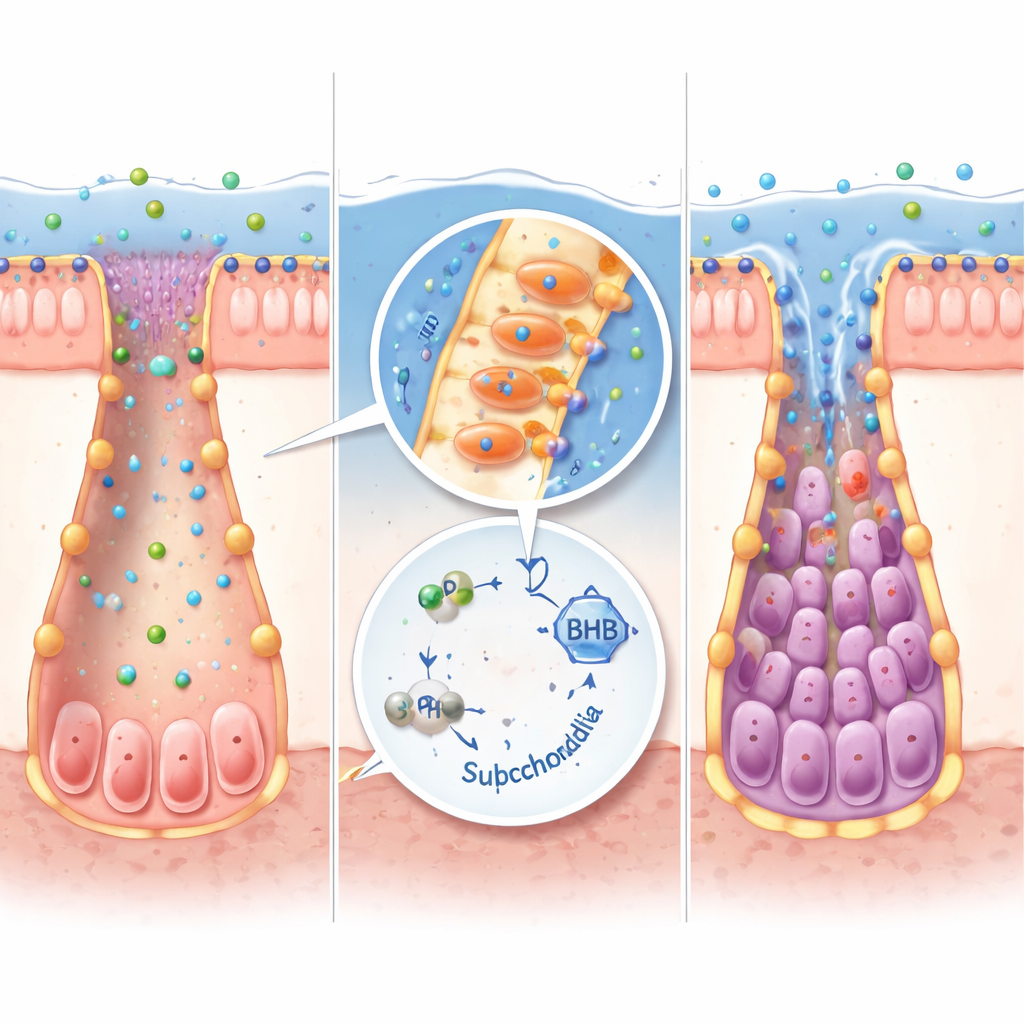
La chiave dell’azione dell’IPA si trovava nelle profonde “cripte” intestinali, le piccole tasche dove risiedono le cellule staminali che rinnovano continuamente il rivestimento. Gli autori hanno mostrato che l’IPA attiva una proteina chiamata PPARα nelle cellule epiteliali intestinali. Questo, a sua volta, aumenta la produzione dell’enzima HMGCS2, che guida la chetogenesi—il processo di sintesi della molecola ricca di energia β‑idrossibutirrato (BHB). L’aumento di BHB nella parete intestinale stimolava l’espansione delle cellule staminali LGR5-positive e la rigenerazione più rapida del tessuto danneggiato. Quando l’enzima HMGCS2 o PPARα venivano eliminati selettivamente dalle cellule intestinali nei topi, l’IPA non poteva più potenziare l’attività delle cellule staminali né proteggere dalla colite, confermando che questa via di produzione di chetoni è essenziale.
Dalle fabbriche batteriche ai tessuti umani
Non tutti i batteri intestinali possono produrre IPA. Rianalizzando ampi dataset di microbioma, i ricercatori hanno identificato Peptostreptococcus russellii come un importante produttore di IPA che risulta diminuito in diverse coorti di MII. In colture di laboratorio questo batterio convertiva il triptofano in IPA in modo efficiente. Quando topi germ-free sono stati colonizzati con P. russellii, i loro livelli di IPA sono aumentati, i geni della produzione di chetoni si sono attivati, i marcatori delle cellule staminali sono cresciuti e la gravità della colite è diminuita rispetto ai topi che ricevevano un trapianto microbico generico. La stessa via IPA–chetone ha funzionato in organoidi intestinali in miniatura derivati da tessuti murini e umani: l’aggiunta di IPA o BHB ha aiutato le cellule staminali a riprendersi dopo danno infiammatorio riducendo al contempo i segnali pro-infiammatori.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, il lavoro delinea una catena semplice ma potente di eventi: alcuni batteri intestinali trasformano il triptofano alimentare in IPA; l’IPA attiva un interruttore metabolico nelle cellule intestinali; questo interruttore aumenta la produzione di BHB; e il BHB, a sua volta, rivitalizza le cellule staminali che ricostruiscono il rivestimento intestinale. Per le persone con MII o altre condizioni che danneggiano la barriera intestinale, terapie che ripristinino l’IPA o ne imitino in sicurezza gli effetti—tramite dieta, probiotici mirati o farmaci progettati—potrebbero promuovere una vera guarigione mucosale senza una soppressione immunitaria generalizzata. Sebbene siano necessari ulteriori studi nei pazienti, questo asse microbo–metabolita–cellula staminale offre una nuova e promettente prospettiva per riparare l’intestino dall’interno.
Citazione: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Parole chiave: microbioma intestinale, cellule staminali intestinali, malattia infiammatoria intestinale, metaboliti microbici, guarigione mucosale