Clear Sky Science · it
CD38 degrada MAVS attraverso la mitofagia per inibire la secrezione di interferone di tipo I nelle cellule del carcinoma nasofaringeo e compromette l’immunità anti-tumorale mediata da linfociti T CD8+
Perché questo è importante per la terapia del cancro
Il carcinoma nasofaringeo è un tumore che origina dietro il naso ed è particolarmente comune nell’Asia orientale e sudorientale. I farmaci basati sul sistema immunitario che liberano i linfociti T del paziente hanno cambiato le prospettive per alcuni pazienti, ma la maggior parte continua a non trarne beneficio. Questo studio scopre un freno nascosto all’interno delle stesse cellule tumorali: una molecola chiamata CD38 che silenzia perlopiù un sistema di allarme interno e indebolisce l’attacco dei linfociti T CD8 citotossici. Comprendere e disattivare questo freno potrebbe rendere le immunoterapie esistenti efficaci per molte più persone.
Un interruttore nascosto sulle cellule tumorali
I ricercatori si sono concentrati su CD38, una proteina presente su molte cellule immunitarie ma anche sulle cellule del carcinoma nasofaringeo. Studi precedenti avevano collegato CD38 alla resistenza contro i farmaci inibitori dei checkpoint che prendono di mira PD-1 e PD-L1. In questo lavoro il gruppo si è chiesto se CD38 all’interno delle cellule tumorali modifichi direttamente la capacità dei linfociti T CD8 di riconoscere e distruggere quelle cellule. Coltivando cellule tumorali umane con o senza CD38 insieme a linfociti T CD8 umani attivati, hanno osservato che la rimozione di CD38 dalle cellule tumorali rendeva i T molto più potenti: secernevano livelli più alti di molecole d’attacco chiave, sopravvivevano meglio e uccidevano più cellule tumorali. Quando CD38 veniva reinserita, la funzione dei T diminuiva, indicando CD38 come soppressore intrinseco del tumore sull’attacco immunitario.
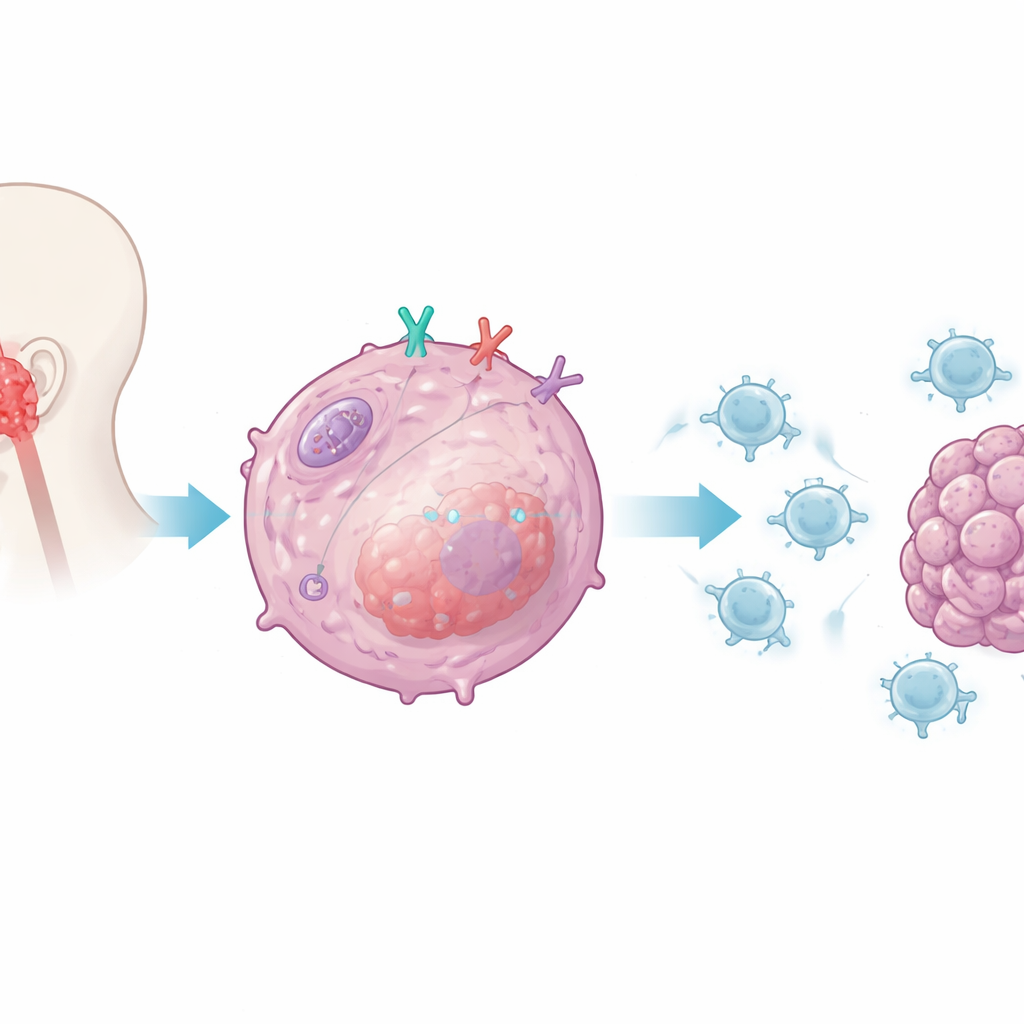
Abbassare l’allarme interno della cellula
Il team ha poi indagato come CD38 invii questo segnale soppressivo. Si sono focalizzati sul sistema di allarme innato delle cellule tumorali, che normalmente rileva materiale genetico simile a virus e innesca gli interferoni di tipo I—messaggeri potenti che stimolano l’immunità. Nelle cellule tumorali prive di CD38 i ricercatori hanno osservato un forte aumento di interferone-beta e di chemochine che richiamano i linfociti T CD8 nei tumori. Hanno dimostrato che CD38 attenua selettivamente la via controllata da un sensore interno chiamato RIG-I e dal suo adattatore MAVS, che risiede sui mitocondri, le centrali energetiche della cellula. Quando CD38 era presente, l’attivazione di questa via e delle sue molecole di segnalazione a valle era ridotta; quando CD38 veniva rimossa, la segnalazione e la produzione di interferone aumentavano, rendendo il tumore più visibile al sistema immunitario.
Come CD38 distrugge un hub di segnalazione chiave
Approfondendo, gli scienziati hanno scoperto che CD38 si associa fisicamente a MAVS sui mitocondri e interferisce con il suo rapporto con RIG-I, indebolendo la trasmissione del segnale. Ancora più sorprendente, livelli più alti di CD38 portavano a una riduzione della proteina MAVS senza alterare il suo codice genetico, suggerendo un’azione distruttiva attiva. Test con vari inibitori hanno mostrato che questa perdita dipendeva dalla macchina di riciclo della cellula nota come autofagia, e in particolare da una forma che prende di mira i mitocondri. CD38 aumentava i marcatori della “self-eating” mitocondriale, riduceva diverse proteine mitocondriali e favoriva l’inclusione di MAVS in strutture autofagosomiali poi degradate. Bloccare la mitofagia preservava MAVS e riportava in funzione la segnalazione degli interferoni, indicando che CD38 disattiva l’allarme guidando MAVS verso il sistema di smaltimento cellulare.
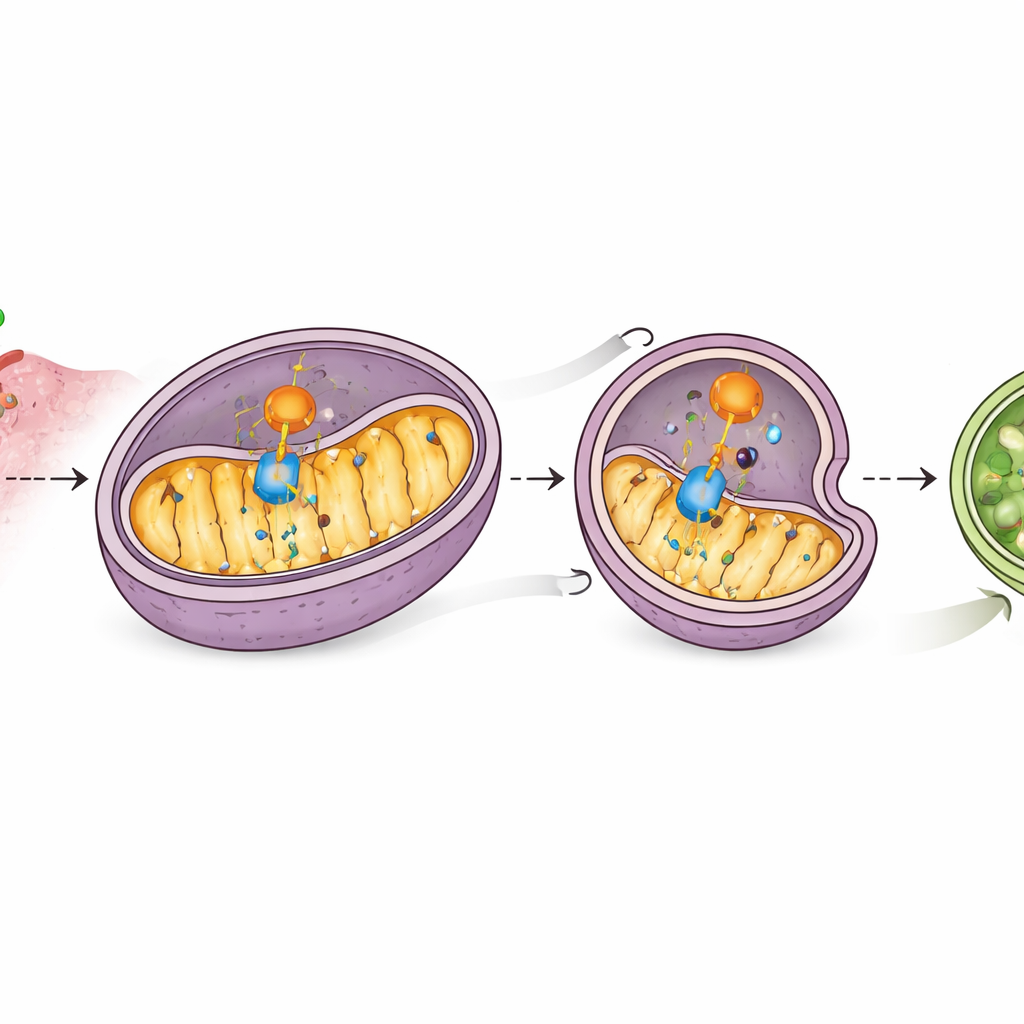
Un aiutante che guida i mitocondri all’autodistruzione
Lo studio ha identificato un altro elemento, PHB2, una proteina interna ai mitocondri che funge da recettore per la rimozione mirata dei mitocondri. Spettrometria di massa ed esperimenti di legame hanno mostrato che CD38 interagisce con PHB2 e aumenta la presenza di PHB2 nei mitocondri, dove PHB2 a sua volta recluta la macchina autofilagica centrale. PHB2 si lega anche a MAVS, e CD38 rafforza questo contatto. Quando PHB2 veniva ridotto, CD38 non riusciva più ad attivare efficacemente la mitofagia mitocondriale, i livelli di MAVS ritornavano e i geni legati agli interferoni si riattivavano. Questo rivela una catena di eventi: CD38 coinvolge PHB2, PHB2 coinvolge MAVS, e insieme conducono MAVS verso mitocondri destinati alla degradazione, silenziando l’allarme degli interferoni.
Prove da modelli animali
Per testare l’impatto in organismi viventi, i ricercatori hanno usato tumori murini ingegnerizzati privi di CD38. In topi immunocompetenti questi tumori crescevano più lentamente, contenevano più linfociti T CD8 e avevano una frazione maggiore di cellule che producevano interferone-gamma, un marcatore di risposte anti-tumorali attive. Bloccare il recettore per gli interferoni di tipo I rimosse questo vantaggio, confermando che la segnalazione degli interferoni è essenziale per l’immunità migliorata. In topi umanizzati portatori di tumori nasofaringei, la riduzione di CD38 rallentò similmente la crescita e aumentò l’infiltrazione dei T CD8, ma questo beneficio svanì quando anche MAVS veniva ridotto nelle cellule tumorali. Questi risultati in vivo consolidano l’idea che l’asse CD38–PHB2–MAVS all’interno delle cellule tumorali modelli la forza della risposta dei linfociti T dell’organismo.
Cosa significa per le terapie future
Complessivamente, il lavoro mostra che CD38 nelle cellule del carcinoma nasofaringeo agisce come un sabotatore interno dell’immunità anti-tumorale. Guidando una forma selettiva di riciclo mitocondriale, CD38 depleta MAVS, indebolisce la produzione di interferone di tipo I, riduce la presentazione degli antigeni e alla fine attenua l’attacco dei linfociti T CD8. I composti attuali che bloccano CD38 mirano principalmente alla sua attività enzimatica e non rimuovono la proteina né restaurano MAVS. Gli autori sostengono che nuove strategie volte a ridurre i livelli di CD38 o a interrompere la sua interazione con PHB2 o MAVS potrebbero riattivare l’allarme degli interferoni all’interno dei tumori. In combinazione con gli inibitori dei checkpoint esistenti, tali approcci potrebbero trasformare più carcinomi nasofaringei—e potenzialmente altri tipi di tumore—da immunologicamente freddi a responsivi all’immunità.
Citazione: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Parole chiave: carcinoma nasofaringeo, immunoterapia del tumore, interferone di tipo I, linfociti T CD8, mitofagia