Clear Sky Science · it
Varianti di perdita di funzione nell'attivatore CAPN1 CD99L2 causano atassia spastica legata al cromosoma X
Perché è importante per le famiglie con problemi motori inspiegati
Molte persone convivono per anni con difficoltà nel camminare, rigidità muscolare o problemi di equilibrio e linguaggio senza mai conoscere la vera causa. Questo studio mostra come i moderni test del DNA possano finalmente fornire risposte ad alcune di queste famiglie. I ricercatori non solo hanno confrontato diversi test genetici per i disturbi del movimento rari, ma hanno anche scoperto una causa finora sconosciuta di una condizione denominata atassia spastica legata al cromosoma X, indicando vie biologiche che potrebbero essere rilevanti anche per malattie cerebrali più comuni.
Trovare gli aghi genetici in un pagliaio di malattie rare
I disturbi del movimento rari, come l’atassia (movimenti instabili) e la paraplegia spastica (gambe rigide e deboli), sono spesso sospettati di origine genetica, ma per la maggior parte dei pazienti i test standard risultano negativi. Il gruppo ha seguito 2.811 persone in Germania e in tutta Europa, inviate per sospetti disturbi del movimento rari, per sei anni. Inizialmente hanno eseguito i test mirati tradizionali che cercano espansioni di ripetizioni note in un numero limitato di geni; questi hanno fornito una risposta in circa l’11% dei casi. Successivamente hanno utilizzato il sequenziamento dell’esoma, che legge solo le porzioni codificanti delle proteine del genoma, trovando spiegazioni genetiche definitive in circa il 19% dei pazienti, soprattutto in quelli con spasticità.
Andare oltre i test standard con il sequenziamento dell’intero genoma
Per approfondire, gli scienziati hanno impiegato il sequenziamento dell’intero genoma, che legge quasi tutto il DNA di una persona, comprese regioni che i test standard e l’esoma possono perdere. Tra 486 individui sottoposti a questo test più completo, il tasso diagnostico è aumentato di circa 7,5 punti percentuali, in gran parte perché il sequenziamento del genoma individua meglio cambiamenti complessi come riarrangiamenti strutturali ed espansioni di ripetizioni. Lo studio ha inoltre mostrato che informazioni cliniche raccolte con cura—in particolare descrizioni dettagliate dei sintomi, età più giovane al momento del test e la presenza di spasticità associata ad altri problemi del movimento—aiutavano a prevedere chi aveva maggiori probabilità di ottenere una diagnosi genetica chiara.
Scoprire una nuova causa legata al cromosoma X dell’atassia spastica
Anche dopo questi approfonditi esami, molti pazienti restavano senza diagnosi. I ricercatori hanno aggregato dati genetici di oltre 13.000 individui e usato un approccio di “burden genico”, chiedendosi quali geni presentassero varianti sospette con maggiore frequenza nei pazienti rispetto ai controlli sani. Questa analisi ha indicato non solo geni noti, ma ha evidenziato in modo marcato anche un gene precedentemente trascurato sul cromosoma X chiamato CD99L2. Combinando risultati provenienti da diverse famiglie in Europa, hanno identificato 25 maschi affetti in 20 famiglie che portavano varianti dannose in questo gene. Questi uomini sviluppavano tipicamente problemi nel camminare, rigidità degli arti inferiori, linguaggio slurred e talvolta difficoltà di equilibrio in età adulta media o avanzata, mentre le portatrici femminili risultavano per lo più indenne—schemi coerenti con una malattia legata al cromosoma X. Le varianti distruggevano principalmente la proteina normale o rimuovevano parti cruciali di essa, suggerendo fortemente che la perdita di funzione sia la causa della malattia.
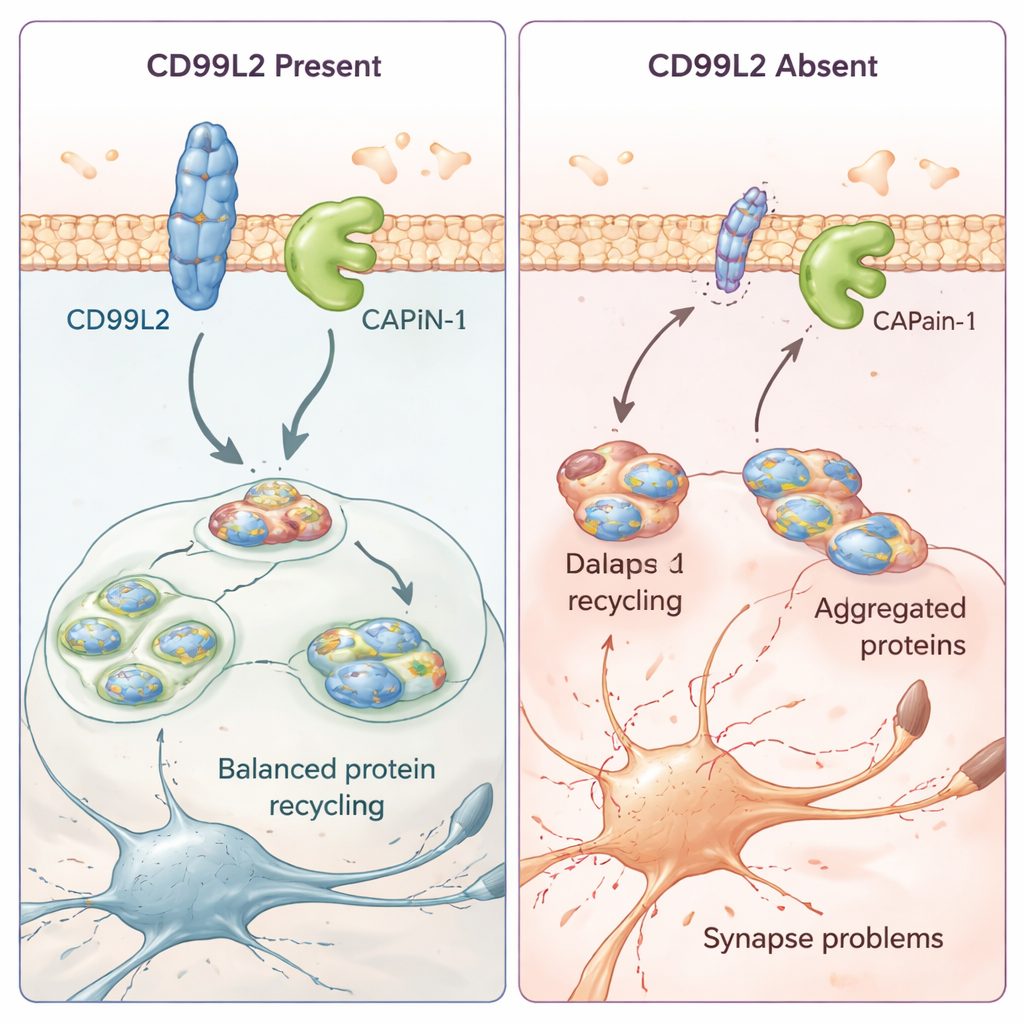
Come una piccola proteina di membrana aiuta a proteggere le cellule cerebrali
Per capire cosa faccia realmente CD99L2 nelle cellule, il gruppo ha utilizzato modelli cellulari e cellule della pelle derivate dai pazienti. Hanno scoperto che la proteina CD99L2 si trova nella membrana cellulare ed è solitamente marcata con piccoli indicatori di “ubiquitina” che ne regolano la durata prima della degradazione. CD99L2 si lega fisicamente alla calpaina-1 (CAPN1), un enzima attivato dal calcio che taglia altre proteine e contribuisce a mantenere sane le sinapsi—i punti di contatto tra le cellule nervose. Quando CD99L2 è presente e integro, aiuta ad attivare e disattivare la calpaina-1 in modo controllato, per poi essere essa stessa scissa e riciclata. Quando CD99L2 manca o è strutturalmente alterata, l’attivazione di calpaina-1 è compromessa. Nelle cellule dei pazienti ciò si accompagna a un’attività alterata di molti geni legati alle sinapsi e alla comunicazione neuronale, suggerendo che cambiamenti sottili ma diffusi nella circuiteria cerebrale possano essere alla base del progressivo disturbo del movimento.
Cosa significa per i pazienti oggi e domani
Per le famiglie con atassia spastica o paraplegia spastica inspiegate, questo lavoro offre due progressi. Primo, dimostra che l’uso precoce del sequenziamento dell’intero genoma, insieme a una descrizione clinica accurata, può aumentare in modo significativo le probabilità di ottenere una diagnosi genetica certa. Secondo, aggiunge CD99L2 all’elenco dei geni che controllano l’attività delle calpaine, una via già coinvolta in altre atassie rare e in condizioni comuni come Alzheimer e Parkinson. In termini pratici, lo studio rivela un nuovo interruttore on–off che contribuisce a mantenere l’equilibrio del mantenimento delle cellule cerebrali; quando questo interruttore si rompe, i neuroni si deteriorano lentamente, portando a rigidità e perdita di coordinazione. Comprendere questo meccanismo potrebbe in futuro aprire la strada a terapie che modulino finemente l’attività delle calpaine e proteggano le cellule cerebrali in una serie di malattie neurologiche.
Citazione: Menden, B., Incebacak Eltemur, R.D., Demidov, G. et al. Loss-of-function variants in the CAPN1 activator CD99L2 cause X-linked spastic ataxia. Nat Commun 17, 1698 (2026). https://doi.org/10.1038/s41467-026-69337-9
Parole chiave: atassia spastica, disturbi del movimento rari, sequenziamento del genoma, CD99L2, calpaina-1