Clear Sky Science · it
Valutazione delle inferenze del percorso di segnalazione EGF usando la fosfoproteomica e le interazioni chinasi-substrato
Perché questo conta anche al di fuori del laboratorio
Le nostre cellule ascoltano e rispondono costantemente ai segnali dell’ambiente. Uno dei più importanti è il fattore di crescita epidermico (EGF), che regola crescita, divisione e sopravvivenza cellulare. Quando questo sistema di comunicazione si guasta, può guidare lo sviluppo di tumori e altre malattie. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: se usiamo le potenti tecnologie di misura e i modelli computazionali odierni, quanto meglio possiamo realmente comprendere il percorso di segnalazione EGF rispetto a quanto mostrato nei diagrammi dei libri di testo?
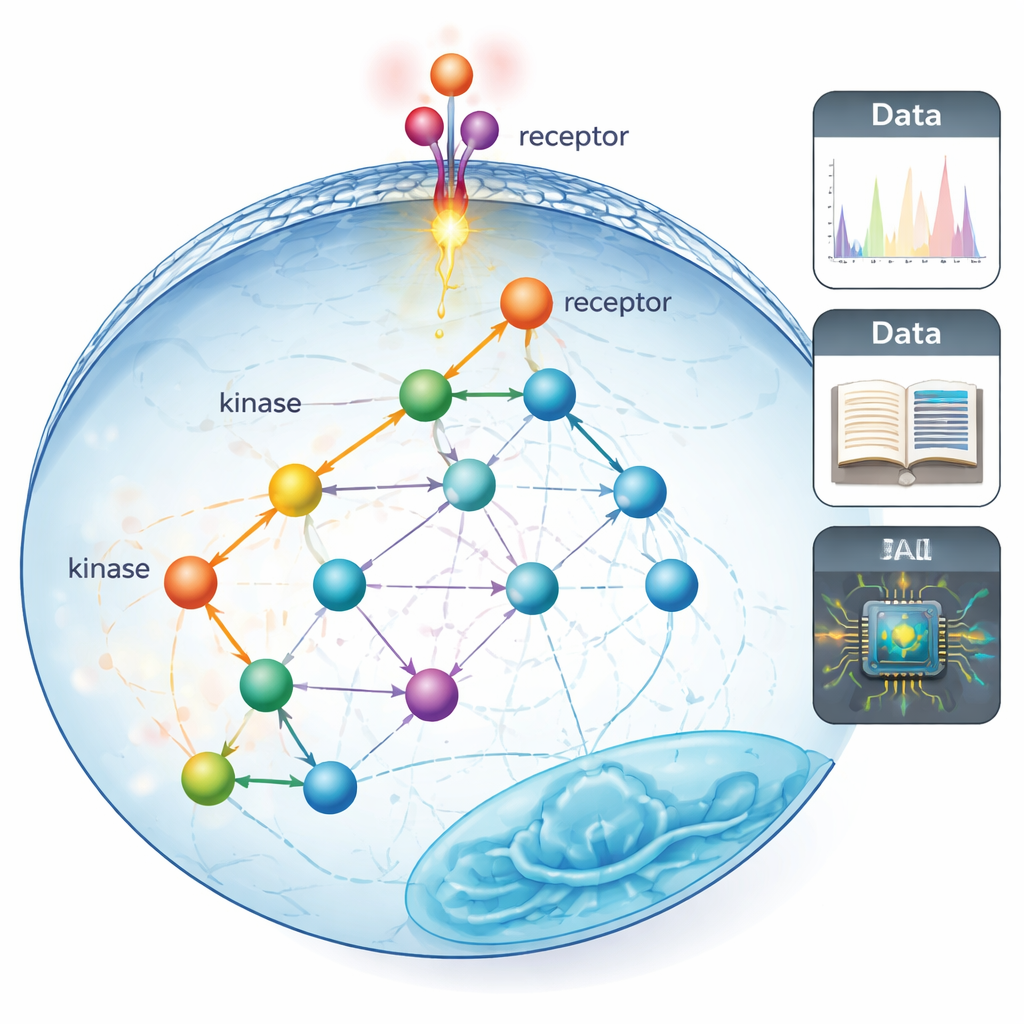
Da linee rette a schemi elettrici della vita reale
I “percorsi di segnalazione” tradizionali sono spesso disegnati come catene ordinate, quasi lineari, di proteine che trasmettono un messaggio dalla superficie cellulare al nucleo. Quei mappe sono state costruite in decenni di esperimenti mirati e lenti, capaci di osservare solo poche proteine alla volta. Gli autori sostengono che questo ci ha lasciato una visione ristretta, come sotto un lampione: sappiamo molto sulle poche proteine facili da studiare, e molto meno sulla rete più ampia di connessioni che probabilmente esiste nelle cellule reali.
Ascoltare migliaia di interruttori molecolari contemporaneamente
Per andare oltre questa visione limitata, il gruppo ha impiegato la fosfoproteomica, una tecnica di spettrometria di massa in grado di monitorare decine di migliaia di piccole etichette chimiche chiamate gruppi fosfato sulle proteine in un singolo esperimento. Queste etichette sono aggiunte da enzimi detti chinasi e funzionano come interruttori rapidi on/off per la segnalazione. I ricercatori hanno prima assemblato le mappe più complete fino ad oggi di “chi può fosforilare chi” unendo tre tipi di informazione: risultati curati dalla letteratura, predizioni di un modello di intelligenza artificiale che legge le sequenze proteiche e ampi screening sperimentali delle preferenze delle chinasi. Questo ha ampliato notevolmente la copertura delle relazioni chinasi–substrato note o sospette, passando da circa il 5% dei siti misurabili fino a oltre il 70–80%.
Stress-test della segnalazione EGF attraverso molti esperimenti
Successivamente si sono concentrati sulla risposta a EGF, un percorso classico e un attore principale nei tumori di polmone, seno, pelle e cervello. Il gruppo ha combinato tre dataset pubblicati all’avanguardia con tre nuove misurazioni molto profonde e a risoluzione temporale in cellule derivate dal rene, oltre a due studi di controllo con stimoli diversi. Insieme, questi esperimenti hanno misurato oltre 40.000 siti di fosforilazione per dataset e hanno seguito come cambiavano nei minuti successivi alla stimolazione con EGF. Pur con differenze nei pattern complessivi tra tipi cellulari e tecnologie, siti chiave di fosforilazione nel percorso EGF si sono attivati ripetutamente, confermando che il segnale centrale è robusto anche attraverso esperimenti diversi.
Ricostruire la conversazione nascosta tra le chinasi
Dopo aver inferito quali chinasi diventavano più o meno attive, gli autori hanno provato a ricostruire la “conversazione” sottostante fra esse: quali chinasi probabilmente attivano o influenzano altre. Hanno convertito le loro mappe chinasi–substrato in reti chinasi–chinasi e applicato tre strategie computazionali, da schemi di ranking semplici a un approccio più complesso che forza il risultato a somigliare a un albero diretto radicato sul recettore EGF. Hanno confrontato i percorsi inferiti con diversi tipi di “verità di riferimento”: una mappa EGF curata in un database, esperimenti su larga scala in cui singole chinasi erano sovraespresse e coppie di siti di chinasi il cui comportamento era fortemente correlato nel tempo.
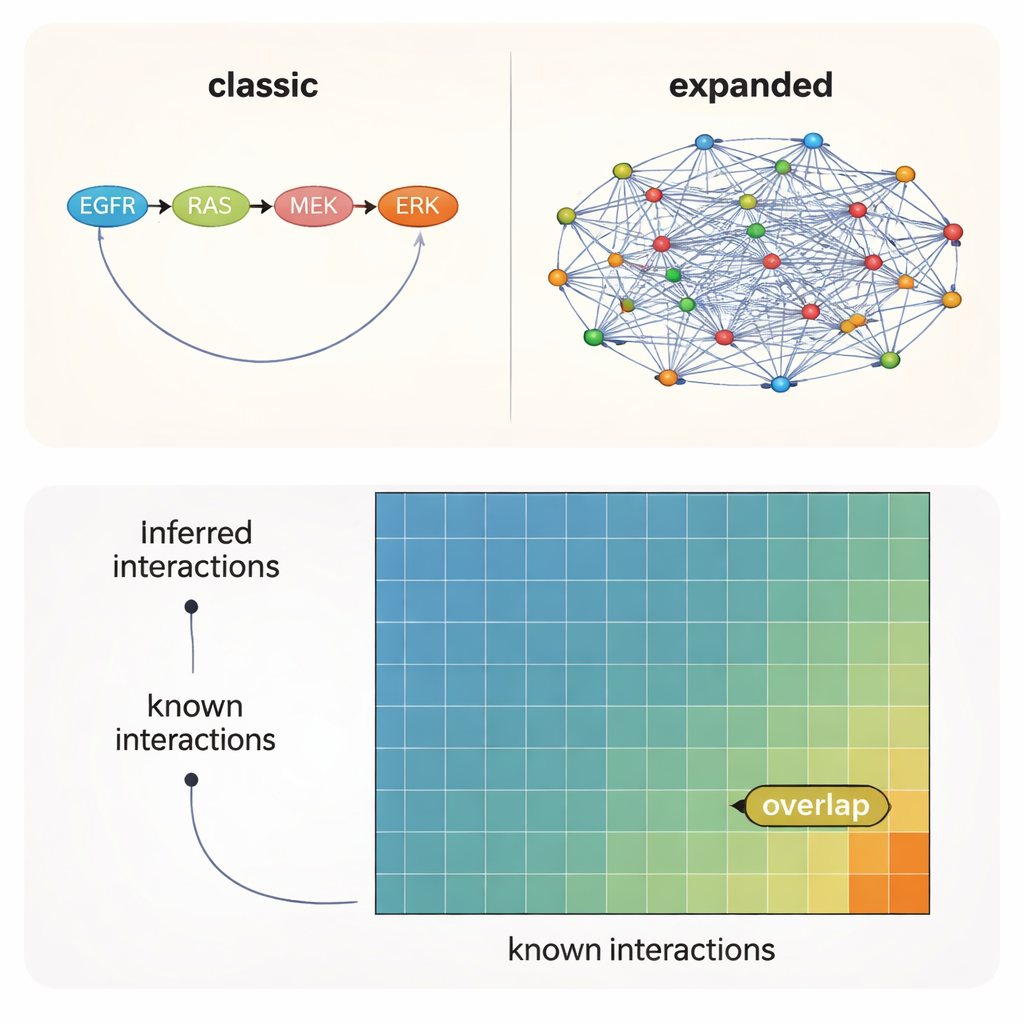
I collegamenti più plausibili restano fuori dalla mappa ufficiale
In tutti i test, un messaggio è stato chiaro: la scelta della conoscenza a priori—la rete di partenza che si fornisce all’algoritmo—contava più del metodo particolare o persino del contesto sperimentale. Le reti costruite dalla letteratura recuperavano il maggior numero di interazioni note, mentre risorse predittive più ampie indicavano molte connessioni plausibili aggiuntive non ancora documentate formalmente. Anche nelle migliori condizioni, però, solo circa il 10–12% delle interazioni suggerite dai dati e dai modelli era presente in uno qualsiasi dei set di riferimento. In altre parole, circa il 90% dei legami chinasi–chinasi supportati risiede in territorio inesplorato.
Cosa significa questo per i trattamenti futuri
Per i non specialisti, la conclusione è che il ben noto diagramma del percorso EGF nei libri di testo è probabilmente solo la punta dell’iceberg. La fosfoproteomica moderna, combinata con metodi computazionali avanzati, rivela una rete di segnalazione molto più ricca e intrecciata. Molti di questi collegamenti suggeriti potrebbero rappresentare modi finora trascurati in cui le cellule tumorali riorientano i segnali per sfuggire ai farmaci, oppure nuove opportunità per progettare combinazioni di farmaci più intelligenti. Lo studio non prova che ogni nuovo collegamento sia reale, ma fornisce una mappa e strumenti aperti per i ricercatori per testare queste idee, con l’obiettivo ultimo di terapie più precise ed efficaci nelle malattie in cui la segnalazione EGF gioca un ruolo centrale.
Citazione: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Parole chiave: segnalazione EGF, fosfoproteomica, protein chinasi, reti di segnalazione cellulare, biologia del cancro