Clear Sky Science · it
Mycobacterium tuberculosis modula la fosforilazione della proteina ospite ATP6V1E1 per favorire la sopravvivenza intracellulare
Perché questo è importante per combattere la tubercolosi
La tubercolosi resta una delle malattie infettive più letali al mondo, causando oltre un milione di morti ogni anno. Le nostre cellule immunitarie sono dotate di potenti “cassette acide di riciclaggio” che normalmente digeriscono i microbi invasori. Questo lavoro rivela come il batterio della tubercolosi, Mycobacterium tuberculosis (Mtb), saboti quel sistema di acidificazione all’interno delle nostre cellule e mostra che un farmaco che prende di mira questo espediente può aiutare gli animali infetti a eliminare l’infezione in modo più efficace.
Il bagno acido della cellula per i germi
Quando i batteri della tubercolosi vengono inalati nei polmoni, vengono rapidamente ingeriti da cellule immunitarie chiamate macrofagi. I batteri finiscono in vescicole di membrana che dovrebbero fondersi con i lisosomi—piccoli sacchi pieni di enzimi digestivi che funzionano al meglio in un ambiente fortemente acido. Quell’acidità è creata da una pompa molecolare, la vacuolare ATPasi (V-ATPasi), che usa carburante cellulare per spingere protoni nei lisosomi e abbassare il pH interno. Una corretta acidificazione è cruciale per degradare Mtb, eppure decenni di studi hanno mostrato che questo patogeno in qualche modo mantiene i suoi compartimenti meno acidi e sopravvive.
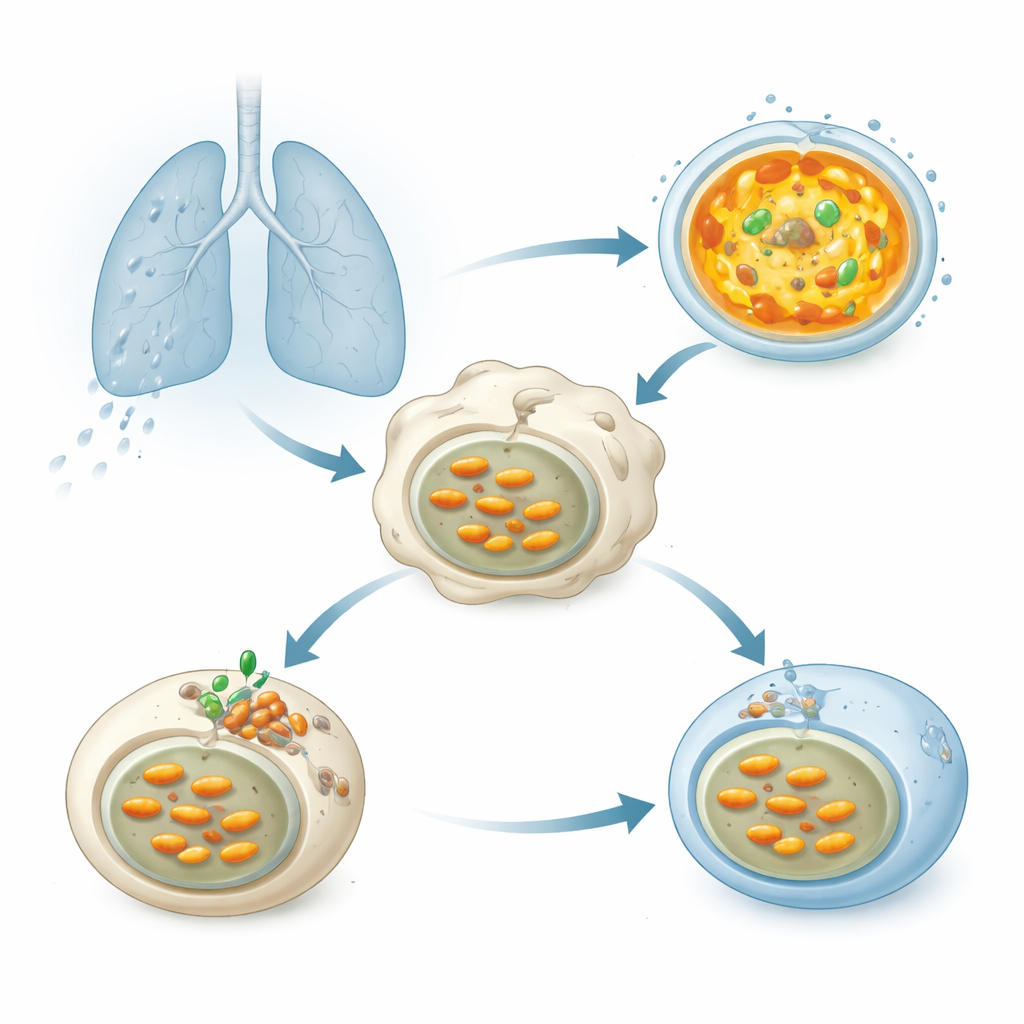
Un alleato batterico segreto che blocca l’acidificazione
I ricercatori hanno selezionato più di 200 proteine che Mtb può rilasciare per vedere quali indeboliscono l’acidificazione lisosomiale nelle cellule umane. Una in particolare è emersa: un enzima chiamato Chp2 (noto anche come Rv1184). Quando le cellule esprimevano Chp2, i loro lisosomi si evidenziavano meno con coloranti sensibili all’acidità, indicando un pH più elevato e meno ostile. Ceppi di Mtb ingegnerizzati per non avere Chp2 non sopprimevano più l’acidificazione; in macrofagi infettati e nei topi, questi batteri mutanti venivano eliminati più efficacemente e causavano danni polmonari più lievi. Ripristinare Chp2 nel ceppo mutante riportava sia il blocco dell’acidificazione sia l’aumento del carico batterico, identificando Chp2 come un fattore di virulenza che aiuta Mtb a persistere all’interno delle cellule ospiti.
La subunità della pompa dell’ospite che agisce come interruttore di controllo
Per capire come Chp2 interferisca con l’acidificazione, il gruppo ha cercato componenti dell’ospite a cui potesse legarsi. Hanno scoperto che Chp2 si attacca direttamente a una specifica parte della V-ATPasi, una subunità chiamata ATP6V1E1 (indicata brevemente come E1), che aiuta a stabilizzare la struttura della pompa. Aumentare la quantità di E1 nelle cellule potenziava l’acidificazione lisosomiale e rendeva più difficile la sopravvivenza di Mtb, mentre la riduzione di E1 aveva l’effetto opposto. Topi portatori di una sola copia funzionante del gene E1 avevano lisosomi meno acidi, carichi batterici più elevati nei polmoni e danni tissutali più gravi dopo l’infezione, dimostrando che E1 è un importante difensore dell’ospite contro la tubercolosi.
Un marcatore da chinasi sulla pompa che attenua l’acidità
Gli autori si sono poi chiesti se “etichette” chimiche su E1 potessero modulare l’attività della pompa. Hanno scoperto che l’aggiunta di gruppi fosfato a due specifici residui tirosina (Tyr56 e Tyr57) su E1 funziona come un freno: la mimica della fosforilazione riduceva l’acidificazione e impediva l’assemblaggio completo della V-ATPasi, mentre l’impedimento della fosforilazione aveva l’effetto opposto. Attraverso uno screening di un pannello di enzimi, hanno identificato una chinasi chiamata BMX come la proteina dell’ospite che pone questa etichetta. Quando BMX è stato bloccato geneticamente o con un inibitore di piccola molecola, la fosforilazione di E1 è diminuita, la pompa si è assemblata più efficacemente sulle membrane lisosomiali, i lisosomi sono diventati più acidi e la sopravvivenza di Mtb all’interno dei macrofagi è diminuita.
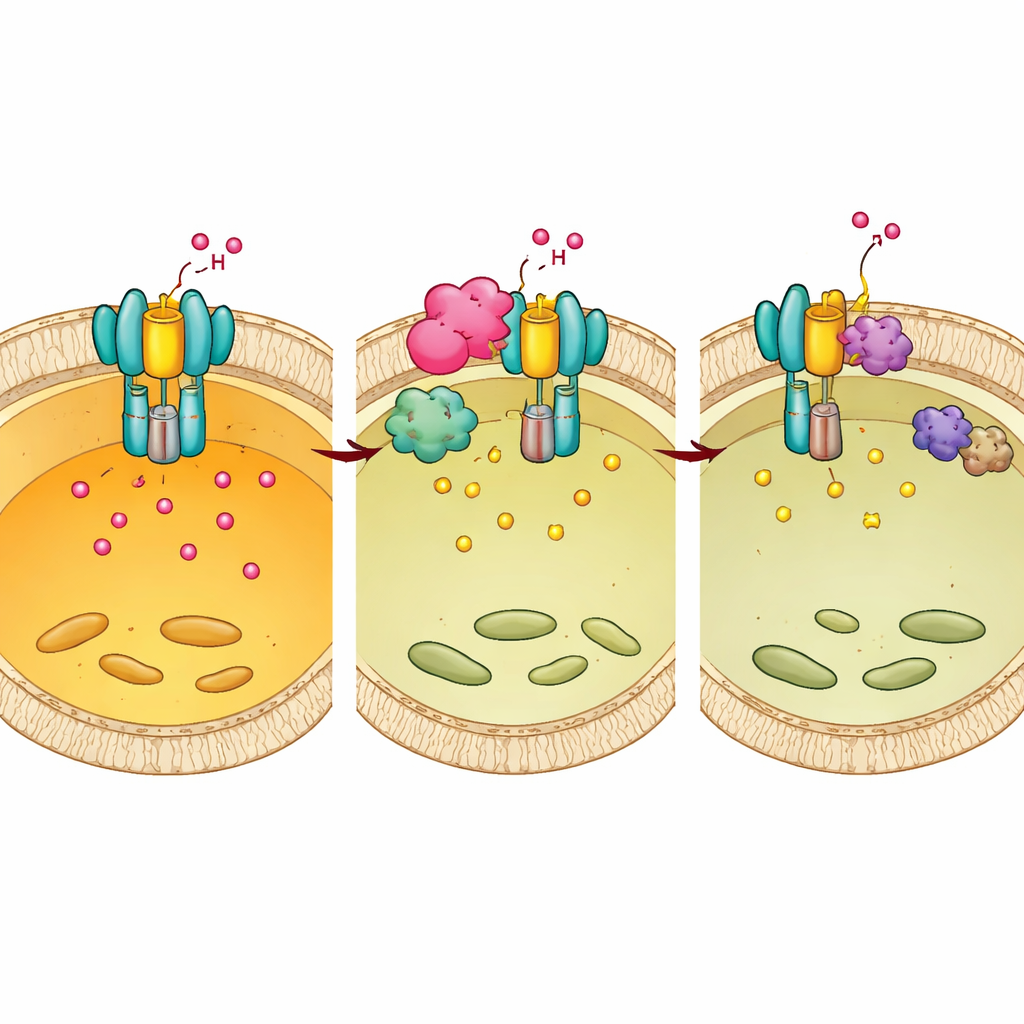
Come Mtb riorganizza l’interruttore dell’ospite a suo favore
Chp2 e BMX risultano lavorare insieme. Esperimenti strutturali e biochimici hanno mostrato che Chp2 funge da impalcatura che avvicina E1 e BMX sulla superficie lisosomiale, aumentando la fosforilazione di E1 su Tyr56/57. Questa marcatura aggiuntiva ostacola l’assemblaggio completo della pompa, innalza il pH lisosomiale e crea un ambiente più mite in cui Mtb può persistere. Quando BMX è stato inibito, il vantaggio di sopravvivenza conferito da Chp2 è scomparso, sia nelle cellule in coltura sia nei topi infettati. Importante, il trattamento dei topi con l’inibitore di BMX dopo l’infezione ha ridotto i carichi batterici e la patologia polmonare negli animali normali, ma non nei topi con E1 indebolito, indicando che il farmaco agisce ripristinando l’efficace acidificazione guidata da E1.
Trasformare l’inganno del patogeno in un’idea terapeutica
In termini concreti, questo studio mostra che i batteri della tubercolosi inseriscono una proteina helper nelle nostre cellule che interfere con la “pompa acida” del sistema di smaltimento, attenuandola quel tanto che basta perché i microrganismi sopravvivano alla degradazione. Identificando la subunità della pompa che funge da manopola di controllo (E1) e l’enzima dell’ospite che la attiva (BMX), gli autori rivelano un punto preciso in cui un farmaco può intervenire. Inibire BMX nei topi riattiva efficacemente il bagno acido intracellulare e migliora la clearance batterica. Questi risultati aprono la strada a terapie dirette sull’ospite che rendono le nostre cellule più ostili a Mtb, potenzialmente da usare insieme agli antibiotici e utili nel contrastare la tubercolosi resistente ai farmaci.
Citazione: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Parole chiave: tubercolosi, lisosomi, terapia diretta sull'ospite, Mycobacterium tuberculosis, V-ATPasi