Clear Sky Science · it
Sviluppo di un potente anticorpo monoclonale per il trattamento delle infezioni da metapneumovirus umano
Perché conta un virus nascosto dell’inverno
Ogni stagione di raffreddori e influenze, un virus poco noto chiamato metapneumovirus umano (HMPV) manda silenziosamente milioni di bambini piccoli, anziani e persone con sistemi immunitari indeboliti nelle cliniche e negli ospedali. A differenza del suo parente virale, il virus respiratorio sinciziale (RSV), non esistono vaccini o trattamenti mirati per l’HMPV. Questo studio riporta la scoperta di un potente anticorpo prodotto in laboratorio, chiamato 4F11, che può bloccare l’HMPV nelle cellule e proteggere animali infetti, indicando la strada verso un nuovo farmaco molto atteso per alcuni dei pazienti più vulnerabili.
Il virus che sfugge al radar
L’HMPV è un comune virus respiratorio presente in tutto il mondo, responsabile di una stima di 14 milioni di infezioni delle vie aeree inferiori nei bambini sotto i cinque anni ogni anno, e provoca anche un notevole tributo negli adulti sopra i 60 anni. Per i pazienti il cui sistema immunitario è gravemente compromesso — come i riceventi di trapianto di cellule staminali — il tasso di mortalità per infezioni polmonari da HMPV può essere allarmantemente alto. I vaccini stanno solo emergendo per virus correlati come l’RSV e, anche se esistesse un vaccino per l’HMPV, molti pazienti altamente immunocompromessi risponderebbero male. A causa di questa lacuna, i ricercatori si stanno orientando verso gli anticorpi monoclonali — proteine immunitarie mirate che possono essere somministrate come farmaci — per prevenire o trattare infezioni gravi.
Alla ricerca di un anticorpo protettivo eccezionale
Il team ha cercato di trovare un anticorpo con tre caratteristiche chiave: doveva essere estremamente potente, funzionare contro molti diversi ceppi di HMPV e lasciare al virus poco spazio per sviluppare resistenza. Si sono concentrati sulla proteina di fusione del virus, una struttura caricata a molla sulla superficie virale che deve cambiare forma per permettere al virus di fondersi ed entrare nelle cellule polmonari. Usando una strategia di “esca e cambio”, hanno selezionato rare cellule B umane da campioni di sangue e milza che potevano riconoscere un ceppo di HMPV ma neutralizzarne un altro, arricchendo anticorpi ad azione ampia. Su oltre mille cellule candidate, hanno isolato tre anticorpi promettenti e hanno scoperto che uno — 4F11 — era eccezionalmente potente, bloccando l’infezione cellulare a concentrazioni quasi 50 volte inferiori rispetto a un anticorpo leader precedente e funzionando contro i quattro principali sottotipi globali di HMPV.
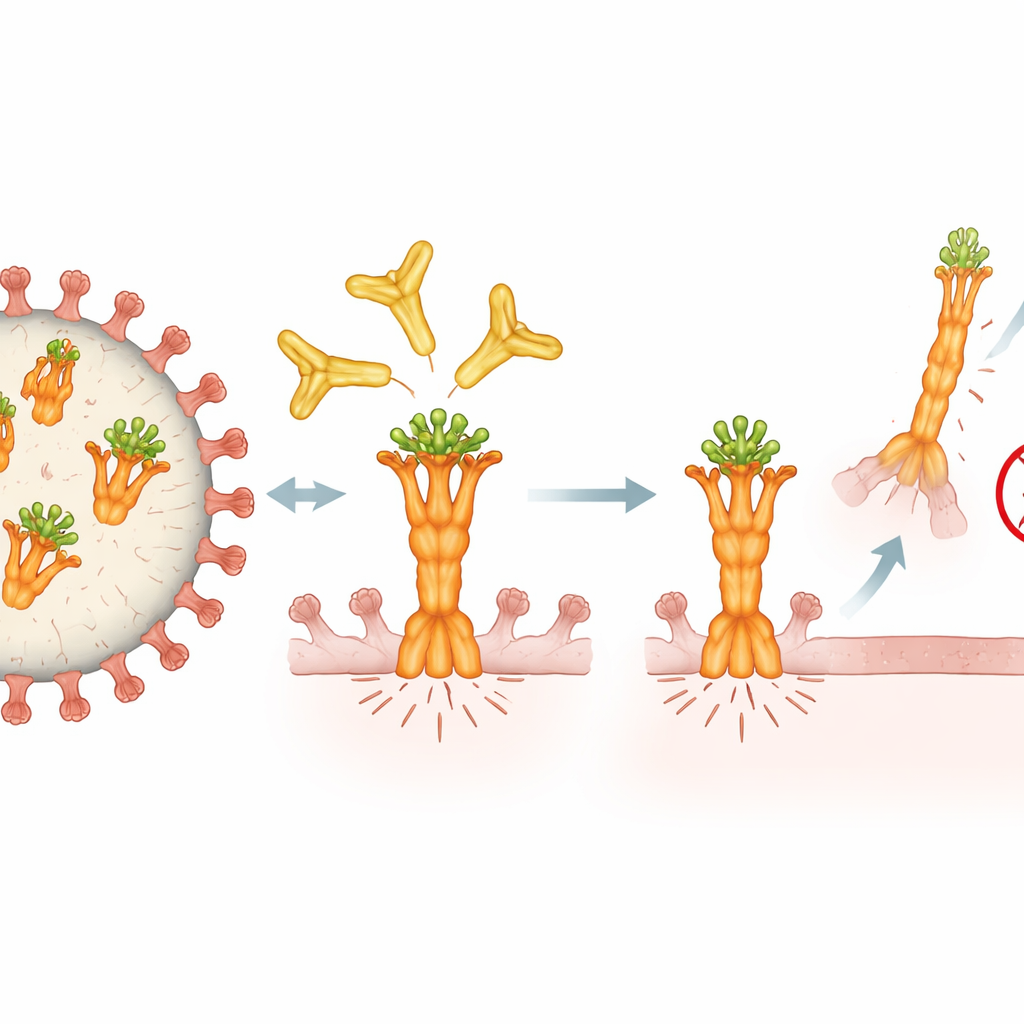
Come 4F11 afferra il punto debole del virus
Per capire perché 4F11 è così efficace, i ricercatori hanno usato la criomicroscopia elettronica ad alta risoluzione per visualizzare come si leghi alla proteina di fusione. Hanno scoperto che 4F11 prende di mira una piccola patch conservata sulla sommità della forma prefusione della proteina — la molla prima dello scatto. A differenza di altri anticorpi che si legano tre copie per ogni proteina di fusione, 4F11 si posiziona da sola all’apice in un rapporto uno a uno, puntando verso il basso e arrivando persino ad afferrare una decorazione zuccherina che protegge la superficie. Questo insolito angolo di legame e la dipendenza da quello zucchero rendono 4F11 un tipo d’anticorpo unico. Riconosce solo la forma prefusione, presente sul virus infettante, e probabilmente impedisce alla proteina di ripiegarsi nella conformazione necessaria per perforare e fondersi con la cellula ospite.
Il virus può sfuggire — e a quale costo?
Il team ha quindi costretto il virus a crescere in coltura cellulare in presenza costante di 4F11 per vedere quanto facilmente potesse evolvere una via di fuga. Rispetto a un altro anticorpo di controllo, che ha rapidamente favorito l’emergere di diverse mutazioni di fuga, l’HMPV ha avuto molto più difficoltà a eludere 4F11. Solo un singolo cambiamento nella proteina di fusione, che altera un amminoacido in posizione 179, ha interrotto completamente il legame di 4F11. Tuttavia, i virus portatori di questa mutazione crescevano molto peggio rispetto al virus normale, indicando un serio danno alla fitness virale. Ricerche nei database di centinaia di sequenze di HMPV hanno mostrato che questa modifica dannosa non è mai stata osservata in natura, suggerendo che sebbene il virus possa, in linea di principio, sfuggire a 4F11 in laboratorio, ne paga un prezzo così alto in termini di crescita che è improbabile che si diffonda ampiamente nel mondo reale.
Testare la protezione in un modello animale
La potenza in laboratorio deve comunque tradursi in protezione reale. Per testarlo, i ricercatori hanno infettato criceti siriani dorati con HMPV e poi, un giorno dopo, li hanno trattati con 4F11 — imitando una terapia precoce piuttosto che una prevenzione. Una singola iniezione a basso dosaggio di 4F11 ha ridotto nettamente i livelli di virus sia nei polmoni sia nelle vie nasali e, alla dose più alta, ha eliminato completamente il virus rilevabile nei polmoni nella maggior parte degli animali. È notevole che queste dosi fossero inferiori a quelle usate per diversi anticorpi monoclonali già approvati per l’RSV nell’uomo. Al contrario, un anticorpo descritto in precedenza, in grado di reagire con più virus, ha offerto scarsa protezione alla stessa dose, mettendo in risalto la forza specifica di 4F11 come terapia mirata per l’HMPV.
Cosa potrebbe significare per i pazienti
Nel complesso, questi risultati pongono 4F11 come un forte candidato per lo sviluppo clinico. Combina alta potenza, ampia copertura dei ceppi HMPV circolanti, un modo distintivo di legare una regione vulnerabile della proteina di fusione e un panorama di resistenza in cui la via di fuga ovvia per il virus comporta un notevole svantaggio per se stesso. Per neonati, anziani e pazienti immunocompromessi a rischio elevato di malattia grave da HMPV, un farmaco basato su 4F11 potrebbe un giorno offrire sia un trattamento d’emergenza dopo l’infezione sia una protezione aggiuntiva insieme o in alternativa ai vaccini.
Citazione: Harris, E.D., McGovern, M., Pernikoff, S. et al. Development of a potent monoclonal antibody for treatment of human metapneumovirus infections. Nat Commun 17, 2714 (2026). https://doi.org/10.1038/s41467-026-69328-w
Parole chiave: metapneumovirus umano, anticorpo monoclonale, infezione respiratoria, proteina di fusione, terapia antivirale