Clear Sky Science · it
La rete neuronale preottica kisspeptin-nNOS-GnRH (KiNG) regola la ritmicità dell’LH tramite attivazione-inibizione nei topi
Perché questa storia cerebrale è importante per la fertilità
L’ovulazione e la fertilità dipendono da un piccolo gruppo di cellule cerebrali che rilasciano un ormone maestro a impulsi e in occasionali picchi. Quando questo timing si altera, la riproduzione può fallire. Questo studio rivela come due tipi di molecole di segnalazione nel cervello del topo, una che attiva l’attività e l’altra che la spegne discretamente, cooperino per modellare questi ritmi ormonali. Comprendere questo circuito temporale nascosto potrebbe, in futuro, aiutare a spiegare alcune forme di infertilità e suggerire nuovi modi per trattare i disturbi riproduttivi.
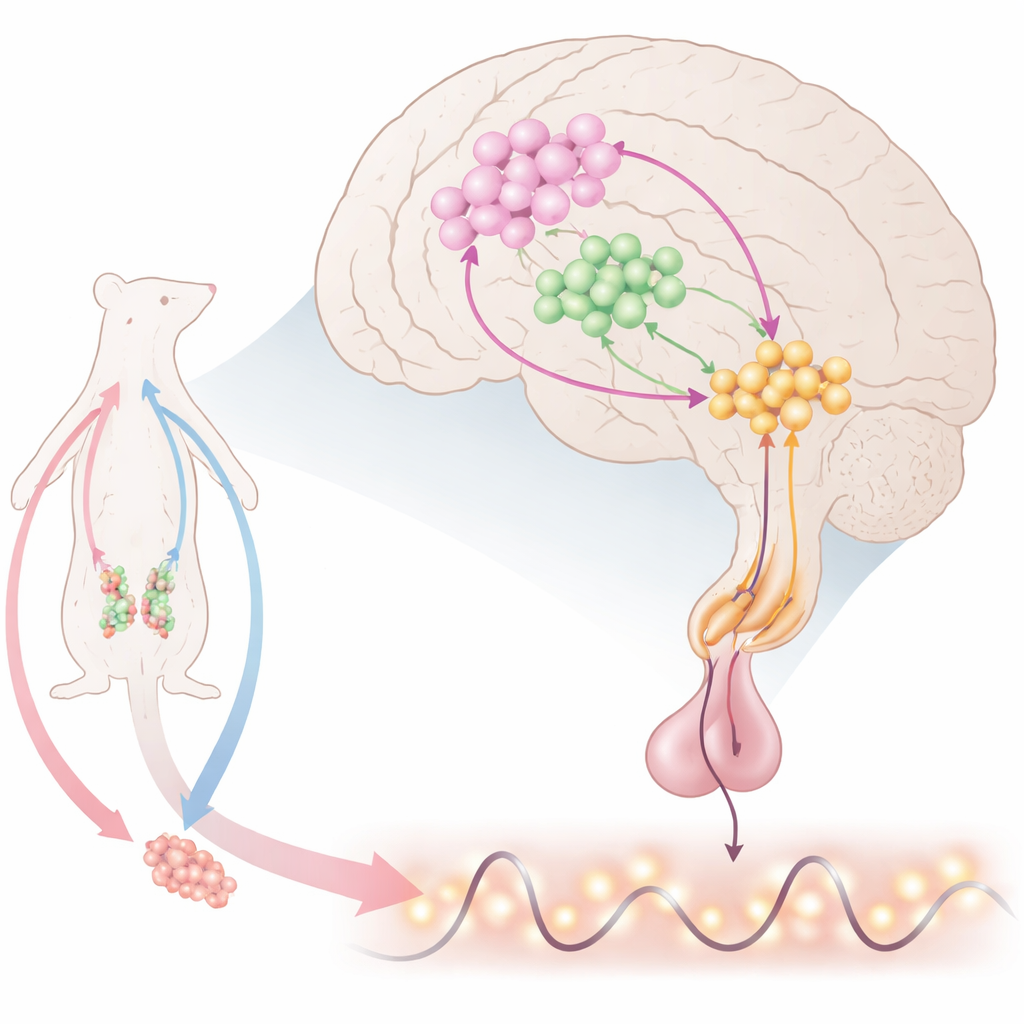
Il cronometrista cerebrale per la riproduzione
In profondità nel cervello, cellule nervose specializzate rilasciano l’ormone di rilascio delle gonadotropine (GnRH), che istruisce la ghiandola pituitaria a immettere luteinizzante (LH) e follicolo-stimolante. Questi, a loro volta, controllano ovaie e testicoli. Il GnRH non viene rilasciato in modo costante; si manifesta piuttosto come impulsi regolari e, nelle femmine, come un ampio picco pre-ovulatorio. Gli scienziati sanno che molti segnali arrivano alle cellule GnRH, ma la combinazione esatta che genera sia impulsi sia picchi è rimasta poco chiara. Questo lavoro si concentra su una piccola regione nella parte anteriore dell’ipotalamo, dove le cellule GnRH si mescolano con altri due protagonisti importanti: neuroni produttori di kisspeptina che eccitano il GnRH, e neuroni che producono ossido nitrico (NO), un segnale gassoso che può diffondersi su brevi distanze.
Una partnership acceso–spento tra due segnali
I ricercatori propongono una rete “KiNG” a tre componenti, composta da kisspeptina, neuroni produttori di NO (nNOS) e cellule GnRH. La kisspeptina è un potente attivatore che può indurre il rilascio di GnRH e LH, ma una stimolazione costante finisce per spegnere il sistema, suggerendo la necessità di un freno interno. Utilizzando sonde molecolari altamente sensibili, strumenti genetici e registrazioni in fette di cervello nei topi, il team mostra che la kisspeptina fa più che eccitare direttamente i neuroni GnRH. Essa attiva anche i vicini neuroni nNOS nell’area preottica, soprattutto in una regione chiamata OV/MePO. Quando i livelli di kisspeptina aumentano, questi neuroni nNOS producono raffiche di NO, che innescano la produzione di un secondo messaggero, il cGMP, nelle cellule circostanti, incluse le stesse cellule GnRH. Questo segnale NO–cGMP attenua il firing del GnRH, fornendo un interruttore di spegnimento incorporato alla spinta della kisspeptina.
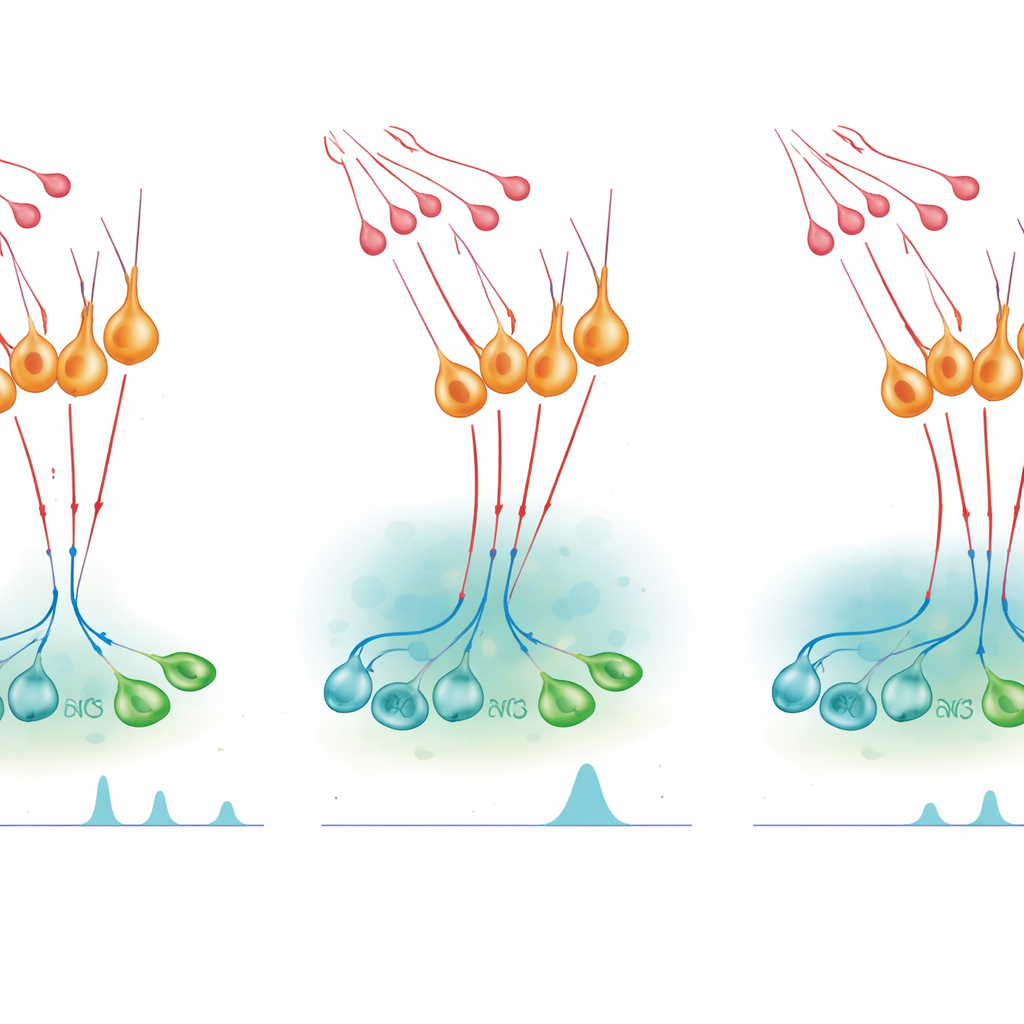
Accendere i picchi ormonali e contenerli
Per testare come questo microcircuito influenzi il rilascio ormonale, il team ha usato interruttori chemogenetici — recettori ingegnerizzati attivati da un farmaco altrimenti inattivo — per accendere o spegnere i neuroni nNOS nei topi vivi. L’attivazione artificiale delle cellule nNOS durante una fase normalmente tranquilla del ciclo femminile è stata sufficiente a produrre un aumento simile a un picco di LH nel sangue, e lo stesso è avvenuto nei maschi. Bloccare la produzione di NO ha cancellato questo effetto, mostrando che il NO di questi neuroni è necessario per il picco. Eppure, quando gli scienziati hanno inibito i neuroni nNOS o ridotto la loro sensibilità alla kisspeptina, una somministrazione di kisspeptina ha prodotto un aumento di LH esagerato e prolungato. Farmaci che bloccano la sintesi di NO hanno avuto un effetto amplificante simile, mentre un farmaco che prolunga la segnalazione del cGMP ha ridotto la durata della risposta alla kisspeptina e diminuito il rilascio successivo di LH. Insieme, questi esperimenti indicano che il NO aiuta sia a sincronizzare i neuroni GnRH per generare i picchi sia a limitarne la durata durante la stimolazione da kisspeptina.
Un ritmo flessibile durante il ciclo ovarico
Lo studio rivela anche che questo equilibrio acceso–spento cambia nel corso del ciclo femminile. Utilizzando un metodo sensibile di rilevamento dell’RNA, gli autori hanno trovato che più neuroni nNOS esprimono il recettore della kisspeptina il giorno prima dell’ovulazione, quando i livelli di estrogeni sono alti e si verifica il picco di LH. Durante le fasi più tranquille, meno neuroni nNOS rispondono alla kisspeptina, producendo solo piccole quantità locali di NO che trattengono delicatamente gli impulsi di GnRH senza fermarli. Nel giorno del picco, un input di kisspeptina più forte e un’aumentata espressione recettoriale potenziano massicciamente la produzione di NO, permettendo al NO di diffondersi più lontano e di silenziare brevemente molti neuroni GnRH contemporaneamente. Quando il segnale NO si affievolisce, queste cellule rimbalzano insieme, generando il grande e coordinato picco di LH necessario per l’ovulazione.
Cosa significa per la salute umana
In termini semplici, questo lavoro mostra che lo stesso segnale che avvia i neuroni GnRH — la kisspeptina — recluta anche un sistema di frenata ritardato tramite il NO, assicurando che gli scoppi ormonali siano forti ma non incontrollati. La rete KiNG agisce dunque sia come acceleratore sia come freno per la temporizzazione riproduttiva, sintonizzando gli impulsi di GnRH nella maggior parte del ciclo e modellando il picco che innesca l’ovulazione. Poiché alterazioni genetiche nelle vie della kisspeptina e del NO sono state trovate in persone con problemi riproduttivi, comprendere questo circuito finemente bilanciato potrebbe orientare nuovi approcci per diagnosticare e trattare infertilità e condizioni correlate.
Citazione: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Parole chiave: ormoni riproduttivi, ipotalamo, kisspeptina, ossido nitrico, tempistica dell’ovulazione