Clear Sky Science · it
La lattilazione delle istoni aumenta l’espressione di CXCL1 per l’infiltrazione dei neutrofili e l’evasione immunitaria nel cancro pancreatico
Perché questo studio sul cancro è importante
Il cancro pancreatico è uno dei tumori più letali, in parte perché spesso resiste alle immunoterapie moderne efficaci in altri tumori. Questo studio rivela come i tumori pancreatici rimodulino il proprio metabolismo degli zuccheri per disarmare silenziosamente il sistema immunitario, e come bloccare quel processo possa riaprire una strada affinché le difese dell’organismo — e farmaci esistenti — possano reagire.
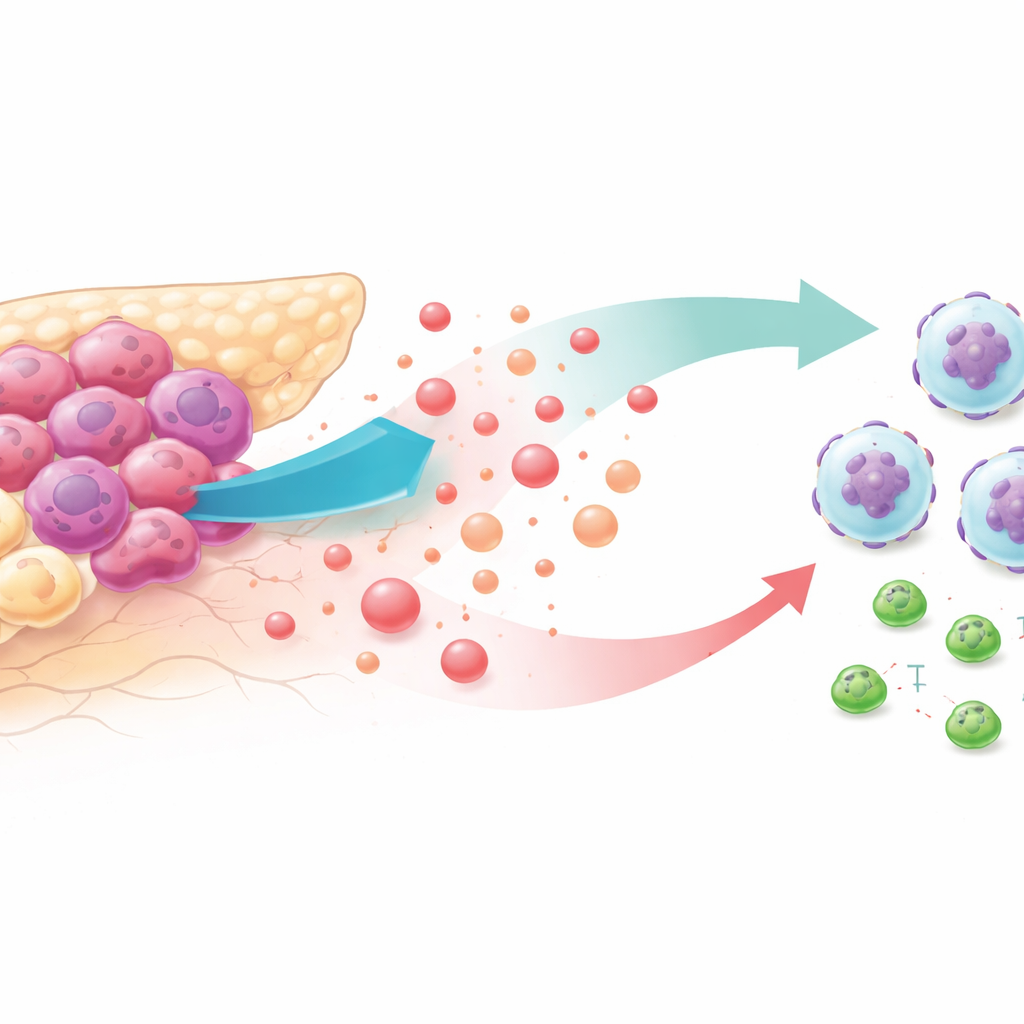
Tumori affamati di zucchero e un quartiere ostile
Le cellule tumorali sono note per consumare glucosio a ritmi elevati, anche quando l’ossigeno è disponibile. Questo stile di vita ad «alta glicolisi» inonda il microambiente tumorale di lattato, un sottoprodotto una volta considerato solo rifiuto metabolico. Analizzando banche dati di tumori di pazienti e modelli murini, i ricercatori hanno scoperto che i tumori pancreatici con la glicolisi più intensa erano ricchi di neutrofili — globuli bianchi che, in questo contesto, favoriscono la crescita tumorale — e presentavano meno cellule T CD8 citotossiche. I pazienti i cui tumori mostravano questo profilo tendevano ad avere una sopravvivenza più breve, suggerendo che metabolismo alterato ed evasione immunitaria sono strettamente collegati.
Come i tumori usano il lattato per richiamare il tipo sbagliato di aiuto
Per capire come la glicolisi attragga i neutrofili, il team ha ridotto la glicolisi tumorale con farmaci o con strategie genetiche in linee cellulari di cancro pancreatico e nei topi. Quando la degradazione dello zucchero era bloccata, le cellule tumorali rilasciavano molto meno un segnale chimico chiamato CXCL1, e i livelli circolanti di questo segnale calavano nei topi e nei campioni di pazienti. In test di migrazione in vitro, i neutrofili si spostavano con vivacità verso il mezzo proveniente da cellule tumorali altamente glicolitiche, ma non verso il mezzo di cellule con glicolisi bloccata — a meno che i ricercatori non aggiungessero di nuovo CXCL1 purificato. In topi vivi, il ripristino di CXCL1 in tumori con glicolisi ridotta riportava i neutrofili ai livelli precedenti e indeboliva l’effetto antitumorale dell’inibizione della glicolisi.
Un nuovo interruttore epigenetico guidato dal lattato
Lo studio è poi sceso al livello del packaging del DNA. I nostri geni sono avvolti attorno a proteine a bobina chiamate istoni, i cui tag chimici funzionano come interruttori di attivazione o repressione genica. Gli autori dimostrano che nel cancro pancreatico il lattato prodotto dalla glicolisi aggiunge un tag specifico «lattile» in una posizione dell’istone nota come H3K18. Questa modifica, chiamata lattilazione dell’istone H3K18, risultava marcatamente più elevata nei tessuti tumorali rispetto al pancreas normale. Quando la glicolisi veniva bloccata, la lattilazione in H3K18 diminuiva, soprattutto vicino alla regione di controllo del gene CXCL1, e la produzione di CXCL1 calava. Il reintegro di lattato ripristinava sia il tag sugli istoni sia l’espressione di CXCL1. Nei campioni dei pazienti, i tumori con maggiore lattilazione in H3K18 mostravano anche livelli più alti di CXCL1, collegando questo marchio molecolare a un paesaggio immunitario pro‑tumorale.
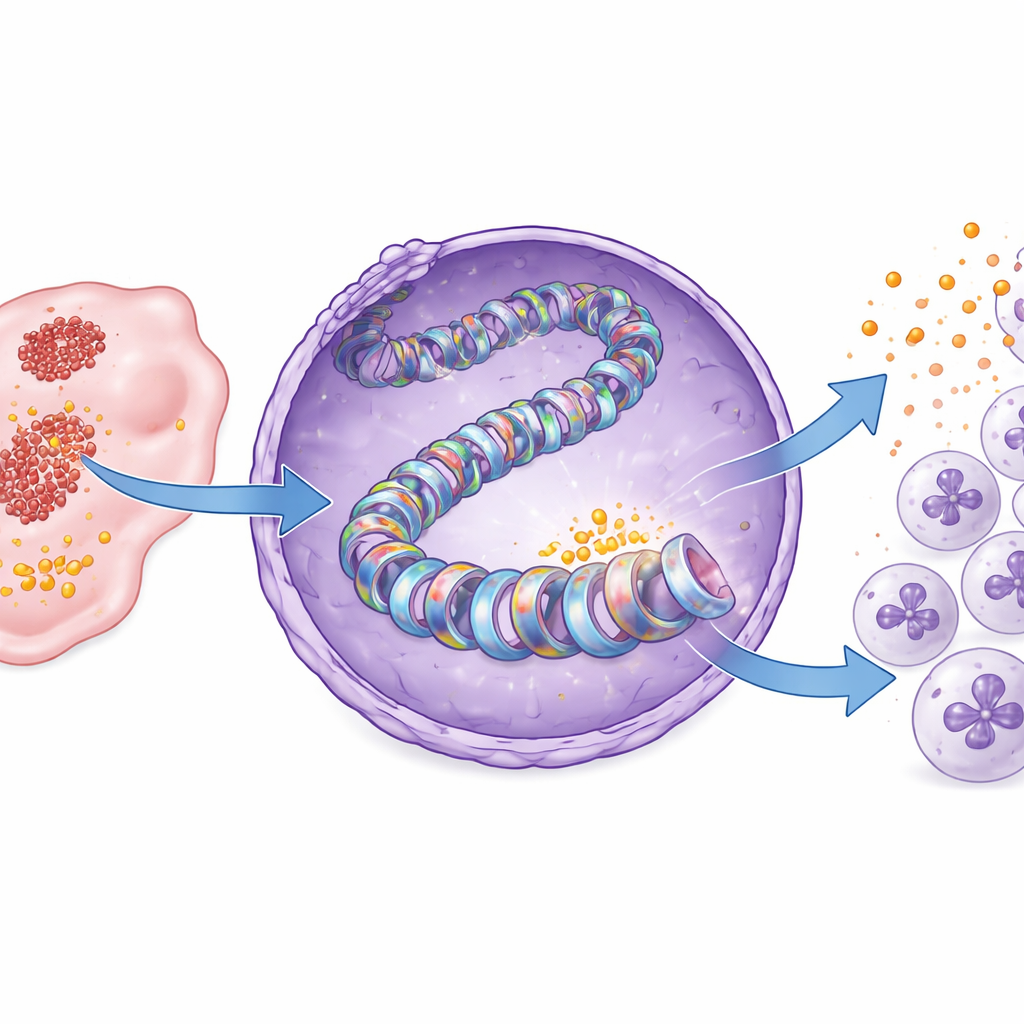
Identificazione dell’enzima e di un punto debole farmacologico
I tag sugli istoni sono scritti da enzimi specializzati. Screening di inibitori di proteine note per modificare gli istoni ha permesso ai ricercatori di individuare un enzima chiamato PCAF come scrittore chiave della lattilazione in H3K18 nel cancro pancreatico. Modellazione strutturale ha suggerito che PCAF può legare il lattil‑CoA, la forma attivata del lattato usata per il tagging, e saggi biochimici hanno confermato che la PCAF purificata può aggiungere direttamente gruppi lattile all’istone H3. Bloccare PCAF con una piccola molecola, bromosporina, riduceva la lattilazione in H3K18 e la produzione di CXCL1 nelle cellule tumorali e nei tumori murini. Di conseguenza, meno neutrofili entravano nei tumori, più cellule T CD8 si accumulavano e la crescita tumorale rallentava, il tutto senza perdita di peso evidente o tossicità nei topi.
Rendere un tumore «freddo» più «caldo» con la terapia combinata
Poiché farmaci anti‑checkpoint immunitario standard come gli anticorpi anti–PD‑1 hanno mostrato un successo limitato nel cancro pancreatico, il team ha testato se smantellare la via lattato–PCAF–CXCL1 potesse rendere questi tumori più sensibili. In modelli murini sia sottocutanei sia ortotopici pancreatici, la combinazione di bromosporina con terapia anti–PD‑1 ha ridotto i tumori più di ciascun trattamento singolarmente, diminuito l’infiltrazione di neutrofili, aumentato le cellule T CD8 attive e prolungato significativamente la sopravvivenza. Questo suggerisce che tagliare la «sirena» metabolica del tumore per i neutrofili aiuta a trasformare un tumore immunologicamente «freddo» in uno «più caldo» con cui la terapia di checkpoint può interagire meglio.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio rivela una reazione a catena: i tumori pancreatici bruciano zucchero, rilasciano lattato, usano quel lattato per azionare un interruttore epigenetico sulle loro proteine di impacchettamento del DNA, aumentano CXCL1 e così richiamano neutrofili che li aiutano a nascondersi dalle cellule T citotossiche. Interrompere questa catena al livello di PCAF con un farmaco non solo rallenta i tumori ma rende anche più efficace l’immunoterapia esistente nei topi. Sebbene siano necessari ulteriori studi per garantire la sicurezza e trovare il modo migliore per mirare questa via negli esseri umani, questi risultati mettono in luce una strategia promettente: riprogrammar e il metabolismo e gli interruttori genetici del tumore per dare al sistema immunitario una possibilità più equa.
Citazione: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Parole chiave: cancro pancreatic o, metabolismo tumorale, lattilazione delle istoni, microambiente tumorale, immunoterapia oncologica