Clear Sky Science · it
Scoperta di peptidi antimicrobici che prendono di mira Acinetobacter baumannii tramite una pipeline basata su few‑shot learning pre‑addestrata e fine‑tuned
Perché questo conta per la salute di tutti i giorni
Le infezioni resistenti ai farmaci stanno aumentando così rapidamente che, entro metà secolo, potrebbero uccidere più persone ogni anno del cancro. Uno dei colpevoli più preoccupanti è Acinetobacter baumannii, un temibile germe ospedaliero che resiste a molti antibiotici e infetta spesso pazienti con ventilatori. Questo studio mostra come gli scienziati abbiano combinato l’intelligenza artificiale con esperimenti di laboratorio per scoprire rapidamente nuovi piccoli candidati farmacologici in grado di uccidere questo batterio causando molto meno danno all’organismo rispetto all’attuale farmaco di ultima istanza.
Un superbatterio ospedaliero difficile da eliminare
Acinetobacter baumannii è un batterio Gram‑negativo che prospera nelle unità di terapia intensiva, in particolare nei pazienti dipendenti dai ventilatori. Il suo involucro esterno robusto e il genoma che evolve rapidamente lo rendono resistente a molti antibiotici standard. Oggi una delle poche opzioni rimaste è un farmaco chiamato polimixina B, ma può danneggiare gravemente i reni e il batterio può comunque sviluppare resistenza. Allo stesso tempo, una classe promettente di piccoli frammenti proteici chiamati peptidi antimicrobici è stata esplorata contro altri microrganismi, ma sono stati trovati molto pochi peptidi che funzionino specificamente e bene su A. baumannii. I metodi tradizionali di screening per tentativi ed errori sono semplicemente troppo lenti e costosi per setacciare il numero astronomico di possibili sequenze peptidiche corte.
Usare algoritmi intelligenti per cercare in uno spazio enorme
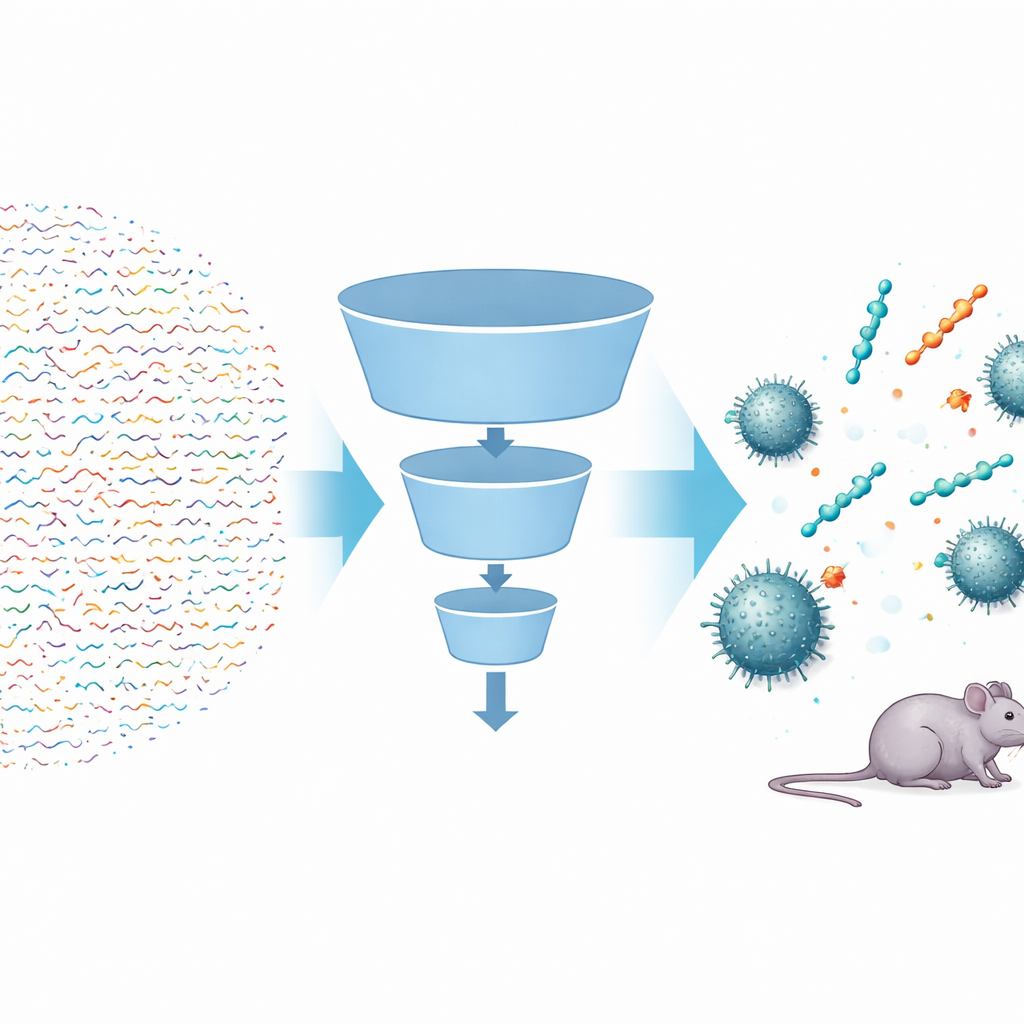
I ricercatori hanno costruito una pipeline di intelligenza artificiale a più passaggi, chiamata FSLSMEP, per esaminare intere librerie di peptidi brevi—quelli con sei, sette o otto unità costitutive—che ammontano a decine di miliardi di candidati. La sfida era che disponevano di sole 148 sequenze note attive contro A. baumannii, molto poche per i metodi standard di machine learning. Per aggirare questo limite, hanno iniziato con un potente modello pre‑addestrato che aveva già “letto” centinaia di milioni di sequenze proteiche naturali e appreso regole generali sul comportamento di tali molecole. Hanno poi affinato (fine‑tuned) questo modello in due fasi: prima su un set più ampio di peptidi attivi contro un batterio correlato, Pseudomonas aeruginosa, e infine sui dati scarsi relativi ad A. baumannii. Lungo il percorso, tre moduli collegati—uno per separare i peptidi probabili da quelli improbabili, uno per classificarli e uno per stimare quanto ciascuno potesse essere potente—hanno funzionato come filtri successivi in un imbuto.
Dalle previsioni al computer ai successi in provetta
Dopo aver scartato inizialmente i peptidi meno promettenti usando semplici regole chimiche, il team ha inviato quasi quattro milioni di candidati nella pipeline. Il classificatore ha eliminato la maggior parte delle sequenze che non sembravano antimicrobiche; il modello di ranking ha favorito quelle le cui caratteristiche suggerivano forte attività; e il modello di regressione ha predetto la concentrazione minima di farmaco necessaria per arrestare la crescita batterica. Da sessantaquattro milioni di peptidi a sei unità, il sistema ha proposto solo dieci candidati migliori. Quando sintetizzati e testati in laboratorio, nove di questi hanno mostrato reale attività antibatterica, un tasso di successo notevole nella scoperta di farmaci. Gli stessi modelli addestrati sono stati poi applicati, senza riaddestramento, a spazi di peptidi molto più grandi a sette e otto unità, dai quali i ricercatori hanno scelto ulteriori sequenze top‑ranked da testare. Di nuovo, la maggior parte si è rivelata attiva, incluse eptapeptidi tanto potenti quanto la polimixina B contro alcuni ceppi.
Uccidono con potenza ma con un tocco più gentile
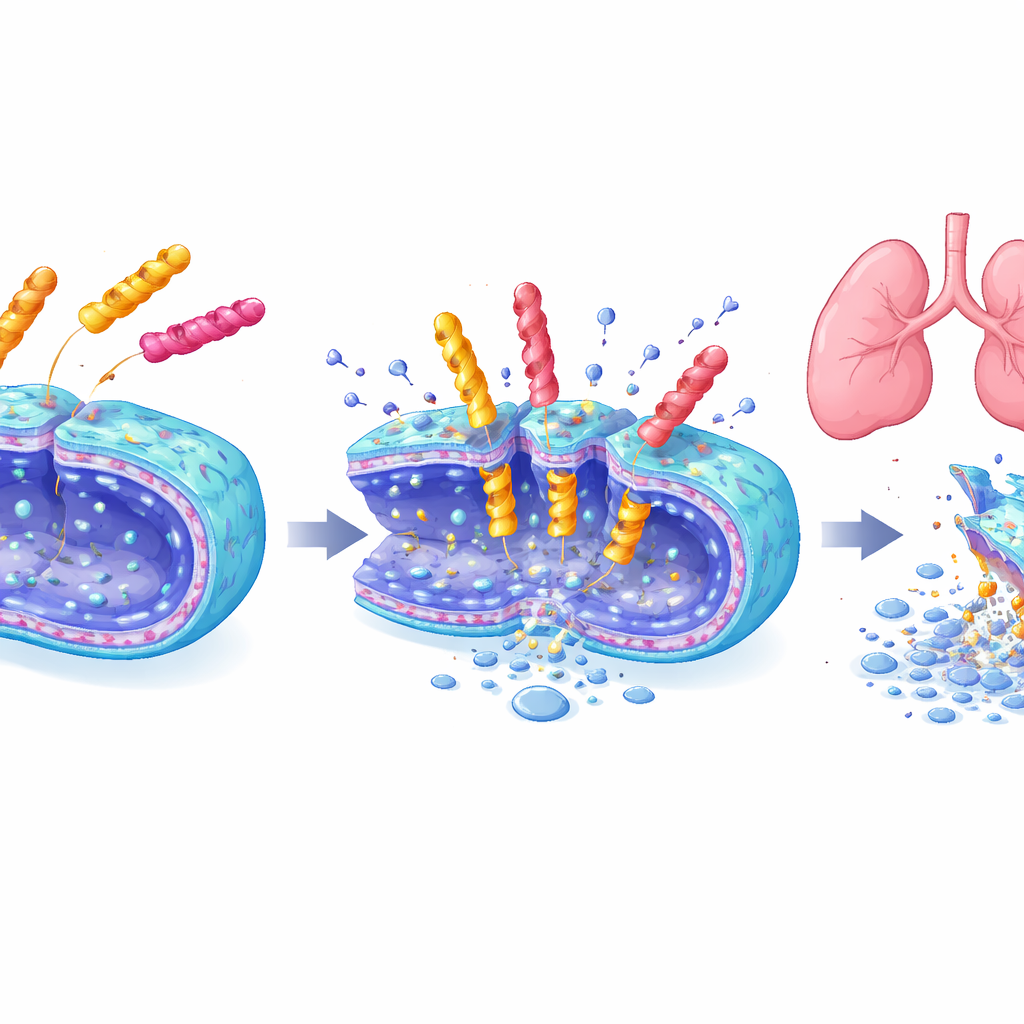
Tre peptidi guida—uno ciascuno dalle librerie a sei, sette e otto unità—sono stati esaminati in dettaglio. Hanno rapidamente eliminato popolazioni di A. baumannii in pochi minuti o ore, danneggiato le membrane batteriche come osservato al microscopio elettronico e hanno funzionato anche su altri microrganismi pericolosi. Allo stesso tempo, hanno causato pochi danni a cellule di mammifero in coltura o ai globuli rossi, a differenza di alcuni peptidi antimicrobici esistenti. Nei test di esposizione a lungo termine, i batteri non hanno sviluppato facilmente resistenza a queste nuove molecole, mentre la resistenza alla polimixina B è aumentata rapidamente. In modo particolarmente evidente, in un modello murino di polmonite, una dose inalata dell’eptapeptide EME7(7) ha eliminato le infezioni polmonari con la stessa efficacia della polimixina B ma non ha danneggiato i reni, mentre la polimixina B ha provocato chiari danni renali e incrementi nei marker ematici di stress renale.
Cosa significa per i medicinali futuri
Questo lavoro dimostra che una pipeline di IA progettata con cura può trasformare un piccolo e incompleto set di dati in un motore potente per scoprire nuovi peptidi antimicrobici. Combinando un ampio pre‑training, un fine‑tuning a fasi e molteplici livelli di filtraggio, i ricercatori hanno esplorato in modo efficiente intere librerie di peptidi corti e trovato candidati che sia combattono un pericoloso superbatterio ospedaliero sia sembrano più sicuri per organi vitali. La stessa strategia ha avuto successo anche nel trovare peptidi attivi contro il patogeno fungino Candida albicans, suggerendo che potrebbe essere riutilizzata per cercare molti altri tipi di peptidi terapeutici. Per i pazienti, questo approccio potrebbe alla fine tradursi in nuovi farmaci che curano infezioni ostinate senza gli effetti collaterali gravi e la rapida insorgenza di resistenza che affliggono gli antibiotici di ultima linea attuali.
Citazione: Huang, J., Zhang, W., Wang, A. et al. Discovery of antimicrobial peptides targeting Acinetobacter baumannii via a pre-trained and fine-tuned few-shot learning-based pipeline. Nat Commun 17, 2475 (2026). https://doi.org/10.1038/s41467-026-69306-2
Parole chiave: peptidi antimicrobici, resistenza agli antibiotici, Acinetobacter baumannii, scoperta di farmaci con machine learning, few‑shot learning