Clear Sky Science · it
Sfruttare la cinetica di legame prevedibile di DNA-PAINT per eliminare il rumore nelle immagini a super-risoluzione
Visioni più nitide del mondo microscopico
I microscopi moderni possono ora “vedere” singole molecole all’interno delle cellule, ma queste immagini sono spesso costellate da punti di fondo fuorvianti. Questo studio presenta un modo per pulire tali immagini sfruttando il modo in cui frammenti di DNA si legano e si staccano nel tempo. Il risultato sono immagini più nitide della macchinaria molecolare all’interno delle cellule, importante per tutto, dalla biologia di base alla scoperta di farmaci.
Come un trucco di lampeggio rivela dettagli nascosti
Un metodo di imaging potente, chiamato DNA-PAINT, trasforma l’adesione casuale di brevi filamenti di DNA in un microscopio a super-risoluzione. Un filamento di DNA è attaccato alla proteina che lo scienziato vuole osservare; un filamento complementare con un colorante fluorescente galleggia nella soluzione. Quando il filamento mobile si lega brevemente al suo partner, produce un piccolo lampo di luce. Registrando molti di questi lampeggi e localizzandone le posizioni, i ricercatori possono ricostruire le posizioni delle proteine con precisione nanometrica—molto più definita rispetto ai microscopi ottici convenzionali.
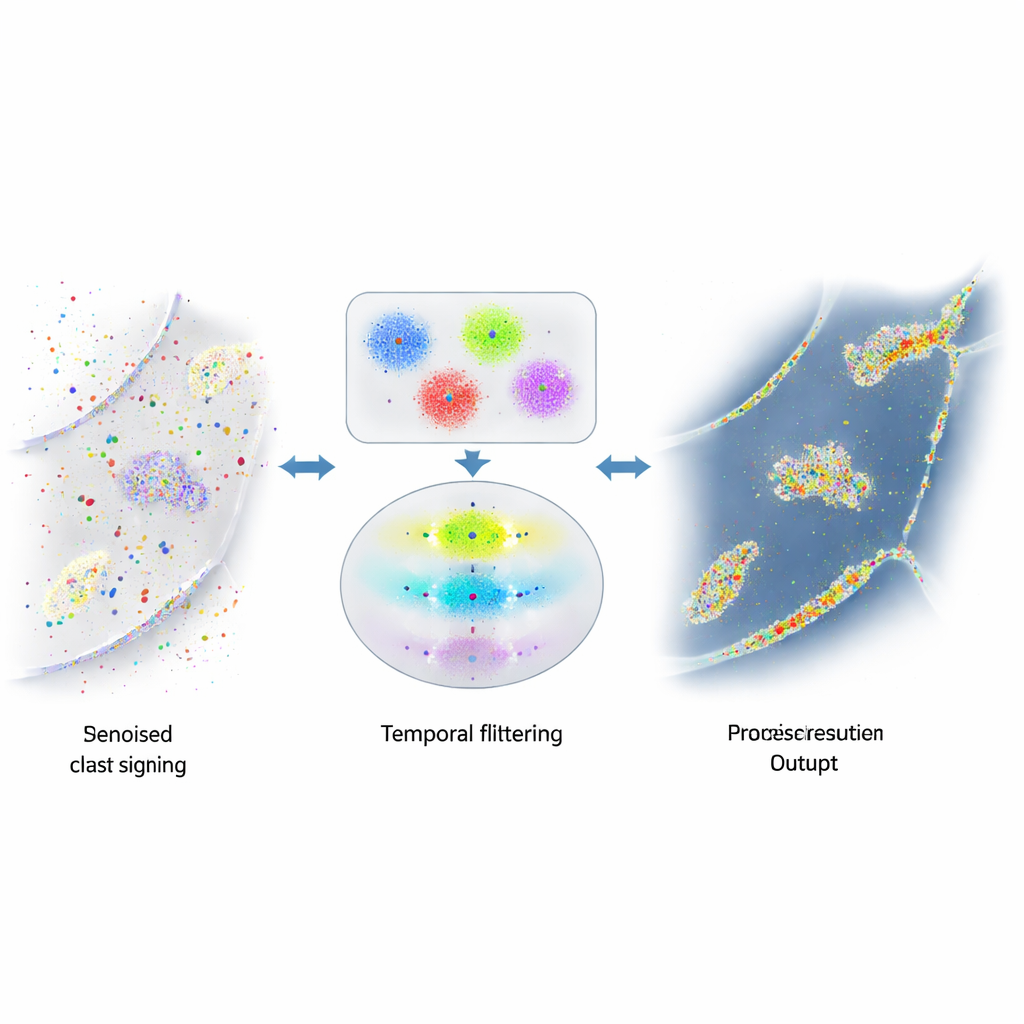
Quando segnali utili sono sepolti nel rumore
Il punto di forza di DNA-PAINT—un gran numero di filamenti fluorescenti liberi—genera anche un problema. Questi filamenti a volte si attaccano dove non dovrebbero, ad esempio a superfici cellulari casuali o al DNA abbondante nel nucleo. Quei lampeggi accidentali sono indistinguibili dall’aspetto da quelli veri e intasano l’immagine finale con punti e ammassi falsi. Tentativi precedenti di ridurre questo rumore si sono concentrati sul cambiare la chimica per rendere meno probabili gli attacchi indesiderati, o su regole approssimative per individuare outlier evidenti. Tuttavia una quantità significativa di segnale fuorviante è rimasta, limitando l’affidabilità delle misure sul numero di proteine o sulle relazioni spaziali.
Usare il tempo per distinguere verità e inganno
Gli autori si sono accorti che le vere coppie di DNA in DNA-PAINT obbediscono a una semplice regola temporale: le pause tra i reali eventi di legame seguono uno schema esponenziale prevedibile. Al contrario, gli eventi di attacco casuale non lo fanno. Hanno costruito un algoritmo a più fasi che prima raggruppa i lampeggi vicini in piccoli cluster basati sulla loro posizione, usando una combinazione di clustering basato sulla densità e k-means per scomporre forme complesse in unità delle dimensioni delle localizzazioni. Per ogni cluster costruiscono quindi una “traccia temporale” degli eventi di legame, fondendo con cura i lampeggi rapidi on-off dallo stesso legame in eventi singoli. Infine applicano un test statistico per verificare se gli intervalli tra gli eventi in ciascun cluster corrispondono al comportamento esponenziale previsto. I cluster che superano il test sono considerati reali; quelli che non lo fanno vengono scartati come rumore.
Mettere il metodo alla prova in cellule reali
Per testare il loro approccio, il team ha immaginato la proteina di adesione cellulare E-caderina nelle camere ovariche della mosca della frutta, dove alcune cellule producevano la proteina taggata e le cellule vicine no. Questo ha creato aree affiancate ricche di segnale genuino e aree che dovrebbero contenere solo fondo. Regolando il numero di eventi di legame che un cluster deve mostrare prima di essere testato, hanno trovato impostazioni che rimuovevano oltre il 90% dei cluster spurii mantenendo più del 98% di quelli veri ai bordi cellulari. Nelle immagini denoised, dettagli fini come sottili strutture tubolari e vescicole sono diventati molto più chiari. La stessa strategia ha funzionato in altri sistemi, incluse mitocondri e microtubuli, e persino su proteine con distribuzioni più diffuse e amorfe, dove solo gli schemi spaziali non danno indizi su cosa sia reale.
Mappe molecolari più nitide per studi futuri
Ascoltando il “ritmo” del legame del DNA invece di limitarsi a osservare dove avvengono i lampeggi, questo metodo elimina in modo affidabile il fondo fuorviante dai dati DNA-PAINT. Per i non specialisti, il risultato chiave è semplice: mappe molecolari più nitide e più affidabili all’interno delle cellule. Ciò rende più sicuro contare il numero di molecole proteiche presenti, valutare quanto vicine siano diverse proteine l’una all’altra e costruire immagini più accurate della vita interna delle cellule. Con la crescita dell’imaging basato sul DNA, questo tipo di denoising intelligente sarà essenziale per trasformare immagini puntinate grezze in solido insight biologico.
Citazione: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
Parole chiave: DNA-PAINT, microscopia a super-risoluzione, denoising delle immagini, imaging a singola molecola, mappatura delle proteine