Clear Sky Science · it
Il fattore genetico dell’encefalopatia necrotizzante acuta, RANBP2, regola la risposta infiammatoria all’infezione da virus dell’influenza A
Quando l’influenza danneggia il cervello
La maggior parte delle persone pensa all’influenza come a una settimana di febbre, tosse e riposo a letto. Tuttavia, in rari casi, soprattutto nei bambini, un’infezione influenzale di routine può improvvisamente degenerare in un disturbo cerebrale potenzialmente letale chiamato encefalopatia necrotizzante acuta (ANE). Famiglie e medici sospettano da tempo che i geni possano influire su chi sviluppa questa complicazione catastrofica. Questo studio svela come una singola proteina guardiana cellulare, RANBP2, normalmente tenga sotto controllo il virus influenzale e impedisca che la risposta infiammatoria dell’organismo sfugga di mano.
Una complicazione influenzale rara ma devastante
L’ANE compare bruscamente dopo una malattia febbrile, spesso influenzale, e può rapidamente causare convulsioni, coma e danni neurologici duraturi. Circa la metà degli episodi di ANE noti nel mondo è collegata al virus dell’influenza A, in particolare al ceppo H1N1. I bambini che ereditano determinate variazioni nel gene RANBP2 corrono un rischio molto più elevato, in una condizione nota come ANE1. Fino ad ora, però, gli scienziati non avevano compreso cosa faccia effettivamente questa proteina durante l’infezione influenzale, né perché una sua alterazione renda l’infiammazione cerebrale così grave.
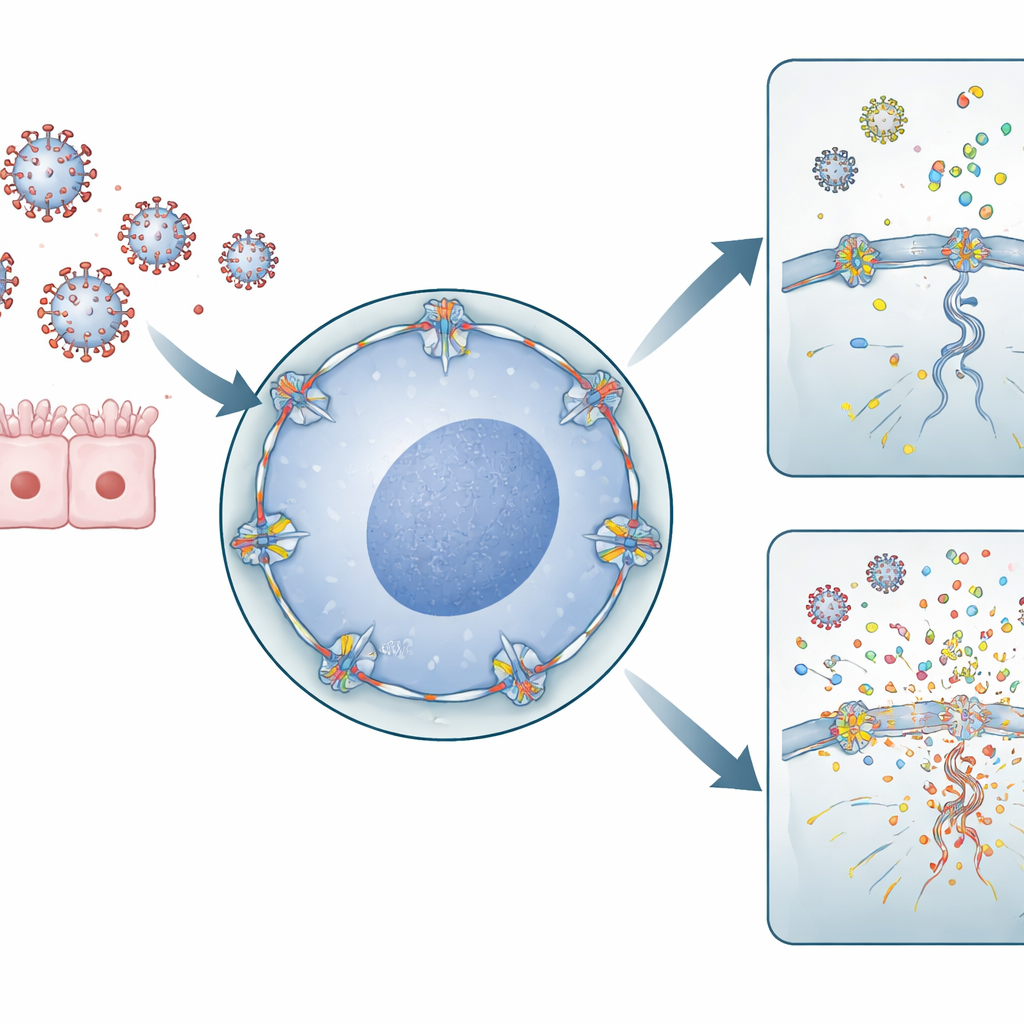
Porte cellulari e genomi virali
Il virus dell’influenza A ha uno stile di vita insolito per un virus a RNA: deve entrare nel nucleo della cellula per copiare il proprio materiale genetico. Per farlo passa attraverso i pori nucleari—ampie porte nella membrana nucleare che controllano il traffico tra il nucleo e il citoplasma circostante. RANBP2 è un componente principale sul lato esterno di questi pori. Gli autori hanno usato cellule umane derivate dal polmone e cellule del sistema immunitario per ridurre i livelli di RANBP2 o introdurre la mutazione associata all’ANE. Hanno scoperto che quando RANBP2 mancava o era mal riposizionata, i genomi influenzali venivano copiati in misura maggiore all’interno del nucleo e i segmenti genetici virali venivano esportati nel citoplasma in modo sbilanciato. Sorprendentemente, questo eccesso di RNA virale non ha prodotto più particelle infettive, ma ha modificato il luogo e il modo in cui il materiale virale si accumulava all’interno della cellula.
Quando i detriti virali alimentano il sistema d’allarme
Il sistema immunitario si basa su sensori molecolari che rilevano frammenti di RNA virale nel citoplasma come segnali di pericolo. Il gruppo ha dimostrato che, nelle cellule prive di RANBP2 normale, segmenti virali extra si accumulavano nel citoplasma, creando esattamente i tipi di pattern che questi sensori riconoscono. Nelle cellule derivate dal polmone ciò ha scatenato livelli più alti di molecole infiammatorie come IL‑6 e IL‑1β. Nei macrofagi umani primari—cellule immunitarie di prima linea ricavate da donatori di sangue—la perdita di RANBP2 ha portato a un marcato aumento di chemochine pro‑infiammatorie, tra cui CXCL8, CXCL10, CCL2, CCL3 e CCL4. Questi messaggeri chimici reclutano e attivano ulteriori cellule immunitarie, amplificando la reazione complessiva all’infezione.
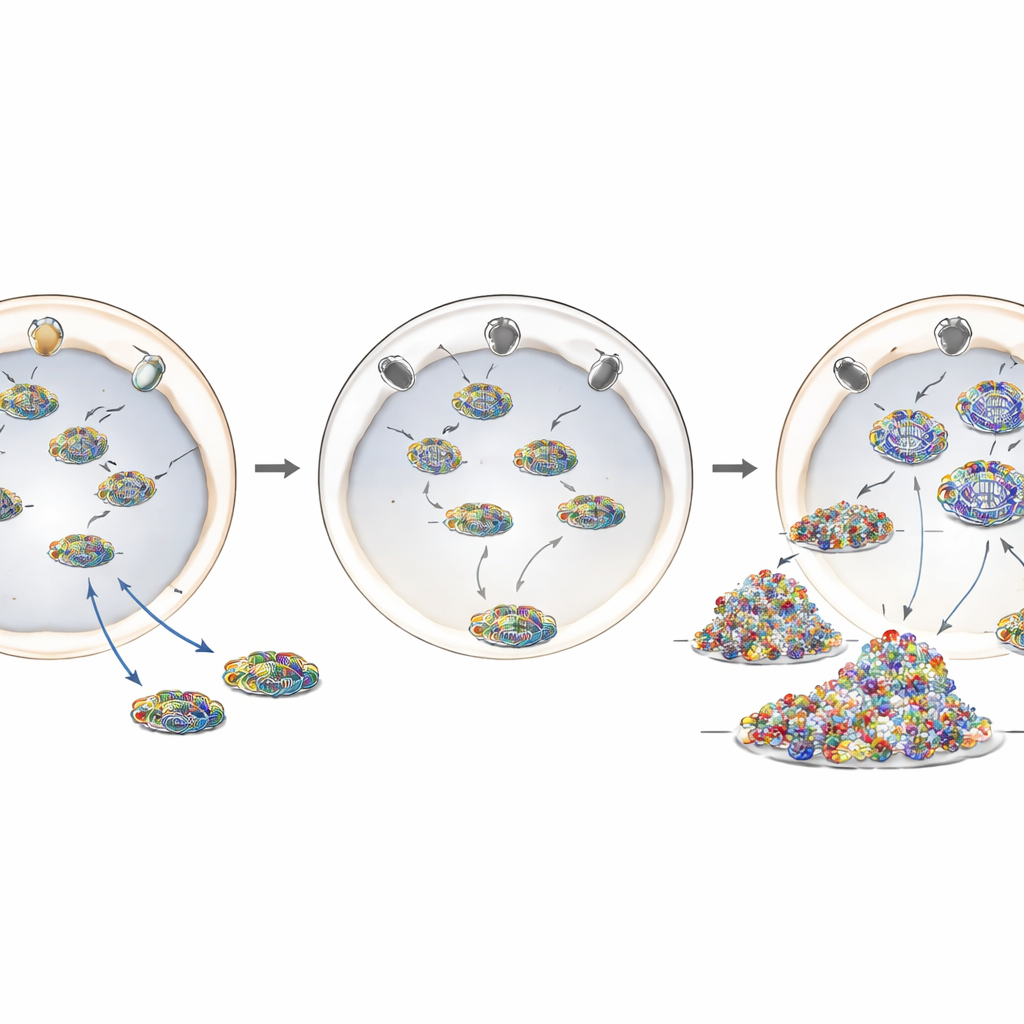
Una mutazione di malattia che sposta una guardiana
Per modellare più da vicino l’ANE1, i ricercatori hanno usato l’editing genomico CRISPR‑Cas9 per introdurre la variazione associata alla malattia più comune, T585M, nel gene umano RANBP2. In queste cellule modificate, i livelli di proteina RANBP2 erano per lo più normali, ma la sua posizione non lo era: invece di formare un bordo luminoso attorno alla membrana nucleare, gran parte della proteina risultava spostata all’interno della cellula. Le cellule portatrici di questa mutazione, sia in una che in entrambe le copie geniche, si comportavano in modo molto simile alle cellule deplete di RANBP2. Favorivano una maggiore replicazione del genoma influenzale, mostravano più materiale virale nel citoplasma e scatenavano una risposta infiammatoria più intensa dopo l’infezione. Ciò suggerisce che il corretto posizionamento di RANBP2 ai pori nucleari—piuttosto che la sua abbondanza complessiva—è cruciale per il suo ruolo protettivo.
Perché questo è importante per i bambini a rischio
Nel loro insieme, i risultati dipingono RANBP2 come una guardiana cellulare che regola finemente come il materiale genetico dell’influenza si muove dentro e fuori dal nucleo. Quando RANBP2 è assente o mal localizzata, l’RNA virale viene sovra‑replicato ed esportato in modo caotico, intasando il citoplasma di detriti molecolari che intensificano fortemente la segnalazione immunitaria. Per la maggior parte dei tessuti, questo può significare un attacco influenzale più severo ma superabile. Nei bambini vulnerabili con ANE1, tuttavia, tale infiammazione incontrollata—soprattutto se raggiunge il cervello—può contribuire a spiegare il danno neurologico improvviso e grave osservato dopo infezioni altrimenti ordinarie. Comprendere questa via potrebbe orientare strategie future per identificare precocemente i pazienti a rischio e per modulare i trattamenti anti‑infiammatori prima che la risposta immunitaria passi dall’essere protettiva al diventare distruttiva.
Citazione: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Parole chiave: influenza, encefalopatia necrotizzante acuta, RANBP2, iperinfiammazione, pori nucleari