Clear Sky Science · it
La classe II del MHC funziona come recettore d’ingresso specifico per ospite per rappresentativi virus dell’influenza A H3N2 umani e suini
Perché questo studio sull’influenza è importante
L’influenza stagionale sembra familiare, ma il virus che la causa è in costante ricerca di nuovi modi per infettare le nostre cellule e saltare tra specie. Questo studio rivela che un ceppo comune di virus influenzale, l’H3N2, può usare non solo la sua via classica d’ingresso nelle cellule ma anche una seconda porta inaspettata che differisce tra esseri umani e suini. Comprendere questa via alternativa d’ingresso aiuta a spiegare come l’influenza si adatti a nuovi ospiti e potrebbe migliorare il modo in cui sorvegliamo e ci prepariamo contro ceppi con potenziale pandemico. 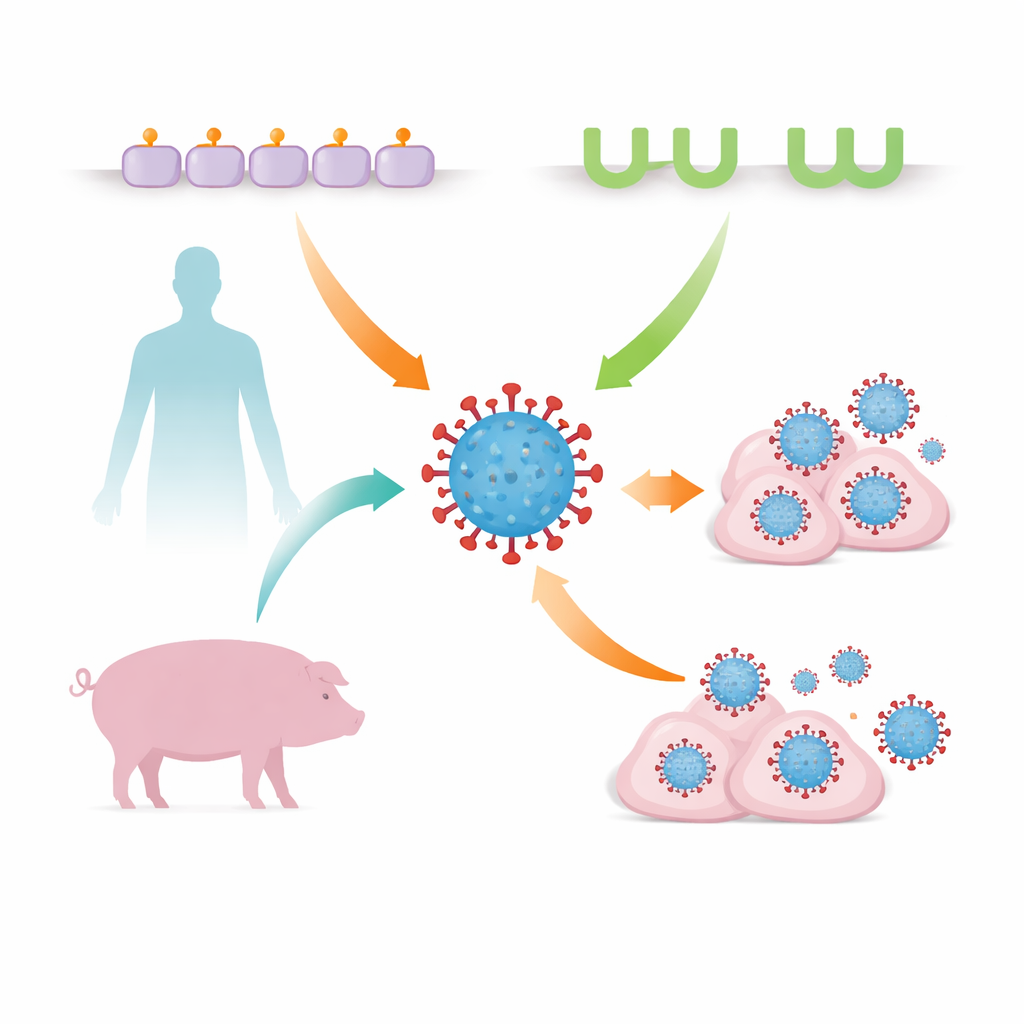
La via usuale con cui l’influenza entra
Per decenni i ricercatori hanno saputo che i virus dell’influenza A tipicamente entrano nelle cellule ancorandosi a molecole zuccherine chiamate acidi sialici che rivestono la superficie cellulare. L’«uncino» virale, una proteina chiamata emagglutinina, riconosce forme e legami specifici di questi zuccheri, che variano tra uccelli, esseri umani e altri animali. Piccole modifiche nell’emagglutinina possono spostare la preferenza per certi zuccheri, aiutando un virus aviario ad adattarsi ai mammiferi. Recentemente, però, sono stati trovati insoliti virus influenzali di pipistrelli e anatre che ignorano del tutto gli acidi sialici e usano invece una proteina chiamata MHC classe II come porta d’ingresso, suggerendo che il nostro quadro dell’ingresso virale era incompleto.
Appare una seconda porta
Il nuovo lavoro mostra che anche virus H3N2 più familiari possono usare la MHC classe II come via alternativa d’ingresso, oltre agli acidi sialici. La MHC classe II normalmente aiuta le cellule immunitarie a esporre frammenti di agenti patogeni per allertare il sistema immunitario. Il team si è concentrato su due virus strettamente correlati costruiti sullo stesso impianto genetico: uno simile a un ceppo stagionale H3N2 umano (hVIC/11) e un altro adattato ai suini (sOH/04). Nei polmoni suini, il virus adattato ai suini è stato trovato strettamente associato a cellule ricche di MHC classe II suina, in particolare macrofagi alveolari—cellule immunitarie di prima linea nelle sacche d’aria del polmone—suggerendo che questa molecola potrebbe agire come una maniglia che il virus può afferrare.
Disabilitare una porta per testare l’altra
Per verificare se la MHC classe II agisce realmente come recettore d’ingresso indipendente, i ricercatori hanno chimicamente rimosso gli acidi sialici dai macrofagi suini e da linee cellulari umane ingegnerizzate. Quando sono stati tolti solo gli zuccheri classici, entrambi i virus hanno comunque realizzato un’infezione parziale. Ma quando gli acidi sialici sono stati rimossi e la MHC classe II è stata contemporaneamente bloccata con anticorpi, l’infezione è calata drasticamente, soprattutto per il virus adattato ai suini. In cellule renali e polmonari umane rese geneticamente incapaci di produrre acidi sialici, l’aggiunta della versione umana di MHC classe II ha permesso un’infezione efficiente del virus simile a quello umano, mentre l’aggiunta della versione suina ha favorito il virus suino. Il trattamento delle cellule con farmaci che impediscono l’acidificazione dei compartimenti intracellulari ha inoltre bloccato questa infezione mediata dalla MHC, indicando che una volta entrato il virus segue la stessa via interna dell’ingresso influenzale standard. 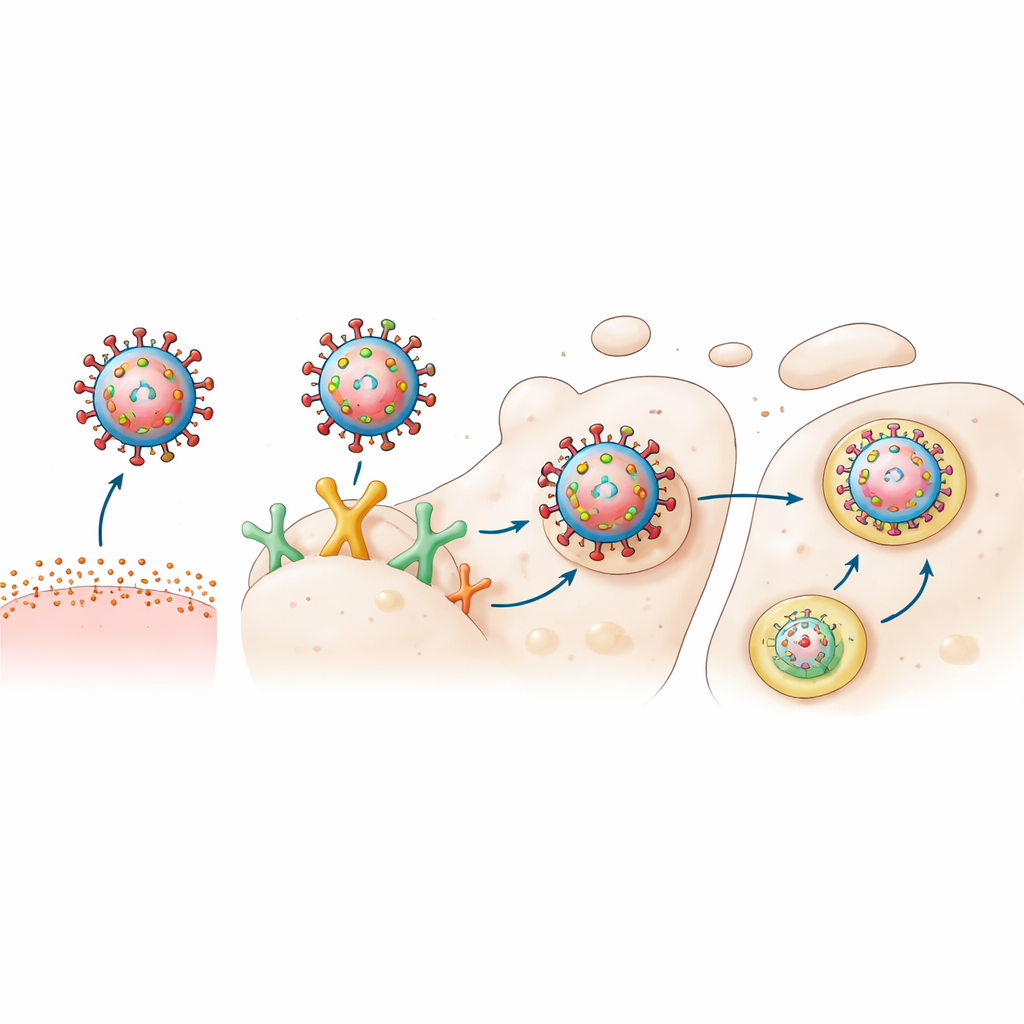
Come piccole variazioni aiutano il virus a cambiare ospite
Gli autori si sono poi chiesti quali parti dell’emagglutinina virale controllino questo nuovo tipo di legame. Lavori precedenti avevano mostrato che quando un virus H3N2 umano passa attraverso i suini spesso acquisisce certe mutazioni puntiformi vicino, ma non direttamente dentro, la tasca di legame per gli acidi sialici. Sono stati testati virus portatori di una qualsiasi di tre tali mutazioni (nelle posizioni etichettate 138, 186 o 193 nella proteina). Questi virus mutanti potevano usare sia la MHC classe II umana sia quella suina per entrare in cellule prive di acidi sialici e in alcuni saggi preferivano persino la versione suina. Allo stesso tempo, queste stesse mutazioni hanno modificato l’affinità dei virus per acidi sialici di tipo umano o aviario. In altre parole, aggiustamenti vicino al sito di legame per gli zuccheri possono modulare sia il recettore classico sia quello nuovo contemporaneamente, dando al virus flessibilità durante l’adattamento a una nuova specie.
Cosa significa per l’influenza e le minacce future
Complessivamente, i risultati mostrano che i comuni virus influenzali H3N2 non sono vincolati a un unico tipo di «maniglia» sulla superficie cellulare: possono usare sia gli acidi sialici sia la MHC classe II, e lo fanno in modo che rispecchia se il virus è meglio adattato agli esseri umani o ai suini. Durante le prime fasi di adattamento a un nuovo ospite, un virus può temporaneamente coinvolgere la MHC classe II di entrambe le specie, ampliando il suo intervallo di bersagli e aiutandolo a stabilirsi. Poiché la MHC classe II è abbondante su cellule immunitarie chiave nel polmone, questa via alternativa potrebbe permettere all’influenza di attaccare selettivamente cellule destinate a difenderci, favorendo potenzialmente la diffusione virale e la malattia. Riconoscere la MHC classe II come recettore d’ingresso specifico per ospite aggiunge un tassello importante al puzzle di come l’influenza attraversa le barriere tra specie e sottolinea la necessità di monitorare non solo il legame con gli zuccheri ma anche i recettori proteici quando si valuta il rischio pandemico di ceppi emergenti.
Citazione: Cardenas, M., Compton, S., Caceres, C.J. et al. MHC class II functions as a host-specific entry receptor for representative human and swine H3N2 influenza A viruses. Nat Commun 17, 2560 (2026). https://doi.org/10.1038/s41467-026-69267-6
Parole chiave: influenza A H3N2, recettori di ingresso virali, MHC classe II, adattamento all’ospite, trasmissione zoonotica