Clear Sky Science · it
Assemblaggio asimmetrico di 4-alchil-butenolidi catalizzato da una flavoenzima trifunzionale nella biosintesi dell’avenolide
Perché i piccoli anelli batterici contano per noi
Molti farmaci salvavita, dai antiparassitari ai prodotti per la protezione delle colture, dipendono da un piccolo motivo chimico chiamato butenolide. Oggi questi anelli sono per lo più prodotti a partire da materie prime derivate dal petrolio attraverso processi industriali multi‑step che consumano energia e generano rifiuti. Questo studio rivela come i batteri del suolo costruiscono uno di questi anelli, un ormone chiamato avenolide che attiva la produzione dei potenti antiparassitari avermectine. Capire questa via naturale indica strade più pulite e meno costose per ottenere sostanze utili e potrebbe aiutare a scoprire nuovi antibiotici.
L’anello speciale al centro di molti farmaci
I butenolidi sono anelli compatti a cinque membri che i chimici apprezzano perché reagiscono in modi versatili e compaiono in molti prodotti naturali e farmaci moderni. Contribuiscono a definire molecole con attività antitumorale, antifungina, antinfiammatoria e insetticida impiegate in medicina e agricoltura. Tuttavia, le sintesi tradizionali di questi anelli richiedono generalmente diversi passaggi attentamente controllati, catalizzatori costosi e materie prime petrolchimiche. Questa combinazione aumenta i costi e l’impatto ambientale, spingendo i ricercatori a cercare scorciatoie biologiche che la natura ha già perfezionato.
Un ormone batterico che attiva un farmaco blockbuster
Nel batterio del suolo Streptomyces avermitilis, la molecola contenente butenolide avenolide agisce come un minuscolo ormone. A concentrazioni estremamente basse si lega a una proteina regolatrice e rimuove il freno molecolare sui geni che sintetizzano le avermectine, potenti agenti che paralizzano vermi parassiti e alcuni insetti. Lavori genetici precedenti avevano suggerito che due enzimi, chiamati SavA e SavB, costruiscono l’avenolide, ma i passaggi effettivi erano sconosciuti. Il gruppo ha prima trasferito i geni rilevanti in un parente più collaborativo, Streptomyces albidoflavus, e ottimizzato le condizioni di crescita fino a ottenere dallo ceppo ingegnerizzato quantità milligrammo di avenolide puro—quanto basta per esaminare il percorso in dettaglio. 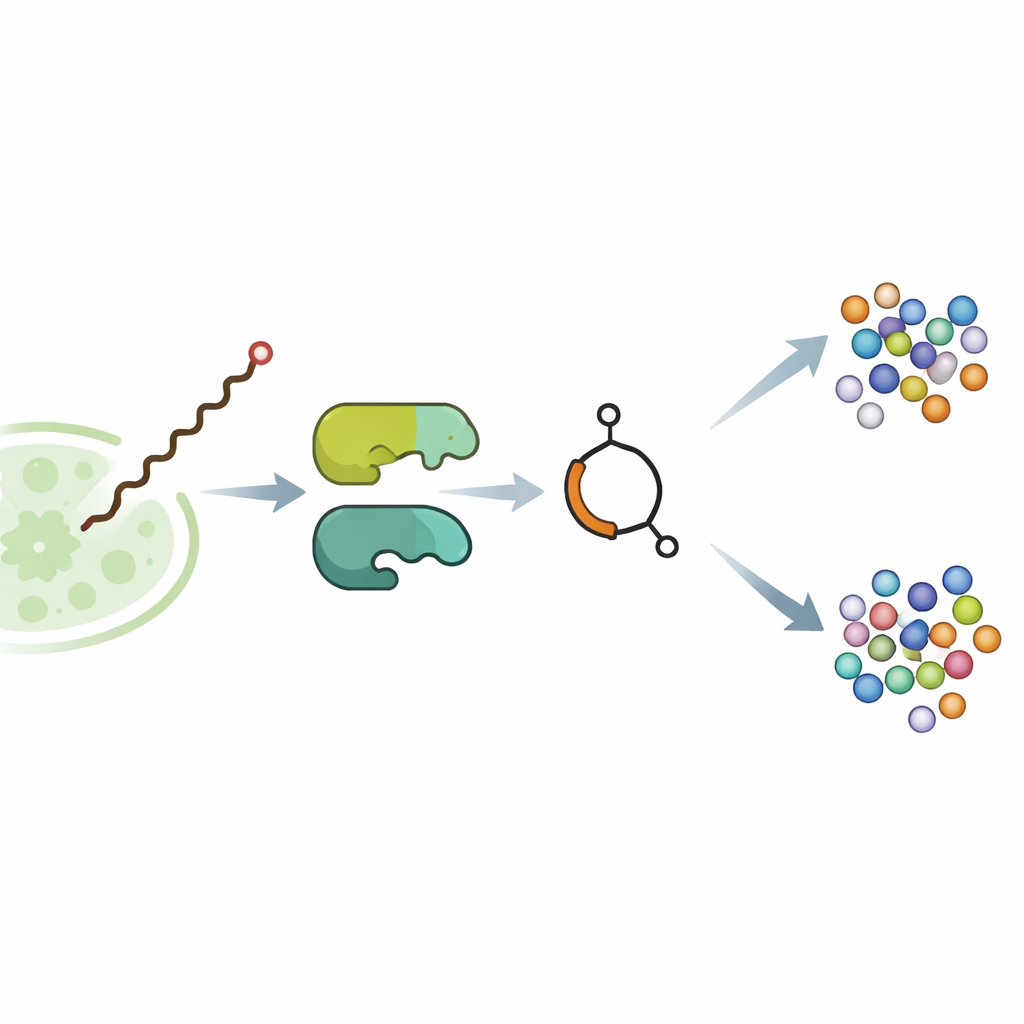
Un singolo enzima che compie tre reazioni consecutive
La sorpresa centrale dello studio è SavA, un enzima contenente flavina che esegue tre trasformazioni chimiche distinte su un frammento di partenza simile a un acido grasso prelevato dal metabolismo cellulare normale. Lavorando in reazioni in provetta con substrati modello sintetizzati ad hoc, i ricercatori hanno dimostrato che SavA prima rimuove atomi di idrogeno per introdurre un doppio legame, poi aggiunge un gruppo contenente ossigeno in una posizione specifica e infine favorisce la chiusura della catena nell’anello butenolide. Esperimenti con isotopi usando ossigeno gassoso arricchito con una forma più pesante di ossigeno hanno confermato che l’ossigeno dell’anello proviene direttamente dall’aria. Modellizzazione strutturale e mutazioni mirate hanno individuato un singolo amminoacido come base che dà inizio alla reazione e hanno rivelato come il cofattore flavinico legato cicli tra forme ossidate e ridotte senza mai essere consumato.
Un enzima finale che rifinisce la catena laterale
Una volta che SavA ha costruito l’impalcatura butenolide chirale, SavB—un citocromo P450—subentra per decorare la catena di carbonio attaccata. In presenza dei suoi partner redox e di un comune cofattore cellulare, SavB esegue una serie precisa di ossidazioni su due atomi di carbonio adiacenti. Analisi risolte nel tempo hanno messo in luce due molecole intermedie: prima un prodotto monoidrossilato, poi una forma chetonica, prima che compaia l’avenolide completamente funzionale. Misure con risonanza magnetica nucleare hanno confermato le posizioni e gli arrangiamenti tridimensionali di questi nuovi gruppi. Il lavoro mostra che SavB introduce questi atomi di ossigeno in un ordine definito e con controllo rigoroso sull’orientazione, caratteristica cruciale per l’attività biologica dell’ormone. 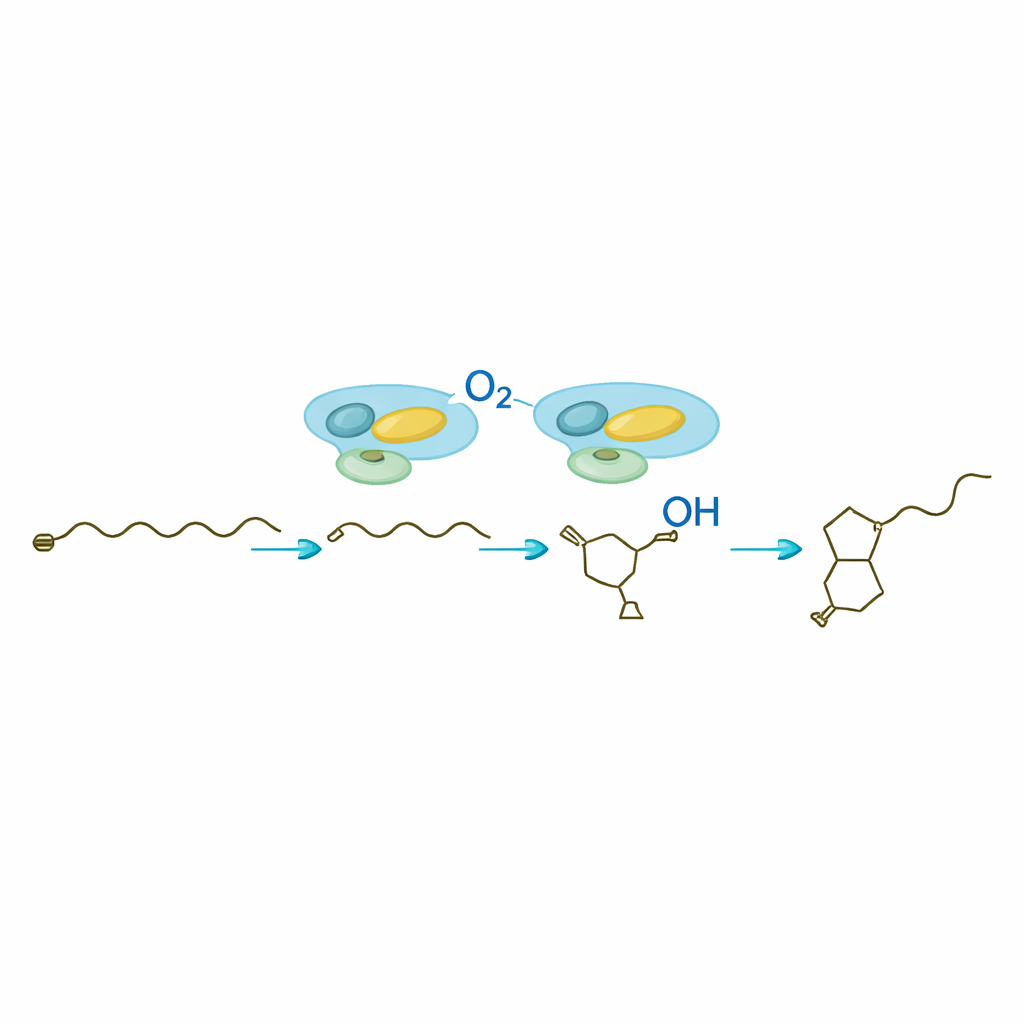
Lezioni di chimica sostenibile dagli enzimi batterici
Insieme, SavA e SavB convertono un comune blocco di partenza derivato dagli acidi grassi in una molecola di segnalazione finemente regolata usando solo l’ossigeno dell’aria e gli aiutanti cellulari standard. A differenza di molti processi industriali, SavA non ha bisogno di agenti riducenti extra o reagenti sacrificabili; il suo cofattore flavinico semplicemente trasporta elettroni mentre è il substrato stesso a fornire la forza motrice. Gli autori evidenziano SavA come un nuovo tipo di flavoenzima polivalente con forte potenziale come biocatalizzatore per la produzione sostenibile di butenolidi e motivi correlati. In termini pratici, sfruttare o ingegnerizzare enzimi di questo tipo potrebbe un giorno consentire a impianti industriali—o a microrganismi ingegnerizzati—di produrre frammenti di farmaci e prodotti agricoli importanti a partire da materie prime rinnovabili in condizioni miti, riducendo sia i costi sia l’impronta ambientale.
Citazione: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Parole chiave: biosintesi dei butenolidi, flavoenzima SavA, ormone avenolide, biocatalisi, segnalazione di Streptomyces