Clear Sky Science · it
Ingegnerizzazione dell'orbitale d degli atomi singoli di rame verso la metanazione elettrocatalitica a livello industriale
Trasformare i gas di scarico delle centrali in carburante
La combustione di carbone e gas per produrre elettricità rilascia enormi quantità di anidride carbonica in atmosfera, alimentando il cambiamento climatico. Questo studio esplora un'idea emergente: invece di considerare la CO2 semplicemente come rifiuto, possiamo usare l'elettricità per riconvertirla in carburante ad alta densità energetica direttamente in centrale? I ricercatori si concentrano sulla conversione della CO2 in metano, il componente principale del gas naturale, usando un catalizzatore altamente efficiente e durevole a base di rame e ossido di titanio. L'obiettivo è raggiungere prestazioni adatte all'industria, non solo al laboratorio.
Perché il metano derivato dalla CO2 conta
Molte centrali esistenti continueranno a funzionare per anni, in particolare le centrali a carbone oltreoceano che attualmente emettono centinaia di milioni di tonnellate di CO2 all'anno. Catturare questa CO2 e convertirla elettrochimicamente in metano offre un modo per ridurre le emissioni e al contempo produrre un combustibile utilizzabile. Il metano è interessante perché immagazzina molta energia e può essere bruciato nelle turbine e nelle infrastrutture del gas esistenti. Tuttavia, la maggior parte dei catalizzatori a base di rame attuali che trasformano la CO2 in metano è troppo lenta, spreca molta energia o si degrada sotto le correnti elevate richieste dai dispositivi reali.
Progettare un sito di rame più intelligente
Il cuore di questo lavoro è un nuovo tipo di catalizzatore a singolo atomo di rame, in cui atomi isolati di rame sono ancorati su un supporto solido invece di raggrupparsi in particelle. Il team usa l'ossido di titanio come supporto e rimuove deliberatamente alcuni atomi di ossigeno dalla sua rete cristallina, creando piccole “vacanze” che modificano l'interazione con gli atomi metallici vicini. Trattando con cura un ossido di titanio drogato con rame in idrogeno, ottengono un composto che gli autori chiamano Cu–Ti1O3, dove singoli atomi di rame si trovano accanto ad atomi di titanio e condividono elettroni direttamente. Queste coppie rame–titanio si comportano in modo molto diverso dai siti di rame convenzionali circondati principalmente da ossigeno.
Come le piccole vacanze controllano la reazione
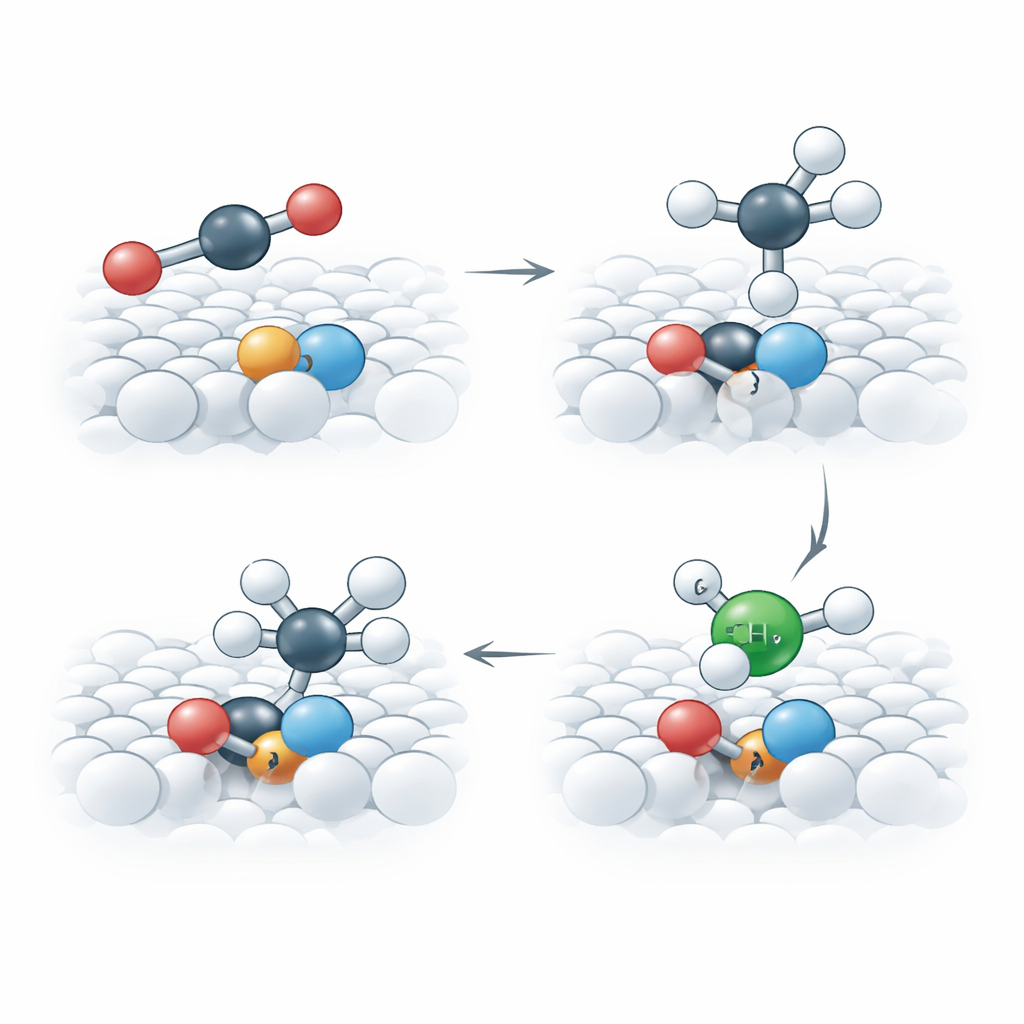
Simulazioni avanzate e misure sperimentali rivelano cosa rende speciali questi siti di rame ingegnerizzati. La mancanza di atomi di ossigeno favorisce un forte legame elettronico tra rame e titanio, che rende il rame più localizzato e “duro” in termini chimici. Questo aiuta la CO2 ad adsorbirsi in una forma piegata e attivata e stabilizza un intermedio critico della reazione contenente carbonio, ossigeno e idrogeno. Lo studio mostra che l'ossigeno di questo intermedio può temporaneamente spostarsi nella vacanza vicina, comportandosi come una parte reversibile della rete cristallina. Questa astuta riorganizzazione facilita la rottura del legame carbonio–ossigeno e il proseguimento della sequenza di passaggi che porta al metano, senza danneggiare il catalizzatore stesso.
Dalla teoria alle prestazioni a scala industriale
Per verificare se questi miglioramenti microscopici contano nella pratica, i ricercatori costruiscono reattori a flusso e un elettrolizzatore a gap zero simili ai sistemi in sviluppo per l'industria. In soluzione alcalina, il catalizzatore Cu–Ti1O3 converte la CO2 in metano con un'efficienza faradica di circa tre quarti, il che significa che la maggior parte della corrente di ingresso viene indirizzata al metano piuttosto che a prodotti secondari indesiderati come l'idrogeno. Raggiunge inoltre tassi di produzione di metano molto elevati—molto superiori a molti catalizzatori di rame precedenti—pur utilizzando l'elettricità in modo efficiente. Forse più impressionante, in una cella più grande da 5 cm² funzionante a correnti di livello industriale, il catalizzatore mantiene un'alta selettività verso il metano per più di 1.200 ore, superando di gran lunga un catalizzatore di confronto a base di rame che si degrada rapidamente formando nanoparticelle di rame.
Implicazioni per centrali elettriche più pulite
In termini semplici, questo lavoro mostra che rimodellare il modo in cui gli elettroni sono condivisi attorno a singoli atomi di rame può trasformare un catalizzatore fragile e mediocre in una “macchina” veloce e durevole per convertire la CO2 in metano. Utilizzando vacanze di ossigeno nell'ossido di titanio per rafforzare la partnership rame–titanio, i ricercatori hanno sbloccato una via di reazione che favorisce il metano e protegge i siti attivi durante lunghi periodi di funzionamento. Sebbene nelle centrali reali intervengano molte ulteriori questioni ingegneristiche ed economiche, le prestazioni e la durabilità dimostrate suggeriscono che tali catalizzatori potrebbero costituire il nucleo di dispositivi futuri che riciclano la CO2 dei gas di scarico in carburante utile, facilitando il percorso verso un'elettricità a minore intensità di carbonio.
Citazione: Liu, Z., Cai, J., Dong, S. et al. Engineering d-orbital of copper single-atom sites toward industrial-level electrocatalytic methanation. Nat Commun 17, 2723 (2026). https://doi.org/10.1038/s41467-026-69260-z
Parole chiave: riduzione elettrocatalitica della CO2, carburante metano, catalizzatore a singolo atomo di rame, vacanze di ossigeno, decarbonizzazione delle centrali elettriche