Clear Sky Science · it
Attivazione cooperativa dell’anione su un centro di cobalto tramite accoppiamento ionico e progettazione del ligando
Perché i piccoli partner attorno ai metalli contano
I chimici spesso si concentrano sul principale “protagonista” di una reazione — un atomo di metallo che aiuta a rompere e formare legami. Ma questo articolo mostra che i partner silenziosi che gli orbitano intorno, invisibili a occhio nudo, possono cambiare completamente il comportamento del metallo. Modellando con cura lo spazio intorno a un atomo di cobalto, gli autori rivelano come due anioni quasi intercambiabili, spesso considerati partecipanti passivi in chimica e nelle batterie, possano portare a esiti radicalmente diversi. 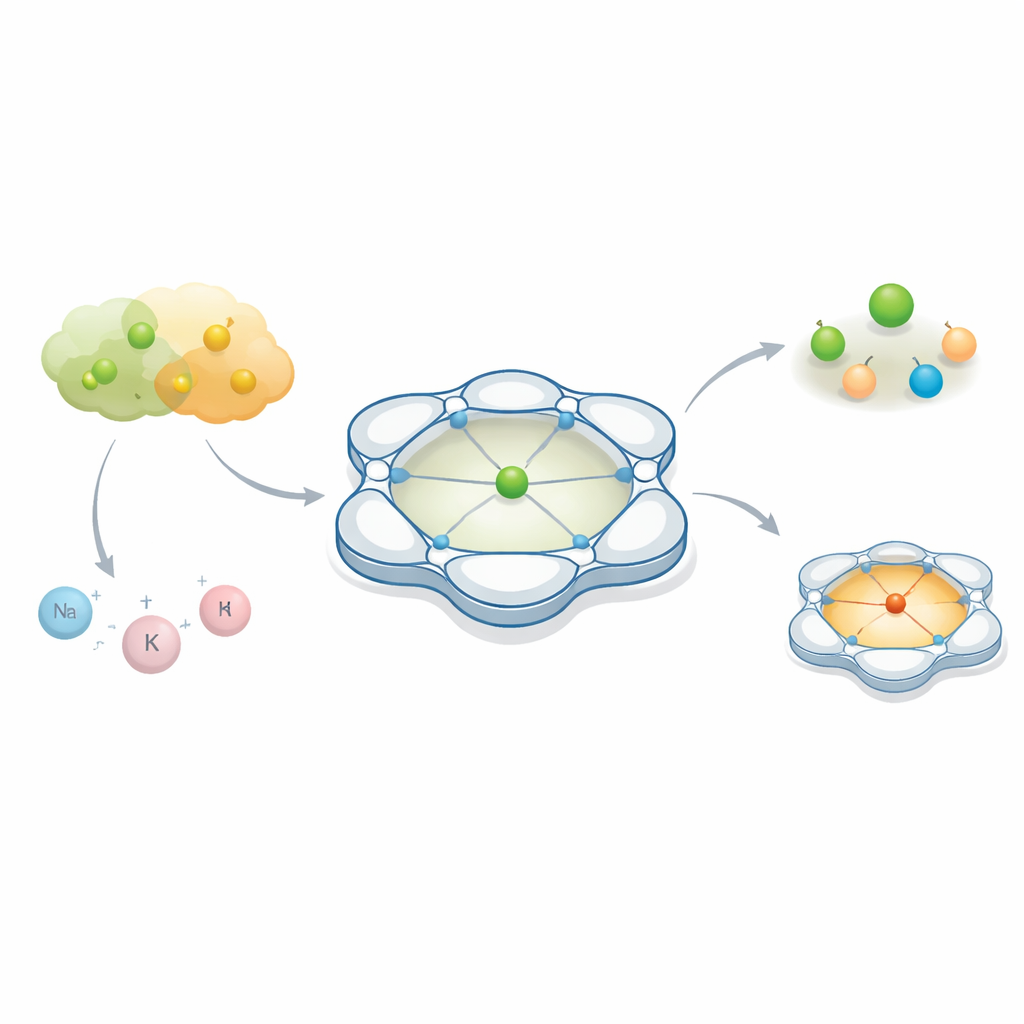
Costruire una tasca su misura attorno al cobalto
I ricercatori hanno progettato un impalcatura organica a forma di gabbia chiamata Py4Im che avvolge strettamente un ione di cobalto. Questa struttura è costruita da diversi anelli di piridina collegati e da un’unità di imidazolidina, che insieme creano una cavità rigida a forma di coppa contenente un singolo gruppo N–H. Questa piccola cavità è “protica”, nel senso che può formare legami idrogeno, e punta in una direzione specifica, come un piccolo porto d’attracco per gli anioni in arrivo. Quando il cobalto è assemblato con questo ligando, il risultato è una famiglia di complessi carichi positivamente la cui forma complessiva e tasca interna restano le stesse mentre il controione — il partner carico negativamente — può essere scambiato. Questo rende il sistema un banco di prova ideale per osservare come anioni diversi si comportino nello stesso ambiente controllato.
Due anioni simili, due comportamenti molto diversi
Il team ha confrontato due anioni d’uso comune, tetrafluoroborato (BF4−) e esafluorofosfato (PF6−), ampiamente impiegati come cosiddetti anioni debolmente coordinanti. Sono popolari perché generalmente mantengono le distanze dai centri metallici, aiutando a stabilizzare specie altamente cariche senza intervenire direttamente. Sorprendentemente, all’interno della cavità Py4Im non si comportano allo stesso modo. In condizioni miti, PF6− cede uno ione fluoruro al cobalto, rompendo un forte legame P–F e formando un complesso cobalto–fluoruro ben definito. Al contrario, BF4−, che di solito è considerato il più “fragile” dei due, si rifiuta di cedere fluoruro nello stesso contesto. Si dispone invece in un assetto stabile legato al centro di cobalto senza completare il passo di rottura del legame.
Osservare l’accoppiamento e il movimento degli ioni
Per comprendere questi comportamenti contrastanti, gli autori hanno utilizzato una combinazione di tecniche NMR ad alta risoluzione e calcoli quantomeccanici. Esperimenti di NMR di diffusione hanno misurato la velocità di moto delle specie positive e negative in soluzione, rivelando quanto strettamente siano accoppiate. Queste misurazioni hanno mostrato che BF4− forma una coppia ionica più vicina e persistente con il complesso di cobalto rispetto a PF6−. La cavità Py4Im posiziona l’anione direttamente sotto l’anello di imidazolidina, dove legami a idrogeno dal gruppo N–H e dai vicini gruppi C–H lo tengono in posizione. I calcoli al computer hanno confermato che questo accoppiamento più forte e direzionale con BF4− stabilizza così tanto lo stato di partenza che la rottura del legame B–F diventa lievemente sfavorita, nonostante quel legame sia intrinsecamente più debole rispetto al P–F di PF6−. PF6−, accoppiandosi più debolmente, può avvicinarsi, trasferire il fluoruro al cobalto e allontanarsi come PF5, portando a un complesso di cobalto contenente fluoruro che è accessibile termodinamicamente. 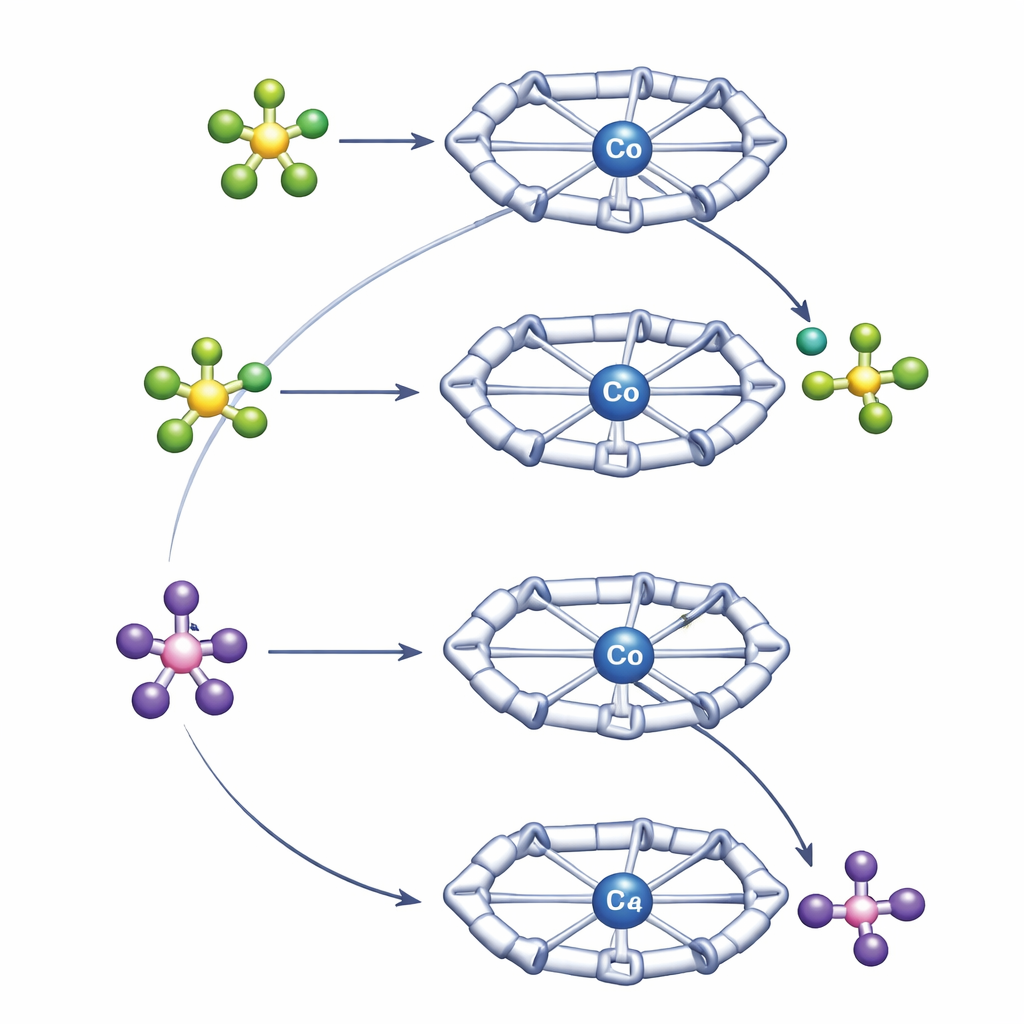
Trasformare un fluoruro legato in uno strumento utile
Una volta formato, il complesso cobalto–fluoruro non è una strada senza uscita. Gli autori dimostrano che si comporta come una sorgente nucleofila di fluoruro — in termini più semplici, può fornire fluoruro a partner carichi positivamente o elettron-poveri. In soluzione, questa specie cobalto–fluoruro trasferisce in modo pulito il fluoruro a centri carboniosi reattivi, ad atomi di silicio in clorosilani e ad acil cloruri, generando fluoruri organici mentre il complesso di cobalto ritorna alla sua forma cloruro o si lega al nuovo partner. In una mossa ingegnosa, il team mostra anche che BF4− può essere convinto a cedere fluoruro se è presente una base separata in grado di “catturare” il frammento BF3 che rimane. Ciò converte la via altrimenti restia di BF4− in una che produce anch’essa lo stesso prodotto cobalto–fluoruro.
Implicazioni per progettare catalizzatori più intelligenti
Per un non specialista, il messaggio chiave è che ioni una volta trattati come sali inerti di sfondo possono in realtà indirizzare reazioni chimiche in modi potenti. Scolpendo una tasca precisa attorno a un centro metallico e controllando quanto strettamente gli anioni si accoppiano con esso, gli autori hanno invertito la reattività attesa di due specie quasi identiche. PF6−, normalmente visto come molto robusto, diventa la fonte di fluoruro più facile, mentre BF4− è bloccato da un accoppiamento più forte a meno che il sistema non venga aiutato. Questo lavoro fornisce un progetto guida per usare insieme progettazione del ligando e scelta del controione per modulare la reattività di un complesso metallico — un’idea che potrebbe influenzare campi che vanno dalla catalisi omogenea alla progettazione di elettroliti per batterie avanzate, dove i “partner silenziosi” in soluzione potrebbero essere tutt’altro che passivi.
Citazione: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Parole chiave: complessi di cobalto, anioni debolmente coordinanti, trasferimento di fluoruro, accoppiamento ionico, progettazione del ligando