Clear Sky Science · it
Un solfuro di molibdeno metallico catalizza reti di reazioni protometaboliche dell’anidride carbonica in condizioni estreme
Come le rocce potrebbero aver avviato la chimica della vita
Molto prima che le cellule viventi evolvessero enzimi, la Terra aveva comunque bisogno di trasformare gas semplici come l’anidride carbonica in molecole organiche necessarie alla vita. Questo studio esplora se alcuni minerali naturali, simili a quelli trovati vicino alle sorgenti sottomarine, potrebbero aver funzionato da primitivi “motori chimici”. Dimostrando che una forma metallica del solfuro di molibdeno può convertire l’anidride carbonica in una rete sorprendentemente ricca di composti organici, il lavoro propone uno scenario concreto per come la chimica fondamentale della vita potrebbe essere iniziata su un pianeta privo di vita.

Camini caldi e motori chimici nascosti
La vita moderna si basa su reti complesse di reazioni che trasferiscono il carbonio attraverso cellule ed ecosistemi. Queste reti dipendono da proteine chiamate enzimi, a loro volta prodotti dell’evoluzione. La grande domanda è cosa ci fosse prima. Gli autori hanno guardato ai camini idrotermali—camini naturali di acqua calda sul fondo oceanico ricchi di solfuri metallici e di idrogeno—come ambienti probabili per la chimica carbonica più antica. In tali luoghi, acqua calda e pressurizzata incontra rocce contenenti metalli come ferro, nichel e molibdeno. Esperimenti precedenti hanno mostrato che alcuni di questi metalli possono trasformare l’anidride carbonica in piccoli composti organici, ma di solito solo lungo frammenti delle vie metaboliche, non in reti complete.
Un minerale che imita antichi enzimi
Il gruppo si è concentrato su una forma particolare di solfuro di molibdeno, chiamata fase 1T′, il cui ordine atomico imita i centri metallo-zolfo presenti negli enzimi moderni che processano l’anidride carbonica. A temperature e pressioni elevate in acqua, con l’idrogeno come carburante, questo minerale ha catalizzato la conversione dell’anidride carbonica disciolta (modellata come bicarbonato) in un’inaspettata ampia gamma di acidi organici. Variando con cura temperatura, tempo di reazione e pressione dei gas, e tracciando i prodotti con cromatografia, spettrometria di massa e RMN, hanno identificato 32 diversi intermedi e prodotti finali che emergono dalla stessa semplice sorgente di carbonio.
Ricostruire i principali percorsi del carbonio della vita senza enzimi
Questi 32 composti non sono casuali. Molti sono le stesse molecole che sono al centro del metabolismo moderno—come acetato, piruvato, ossalacetato, succinato e alfa-chetoglutarato. Collettivamente, si sovrappongono a cinque importanti vie di fissazione del carbonio usate dai microbi contemporanei: la via acetil–CoA e varianti del ciclo di Krebs e di anelli correlati. Negli esperimenti, queste vie sono apparse come una rete interconnessa: l’acetato collegava diversi cicli; molecole più grandi si rompevano e si riformavano; e intermedi chiave scomparivano e ricomparivano man mano che le condizioni cambiavano. La produzione di acidi policarboniosi ha raggiunto alta efficienza, con fino a circa il 70% del carbonio convertito che finiva in molecole contenenti due o più carboni. La rete di reazione ha mostrato anche oscillazioni in cui le quantità di certi prodotti aumentavano e diminuivano nel tempo, richiamando il comportamento dinamico dei sistemi chimici viventi.
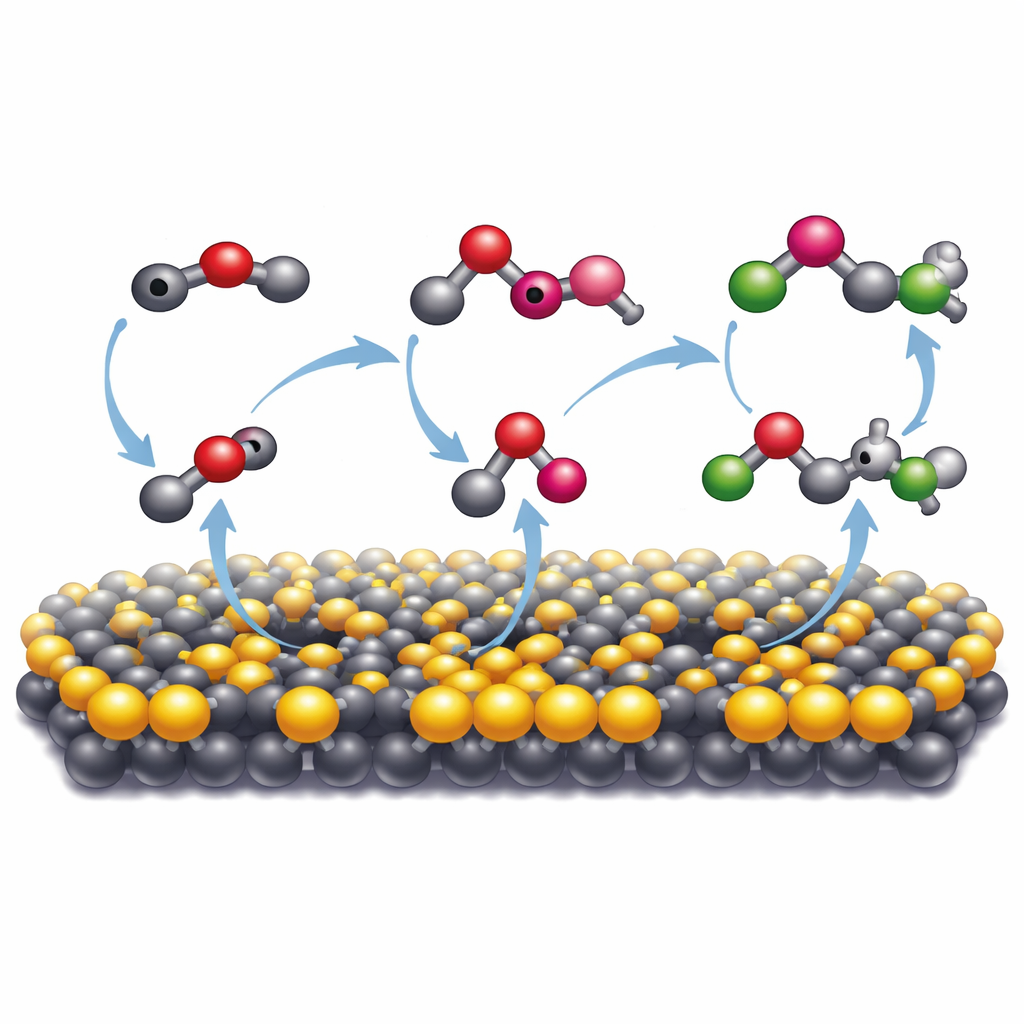
Come il minerale fa unirsi gli atomi di carbonio
Per capire perché questo particolare minerale fosse così efficace, i ricercatori lo hanno confrontato con una forma più comune di solfuro di molibdeno che ha una diversa struttura atomica. Solo la forma metallica e distorta—with molti atomi di zolfo mancanti—ha favorito l’estesa formazione di organici più grandi. Tecniche spettroscopiche hanno rivelato che su questa superficie il monossido di carbonio derivato dall’anidride carbonica si lega fortemente ed è ulteriormente ridotto in frammenti altamente reattivi, o radicali. Questi radicali sono stabilizzati quel tanto che basta sulla superficie minerale per incontrarsi e formare nuovi legami carbonio–carbonio. Misurazioni del spin elettronico hanno confermato la presenza di tali radicali, e l’aggiunta di una sostanza chimica “trappola” per radicali ha fortemente soppresso i prodotti policarboniosi. Simulazioni al computer hanno supportato questo quadro, mostrando che le vacanze di zolfo e la struttura elettronica alterata della fase 1T′ rendono più facile per la superficie donare elettroni e avvicinare frammenti di carbonio in modo che possano combinarsi.
Dalla chimica delle rocce al primo metabolismo
Messo insieme, questi risultati suggeriscono che certi solfuri metallici sulla Terra primordiale potrebbero aver alimentato una chimica carbonica complessa e auto-organizzante molto prima dell’esistenza di enzimi. In ambienti di camini idrotermali, dove fluidi caldi ricchi di idrogeno incontrano anidride carbonica e rocce contenenti metalli, un minerale come il solfuro di molibdeno 1T′ potrebbe aver continuamente convertito il carbonio inorganico in una rete di vie organiche interconnesse simili ai cicli metabolici moderni. Per un non specialista, il messaggio chiave è che la chimica centrale della vita potrebbe non aver avuto bisogno della vita per iniziare: nelle condizioni giuste, rocce semplici, acqua e gas possono spontaneamente costruire molte delle stesse molecole e anelli di reazione che le cellule viventi usano ancora oggi.
Citazione: Chen, P., Liu, X., He, D. et al. Metallic molybdenum sulfide catalyses protometabolic carbon dioxide reaction networks under extreme conditions. Nat Commun 17, 2395 (2026). https://doi.org/10.1038/s41467-026-69255-w
Parole chiave: origine della vita, chimica prebiotica, camini idrotermali, fissazione del carbonio, solfuro di molibdeno